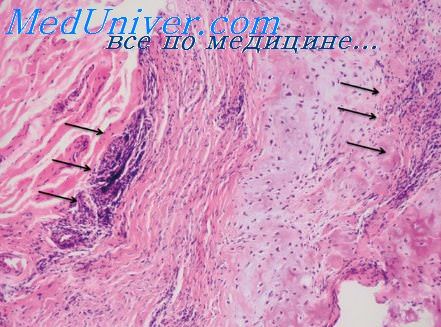
Фиброзирующий альвеолит при ревматоидном артрите
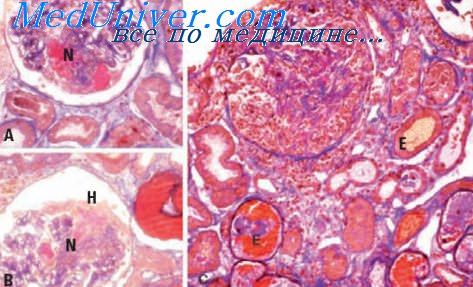
Фиброзирующий альвеолит при ревматоидном артрите. Морфология ревматоидного альвеолитаГистологические изменения в легких зависят от активности воспалительного процесса. В острой стадии характерны резко выраженная круглоклеточная инфильтрация стенок альвеол и иногда весьма заметное лимфоидпое скопление с зародышевыми фолликулами, продуцирующими IgG и IgM [Turner-Warwick, 1967]. В отдельных случаях наблюдается типичная десквамационная интерстициальная пневмония и у этих больных были обнаружены большие отложения фибрина. Чаще однако выявляются изменения стенок с фиброзом, деструкция архитектоники альвеол и бропхоэктазы. В одном или двух случаях, наблюдавшихся путем повторных рентгенологических исследований грудной клетки, от момента появления первых изменений бропхоэктазы образовались быстро, возможно, этим объясняется отсутствие эффекта от кортикостероидной терапии, отмечаемое всеми авторами. Есть основания полагать, что интерстициальные поражения легких при ревматоидном артрите чаще встречаются у мужчин, чем у женщин. То же самое подтвердилось на пашем материале. Фиброзирующий альвеолит при ревматоидном артрите имеет такие же клинические признаки, как и «изолированный криптогенный фиброзирующий альвеолит», — тонкие крепитации, пальцы в форме барабанных палочек и функциональный рестриктивный дефект. Эти явления наблюдаются в том же проценте случаев. Согласно прежним сообщениям, легкие могут быть поражены в любое время на протяжении естественного течения ревматоидного артрита [Patterson et al., 1965].
Из наших 39 больных у большинства (71%) легочные поражения появились в течение 4 лет после первого суставного симптома, хотя иногда они возникают через много лет после развития таких симптомов. Если легкие поражаются в первую очередь, то средняя продолжительность легочных симптомов до вовлечения суставов равна 3 годам [Turner-Warwick, Courtenay-Exans, 1977]. Tomasi и соавт. (1962) полагают, что легкие вовлекаются главным образом у больных с подкожными узелками и высокими титрами ревматоидного фактора. Patterson и соавт. (1965) из 705 больных ревматоидным артритом обнаружили рентгенографическую картину фиброзирующего альвеолита у 9 человек (т. е. примерно у 1 из каждых 70); у 6 были подкожные узелки, причем титры ревматоидного фактора оказались высокими. В пашей первой группе из 16 больных у 8 (50%) были обнаружены подкожные узелки и ДРА в титрах 1 : 128 и выше. Прогрессирование легочных поражений не всегда параллельно прогрессированию суставного заболевания [Patterson et al., Stack, Grant, 1965]. Это важно отметить, поскольку указанный факт означает, что при поражении более чем одного органа больных часто направляют к разным специалистам, и, очевидно, будут описаны разные формы болезни. Мы подчеркивали ото, говоря о системной красной волчанке и поражениях легких, и можем лишь повторить уже сказанное в отношении ревматоидного артрита. — Также рекомендуем «Иммунология фиброзирующего альвеолита при ревматоидном артрите. Механизмы развития фиброзирующего альвеолита» Оглавление темы «Легкие при системных заболеваниях»: |
Источник
Иммунология фиброзирующего альвеолита при ревматоидном артрите. Механизмы развития фиброзирующего альвеолитаТесты иммунофлюоресценции, поставленные в 6 случаях, выявили отложение IgG и IgM у 3 больных. Однако признаков комплемента, которые наблюдаются в некоторых других случаях фиброзирующего альвеолита, не было обнаружено. В легких были найдены плазматические клетки и зародышевые фолликулы, содержащие IgG и IgM [Turner-Warwick, 1967]. Кроме того, в плазматических клетках, но не в зародышевых фолликулах был выявлен ревматоидный фактор при помощи гамма-глобулина, меченного флюоресцеином. De Horarius и соавт. (1972) также обнаружили IgG и IgM без комплемента. По предположению авторов, отложения IgM состоят из ревматоидного фактора, связанного с иммунными комплексами, причем содержание комплемента в них слишком мало для того, чтобы его можно было выявить методом иммунофлюоресценции. Это мнение поддерживается точной корреляцией между повышенным связыванием сывороточного Clq и наличием циркулирующего ревматоидного фактора [Mohammed et al., 1977], а также данными экспериментальных исследований [Abruzzo, Christian, 1961]. Наряду с этим против такого предположения говорит невозможность обнаружить ревматоидный фактор в тех участках, где имеются отложения IgM. Можно выдвинуть и другую гипотезу: отложения IgG и IgM представляют собой агрегаты, образующиеся без комплемента, как описывают Tomasi и соавт. (1962), применявшие методы ультрацентрифугирования. Интересно, что отложения, найденные до настоящего времени в легких, видимо, не содержат комплемента, а в отложениях в синовиальной мембране он содержится [Bonomo et al., 1970]. Можно опять предположить, что разные ткани задерживают иммунные комплексы разного типа и, возможно, разных размеров. Ранее уже обсуждались различия в распределении иммунных комплексов в разных органах при системной красной волчанке. Возможно, что при ревматоидном артрите также имеют значение размеры решетки комплексов. Может различаться не только задержка комплексов в разных капиллярных системах, но и скорость клиренса из них.
Не решен вопрос и о том, имеют ли отложения IgG и IgM в легких патогенетическое значение. Установлено, что агрегаты гамма-глобулина активируют комплемент по альтернативному пути, и, возможно, что таким образом может быть вызвано и повреждение ткани. Необходимо рассмотреть также роль клеточного иммунитета. In vitro ставились тесты на сенсибилизацию лимфоцитов, причем антигеном служил денатурированный нагреванием гамма-глобулин и изучалось торможение миграции лейкоцитов [Brostoff et al., 1973]. Какова бы ни была первопричина денатурирования гамма-глобулина, но как только оно произошло, клеточный иммунный ответ может способствовать дальнейшему местному повреждению тканей. Таким образом, в связи с патогенезом легочных поражений необходимо рассматривать также роль сенсибилизированных лимфоцитов, как и образование иммунных комплексов. Эта роль имеет не только теоретическое значение, но она важна и при выборе более рациональной терапии. В любом обсуждении патогенеза внимание уделяется прежде всего денатурированному глобулину и ревматоидному фактору, однако существует предположение и о совершенно иных механизмах. Одна интересная возможность — это аутоаллергическая ПЧЗТ к гомологичному, быть может, измененному коллагену. Steffen и Wick (1971) высказали это предположение на основании опытов па животных, так же как Dumonde и Glynn (1962), которые пользовались в качестве антигена человеческим фибрином. Дальнейшим подтверждением могут служить недавно обнаруженные антиколлагеновые антитела у больных фиброзирующим альвеолитом [Kravis ot al., 1976]. — Также рекомендуем «Легочные кровоизлияния. Гемосидероз при системной красной волчанке и синдром Гудпасчера» Оглавление темы «Легкие при системных заболеваниях»: |
Источник
Вопрос о собственно ревматоидной патологии органов дыхания в течение многих лет был дискуссионным; определенные противоречия в этом отношении сохраняются и до настоящего времени.
РА могут быть присущи четыре основных типа патологических изменений легких — плеврит, интерстициальный пневмонит, ревматоидные узелки и особый вариант пневмокониоза (синдром Каплана).
Плеврит — самое частое ревматоидное поражение легких. Он может встретиться на разных этапах заболеваний (включая самые ранние). Наблюдается чаще у мужчин и обычно не имеет клинических симптомов, обнаруживают его при плановом рентгенологическом исследовании в виде характерного накопления жидкости в плевральных полостях или остаточных явлений — плевральных сращений. Боль при дыхании, укорочение перкуторного звука, ослабление дыхания, шум трения плевры, одновременное повышение температуры отмечаются сравнительно редко и ввиду малой выраженности часто остаются вне поля зрения.
Выпот может накапливаться очень быстро и обычно бывает небольшим и двусторонним, редко наблюдается значительный односторонний экссудат. Экссудат имеет кислую реакцию (рН менее 7,0), содержание белка от 30 до 70 г/л (чаще 30—35 г/л), лейкоцитов менее 5·109/л с преобладанием лимфоцитов и иногда небольшой эозинофилией, содержание сахара менее 1,6—2,2 ммоль/л (30—40 мг%), активность ЛДГ выше, чем в сыворотке крови, при длительно существующем выпоте обнаруживают кристаллы холестерина.
По иммунологической характеристике ревматоидный плевральный экссудат во многом напоминает синовиальную жидкость из воспаленного сустава. В нем закономерно обнаруживают аналогичные иммунные комплексы; РФ в титре, равном титру в сыворотке или превосходящем его; снижение содержания компонентов комплемента, особенно С4; нейтрофилы, фагоцитировавшие иммунные комплексы, т. е. аналоги рагоцитов синовиальной жидкости.
Обращает внимание часто обнаруживаемый низкий уровень сахара (иногда ниже 1,5 ммоль/л!) как в синовиальном, так и в серозном (плевральном и перикардиальном) экссудатах при РА. Эта важная в дифференциально-диагностическом отношении особенность может отражать повышенное потребление глюкозы при ревматоидном воспалении либо нарушение ее активного транспорта через биологические барьеры, свойственные именно этому заболеванию.
Выраженность воспалительной реакции в плевральной полости по сравнению с полостью сустава гораздо ниже как по клеточной характеристике плеврального выпота (меньшее количество лейкоцитов и нейтрофилов), так и по клиническому течению, которое обычно оказывается латентным. Течение ревматоидных плевритов обычно благоприятное.
Как правило, они в течение нескольких месяцев подвергаются обратному развитию даже без специального лечения, хотя некоторые авторы считают целесообразным назначать кортикостероиды внутрь или внутриплеврально. Выраженный фиброз плевры с нарушением экскурсии легких, требующий хирургической декортикации, описан как очень редкое осложнение.
Плевральный выпот у больных РА может быть связан не только с ревматоидным плевритом. Нередко речь идет о транссудате у больных с недостаточностью кровообращения вследствие различных причин, в том числе и недиагностированного ревматоидного слипчивого перикардита. Следует помнить и о других типах плеврита — туберкулезном, метапневмоническом и т. д.
Бурный односторонний экссудативный плеврит у больного РА (особенно ослабленного, длительно получающего кортикостероиды) на фоне высокой температуры и ознобов очень подозрителен в плане эмпиемы, которая может развиться на фоне истинного ревматоидного плеврита. В подобных случаях весьма информативно исследование плеврального выпота — при транссудате низкий уровень белка и лейкоцитов, нормальное содержание сахара, ЛДГ и холестерина; при эмпиеме — лейкоцитоз выше 50—60·109/л, положительные бактериологические данные и т. д.
Интерстициальный пневмонит (диффузный легочный фиброз, фиброзирующий альвеолит) относительно чаще встречается у больных РА с прогрессирующим суставным процессом и высоким титром РФ и другими признаками иммунологической активности (противоядерные антитела, криоглобулины, нарастание иммунных комплексов [CervantesPerez P. et al., 1980].
Общая частота данного синдрома при РА невелика—около 1,5%, что не раз вызывало сомнения в патогенетической основе такого сочетания. Однако результаты биопсии легочной ткани и анализа альвеолярного экссудата (инфильтрация нейтрофилами и эозинофилами, нарастание IgG), положительная динамика этих результатов после лечения преднизолоном и отмеченный выше параллелизм с уровнем РФ и другими иммунологическими показателями позволяют полагать, что связь данной патологии с ревматоидным процессом не случайна. Это мнение подкрепляется также нередким сочетанием интерстициального пневмонита с другими системными проявлениями РА и наибольшей частотой при синдроме Фелти.
Основные клинические признаки рассматриваемого синдрома — сухой кашель и медленно прогрессирующая одышка, влажные хрипы в нижних отделах легких без значительного изменения характера дыхания и притупления перкуторного звука; на поздних стадиях — цианоз и другие симптомы легочно-сердечной недостаточности. Сравнительно часто обнаруживают утолщения концевых фаланг пальцев в виде «барабанных палочек» и изменения ногтей типа «часовых стекол». Показатели функции легких (жизненная емкость, интенсивность газообмена и др.) снижаются, иногда очень значительно.
Рентгенологически на первых этапах отмечается усиление интерстициальной структуры легких, затем появление на этом фоне «пушистого» рисунка, характерного для экссудативного альвеолита. Все изменения наиболее выражены в нижних долях, верхушки почти никогда серьезно не поражаются. По мере прогрессирования патологического процесса формируется типичная клиника диффузного легочного фиброза с рентгенологической картиной «пчелиных сотов» (сочетание выраженного фиброза с мелкими участками повышенной воздушности в базальных отделах).
В литературе имеется тенденция связать отдельные случаи интерстициального пневмонита с некоторыми антиревматическими средствами — препаратами золота, D-пеницилламином, метотрексатом, циклофосфамидом и даже бутадионом. Трактовка подобных наблюдений весьма сложна. Следует исходить из того, что интерстициальный пневмонит при РА заведомо чаще развивается вне связи с какой-либо терапией. Случаи, где такая связь предполагается, являются редким исключением.
Мы считаем, что у соответствующих больных речь идет об индивидуальной (по-видимому, иммунной) реакции на лекарственный препарат. Это мнение косвенно подтверждается тем, что все перечисленные лекарства способны вызывать спектр иммунных реакций, а также принципиальной обратимостью легочной патологии после отмены соответствующего препарата (в отличие от интерстициального пневмонита, развившегося при РА вне явной связи с экзогенным агентом).
Таким образом, рассматриваемый синдром имеет, по-видимому, различную патогенетическую основу: у одних больных он в большей степени отражает основной патологический процесс, у других — иммунную реакцию на лекарственные средства.
Ревматоидные узелки, которые могут иметь различную висцеральную локализацию, довольно редко обнаруживают в легких. Как правило, речь идет о случайной рентгенологической находке у мужчин, больных классическим РА с высоким содержанием в сыворотке крови РФ. Количество ревматоидных узелков в легких варьирует от одного до десятков, а размеры — от нескольких миллиметров до нескольких сантиметров. Их расположение чаще субплевральное, нередко в верхних отделах.
Как правило, они не сочетаются с такими свойственными РА легочными проявлениями, как диффузный фиброз легких и экссудативный плеврит. В редких случаях возможно разрушение узелка с кровохарканьем и образованием небольших каверн, а при плевральной локализации — возникновение пневмоторакса. У большинства больных ревматоидные узелки в легких подвергаются обратному развитию независимо от лечения.
В диагностически трудных ситуациях (появление узелков до симптомов артрита) показана биопсия, с помощью которой обнаруживают в подобных случаях гистологическую картину, типичную для ревматоидного узелка любой локализации, — центральный некроз, палисадоподобное расположение эпителиоидных клеток, инфильтрацию лимфоцитами и моноцитами и облитерирующий васкулит.
Синдром Каплана, впервые описанный в 1953 г. у шахтеров, по существу представляет собой разновидность описанного выше узловатого поражения легких. К особенностям его относят сочетание множественных и обычно крупных (более 1 см в диаметре) ревматоидных узелков в легких с пневмокониозом. Эти узелки часто распадаются с образованием полостей или кальцифицируются. Полагают, что обильно поступающие в легкие частицы пыли (угольной, асбестовой, кремниевой и др.) могут повреждать легочную ткань, что у больных РА способствует образованию в этих очагах ревматоидных узелков.
Среди шахтеров с пневмокониозом, заболевших РА, синдром Каплана встречается, по данным некоторых авторов, в 25% случаев. Как правило, это больные с высоким уровнем РФ в сыворотке крови и частым развитием подкожных узелков.
Нередко синдром Каплана предшествует клиническим проявлениям РА, а у ряда больных легочная патология остается изолированной и суставные симптомы вообще не развиваются. Однако и в этих случаях у большинства больных в сыворотке крови обнаруживают РФ.
Функция легких при синдроме Каплана нарушается незначительно.
Факторы риска относительно развития при РА именно легочных изменений широко обсуждаются в литературе. Правомерность самой постановки этого вопроса очевидна на примере синдрома Каплана, для возникновения которого бесспорным фактором риска (как и фактором патогенеза) является контакт с минеральной пылью. К другим важным факторам риска можно уверенно отнести мужской пол, наличие синдромов Фелти или Шегрена.
Для развития интерстициального пневмонита, по мнению многих авторов, серьезное предрасполагающее значение имеют курение, высокая воспалительная и иммунологическая активность ревматоидного процесса [Hyland R. et al., 1983], пожилой возраст и сопутствующие неспецифические легочные инфекции. Высказываются предположения о предрасполагающей роли HLADR4 и HLADR3, а также гетерозиготного носительства генов, ответственных за угнетение ингибиторов протеаз.
Мы уже отмечали, что в единичных случаях интерстициальный пневмонит может быть реакцией на длительно действующие антиревматоидные препараты — соли золота и D-пеницилламин, причем после отмены эгих лекарственных средств легочные изменения подвергаются обратному развитию. Аналогичные соображения высказывались также по поводу иммунодепрессантов — циклофосфамида, метотрексата и хлорбутина (но не азатиоприна), хотя в этих случаях нельзя полностью исключить активирование ими легочной инфекции.
При назначении D-пеницилламина описывались также острые облитерирующие бронхиолиты, в том числе с летальным исходом. Этот синдром, однако, очень редко наблюдается и у больных РА, не лечившихся данным препаратом; его действительная связь с заболеванием не вполне ясна (не исключается острая интеркуррентная вирусная инфекция). Облитерирующий бронхиолит характеризуется быстро прогрессирующей одышкой, сухим кашлем, диффузными влажными хрипами и свистящими хрипами на середине выдоха. Рентгенологическая картина может быть нормальной; функция легких резко ухудшается.
Следует также иметь в виду, что при назначении D-пеницилламина может развиться как синдром Гудпасчера с легочными инфильтратами, так и миастения, которая в случае поражения дыхательных мышц способна привести к дыхательной недостаточности и быстрому летальному исходу.
Однако, несмотря на все изложенное, истинное значение лекарственных препаратов как факторов риска легочных изменений при РА настолько невелико, что при выборе терапии эти соображения практически не учитываются.
Сигидин Я.А.
Опубликовал Константин Моканов
Источник