Фотодинамическая терапия ревматоидного артрита

Данный метод заключается в применении фото-активных препаратов (светочувствительных веществ), которые вводятся в организм пациента и активируются излучением. Эта щадящая для организма технология хорошо зарекомендовала себя в лечении патологически измененной ткани, злокачественных новообразований, очагов воспалений и т.д.
Большинству современных городских жителей присущ малоподвижный образ жизни. Офисный труд и передвижение за рулем автомобиля не требуют особой физической активности. Как следствие, повсеместное распространение на сегодняшний день имеют различные болезни позвоночника, проявляющиеся болями в спине и шее. Протрузии и грыжи позвоночника требуют длительного и сложного лечения. Ведущие центры неврологии, травматологии и ортопедии внедряют новые современные и прогрессивные методы лечения данной патологии.
Высокую оценку у специалистов получила методика фотодинамической лазеротерапии. Являясь отечественной разработкой, изначально фотодинамическая терапия нашла свое применение в борьбе с онкологическими заболеваниями в ведущих клиниках страны, в г. Москве и г. Санкт-Петербурге. На сегодняшний день данный метод также эффективен в комплексном лечении следующих заболеваний:
Болезнь Пертеса;
Болезнь Осгуд-Шлаттера;
Киста Беккера;
Остеохондроз, межпозвонковые грыжи;
Посттравматический асептический некроз головки бедренной кости;
Остеоартроз;
Ревматоидный артрит, в том числе ювенильный.
Принцип действия методики
 С точки зрения физиотерапии фотодинамическая лазеротерапия представляет собой двухкомпонентную терапевтическую методику, в которой особое вещество – фотодитазин – вводится внутрь, а затем производится воздействие на организм низкоэнергетического лазера.
С точки зрения физиотерапии фотодинамическая лазеротерапия представляет собой двухкомпонентную терапевтическую методику, в которой особое вещество – фотодитазин – вводится внутрь, а затем производится воздействие на организм низкоэнергетического лазера.
Немаловажное значение имеет способ введения фотодитазина: на 1-2 часа он наносится на тело в виде геля и накрывается темной пленкой, чтобы избежать разрушения под воздействием света. В течение этого времени вещество кумулируется в патологически измененных тканях. Далее под воздействием лазера клетки с патологическими изменениями разрушаются, при этом здоровые клетки остаются нетронутыми.
Переносимость процедуры пациентами
Физиотерапевты отмечают абсолютную безболезненность и даже комфортность процедуры (пациенты под воздействием лазера чувствуют приятное тепло). Также важным достоинством метода является отсутствие каких-либо ограничений – не исключается пребывание на солнце, так как фотодитазин не повышает фоточувствительность кожи.
Преимущества методики перед традиционными способами лечения
Высокую оценку у специалистов заслужила характерная для данного метода избирательность терапевтического воздействия, обусловленная селективным накапливанием действующего вещества в тканях с патологическими изменениями. Такие ткани подвержены воспалительным процессам, а фотодитазин накапливается именно в очагах воспаления, не затрагивая здоровые участки. Препарат не вызывает фотохимических осложнений, быстро выводится из организма, его можно использовать детям и подросткам.
Еще одной важной особенностью фотодинамической терапии является существенное сокращение сроков реабилитации пациентов. Кроме того, в отличие от инвазивных методов лечения, после нее не остается каких-либо косметических дефектов (шрамов, рубцов и пр.). К примеру, хирургическое лечение кисты Беккера характеризуется послеоперационным рубцом подколенной области; учитывая, что болезнь наиболее часто встречается у детей, для растущего организма это существенное негативное последствие. Применение фотодинамической терапии при кисте Беккера позволяет значительно сократить показания к оперативному лечению. При воспалительных заболеваниях суставов ФДТ способствует купированию болевого синдрома, снижению размеров сустава, исчезновению синовита, уменьшению толщины синовиальной оболочки, нормализации показателей крови.
Противопоказания
На сегодняшний день физиотерапевты отмечают отсутствие каких-либо побочных действий при лечении методом фотодинамической терапии. Его не рекомендуют применять пациентам, имеющим высокую фоточувствительность, а также беременным.
Продолжительность применения метода и его результативность
С 2005 года метод фотодинамической терапии запатентован и успешно применяется в лечении ревматоидного артрита, в том числе и ювенильного, в восстановительном центре (г. Санкт-Петербург) врачом-физиотерапевтом Сергеем Николаевичем Курченко. Начиная с октября 2011 года, этот метод используется и в нашем медицинском центре.
Мы отмечаем высокую эффективность метода в лечении кисты Беккера, когда уже после двух процедур констатируют выраженное уменьшение размера кистозного образования.
При лечении с помощью фотодинамической терапии болезни Пертеса (разрушение головки бедренной кости в связи с нарушением кровоснабжения) необходимость в соблюдении постельного режима снижается более чем на год.
Особую ценность данный факт имеет в связи с особенностью заболевания: оно характерно в основном для детей 3-7 лет, длится годами и требует относительной неподвижности. Применение фотодинамической терапии позволяет ребенку с болезнью Пертеса максимально быстро встать на ноги. Также существенно сокращается число осложнений, так как формирование головки бедренной кости происходит максимально физиологично.
Невозможно переоценить роль методики в лечении больных с межпозвонковыми грыжами. Данное заболевание характеризуется интенсивными и подчас невыносимыми болями. Использование фотодинамической терапии позволяет таким больным раньше обычного срока вернуться к полноценной жизни.
Профессионалы акцентируют внимание на том, что ФДТ не является единственным методом лечения межпозвонковых грыж, а применяется в комплексе с другими методами лечения болезни.
Распространение методики для лечения ортопедических патологий в России
Фотодинамическая терапия на сегодняшний день представляет собой новаторскую прогрессивную методику, которой владеет пока ограниченный круг специалистов в Москве, Санкт-Петербурге, Новосибирске и Краснодаре. В перечисленных крупных городах метод чрезвычайно популярен среди пациентов и врачей, отмечается также интерес к нему с точки зрения профессионального развития специалистов.
Беседу вела Пулакис О.Н., 21.11.13 г.
Источник
«Радиация и риск». 2014. Том 23. № 1, с.66-77
Сведения об авторах
Романко Ю.С. – зав. НОО, д.м.н.,ФГБУ МРНЦ Минздрава России.
Каплан М.А. – зав. отд., д.м.н., профессор,ФГБУ МРНЦ Минздрава России.
Попучиев В.В.– вед. научн. сотр., д.м.н., ФГБУ МРНЦ Минздрава России. Контакты: 249036, Калужская обл., Обнинск, ул. Королева, 4,
Тел.: (48439) 9-12-32; e-mail:
Этот адрес электронной почты защищен от спам-ботов. У вас должен быть включен JavaScript для просмотра.
.
Сурова Л.В. – мл. научн. сотр., ФГБУ МРНЦ Минздрава России.
Эпатова Т.В. – ст. научн. сотр., ФГБУ МРНЦ Минздрава России.
Аннотация
В обзоре представлены данные о возможностях применения фотодинамической терапии и диагностики в качестве малоинвазивной синовэктомии, местной противовоспалительной терапии и экстракорпоральной фотохимиотерапии (фотофереза) в лечении ревматоидного артрита. Анализ литературы свидетельствует о перспективах разработки новых эффективных схем лечения ревматоидного артрита с использованием фотодинамической терапии.
Ключевые слова
Фотодинамическая терапия, ревматоидный артрит, противовоспалительная терапия, синовэктомия, фотоферез.
Список цитируемой литературы
1. Балабанова Р.М., Амирджанова В.Н., Насонов Е.Л. Применение генно–биологических препаратов при ревматоидном артрите в Российской Федерации //Научно–практическая ревматология. 2012. Т. 50, № 6. С. 10–14.
2. Волгин В.Н., Странадко Е.Ф. Изучение фармакокинетики фотодитазина при базально-клеточном раке кожи //Лазерная медицина. 2011. Т. 15. Вып. 1. С. 33–35.
3. Кавалерский Г.М., Гаркави А.В., Меньшикова И.В., Сергиенко С.А. Артроскопическая синовэктомия при ревматоидном синовите коленного сустава //Научно-практическая ревматология. 2009. № 4. С. 84–89.
4. Каплан М.А., Капинус В.Н., Попучиев В.В. и др. Фотодинамическая терапия: результаты и перспективы //Радиация и риск. 2013. Т. 22, № 3. С. 115–123.
5. Каплан М.А., Никитина Р.Г., Романко Ю.С. и др. Фотодинамическая терапия саркомы М–1 у экспериментальных животных //Лазерная медицина. 1998. Т. 2, № 2–3. С. 38–42.
6. Каплан М.А., Пономарев Г.В., Баум Р.Ф. и др. Изучение специфической фотодинамической активности фотодитазина при фотодинамической терапии саркомы М–1 у крыс //Российский биотерапевтический журнал. 2003. Т. 2, № 4, С. 23–30.
7. Каплан М.А., Романко Ю.С. Фотодинамическая терапия //Физиотерапия, бальнеология и реабилитация. 2004. № 1. С. 43–48.
8. Каратеев Д.Е., Лучихина Е.Л., Муравьёв Ю.В. и др. Первое российское стратегическое исследование фармакотерапии ревматоидного артрита //Научно-практическая ревматология. 2013. Т. 51, № 2. С. 117–125.
9. Кильдюшевский А.В., Карзанов О.В., Ермилова А.И. и др. Экстракорпоральная фотохимиотерапия в лечении аутоиммунных и пролиферативных заболеваний кожи //Альманах клинической медицины. 2007. № 15. С. 168–172.
10. Кричевская О.А., Вакуленко О.Ю., Горячев Д.В., Эрдес Ш.Ф. О некоторых подходах к количественной оценке снижения производительности труда при ревматических заболеваниях //Научно-практическая ревматология. 2012. Т. 50, № 6. С. 90–97.
11. Курченко С.Н., Дудин М.Г., Мазуркевич Е.А., Шашко А.А. Применение фотодинамической терапии с препаратом «фотодитазин» для лечения дегенеративно-дистрофических и воспалительных заболеваний опорно-двигательного аппарата у детей и подростков //Альманах клинической медицины. 2008. Т. 17, № 2. С. 215–216.
12. Липина М.М., Макаров М.А., Амирджанова В.Н. и др. Роль артроскопической синовэктомии коленного сустава при лечении больных ревматоидным артритом //Доктор.Ру. 2012. № 6 (74). С. 38–44.
13. Маслянский А.Л., Иливанов Е.П., Рокоманюк В.И. и др. Сочетанная пульстерапия метотрексатом и дексаметазоном у больных ранним ревматоидным артритом с неблагоприятными прогностическими факторами: открытое рандомизированное исследование //Научно-практическая ревматология. 2013. Т. 51, № 2. С. 125–131.
14. Молочков В.А., Снарская Е.С., Поляков П.Ю. и др. К проблеме лечения базалиом кожи //Российский журнал кожных и венерических болезней. 2005. № 6. С. 4–9.
15. Муравьёв Ю.В. Проблема неблагоприятных реакций на лекарственные препараты //Научно–практическая ревматология. 2010. № 3. С. 13–14.
16. Мухин Н.А., Новиков П.И., Моисеев С.В. и др. Оценка краткосрочной эффективности и безопасности биологических препаратов при различных ревматических заболеваниях – опыт многопрофильного терапевтического стационара //Научно-практическая ревматология. 2013. Т. 51, № 2. С. 138–144.
17. Насонов Е.Л., Каратеев Д.Е. Применение генно-инженерных биологических препаратов для лечения ревматоидного артрита: общая характеристика //Научно-практическая ревматология. 2013. Т. 51, № 2. С. 163–169.
18. Олюнин Ю.А. Целенаправленное лечение ревматоидного артрита: рекомендации международной комиссии. Treatment to targent expert committee – экспертная комиссия по целенаправленному лечению //Современная ревматология. 2010. № 3. С. 7–9.
19. Павлов В.П., Макаров С.А., Макаров М.А. и др. Высокотехнологичные хирургические методы в комплексном восстановительном лечении суставной патологии верхних и нижних конечностей у больных с ревматическими заболеваниями //Современная ревматология. 2012. № 2. С. 103–108.
20. Панасюк Е.Ю., Амирджанова В.Н., Авдеева А.С. и др. Опыт применения тоцилизумаба у больных ревматоидным артритом (по данным многоцентрового исследования ЛОРНЕТ) //Научно–практическая ревматология. 2013. Т. 51, № 2. С. 104–110.
21. Романко Ю.С. Фотодинамическая терапия базально–клеточного рака кожи (экспериментально–клиническое исследование): дис. … д-ра мед. наук. Обнинск: ГУ «Медицинский радиологический научный центр РАМН», 2005. 204 с.
22. Романко Ю.С., Коренев С.В., Попучиев В.В. и др. Основы фотодинамической терапии. Калининград, 2010. 136 с.
23. Романко Ю.С., Цыб А.Ф., Каплан М.А., Попучиев В.В. Влияние фотодинамической терапии с Фотодитазином на морфофункциональные характеристики саркомы М–1 //Бюллетень экспериментальной биологии и медицины. 2004. № 12. С. 658–664.
24. Романко Ю.С., Цыб А.Ф., Каплан М.А., Попучиев В.В. Зависимость противоопухолевой эффективности фотодинамической терапии от плотности световой энергии //Бюллетень экспериментальной биологии и медицины. 2005. Т. 139, № 4. С. 456–461.
25. Салихов И.Г., Лапшина С.А., Кириллова Э.Р. Лечение ревматоидного артрита //Практическая медицина. 2008. № 32. С. 3–7.
26. Скугарева О.А., Попучиев В.В., Сухова Т.Е. и др. Фотодинамическая терапия с интерстициальным облучением опухоли //Российский журнал кожных и венерических болезней. 2012. № 2. С. 4–6.
27. Способ фотодинамической терапии последствий и осложнений поражений опорно-двигательной системы: патент 2233678 Российская Федерация: МПК7 А61N5/067 /Мазуркевич Е.А., Корнилов Н.В., Гельфонд М.Л., Рассадин А.Ю., Мазуркевич Т.Э.; патентообладатель Российский научно-исследовательский институт травматологии и ортопедии им. Р.Р. Вредена. Опубл. 10.08.2004. Бюл. 22.
28. Странадко Е.Ф. Основные этапы развития и современное состояние фотодинамической терапии в России //Лазерная медицина. 2011. Т. 16, Вып. 2. С. 4–8.
29. Трошкова Г.П., Фатюхина О.Е., Радаева И.Ф., Колокольцова Т.Д. Оценка безопасности и эффективности применения метода лазерно-индуцированной флуоресценции в медицине на модельной системе культивируемых клеток //Успехи современного естествознания. 2007. № 12. С. 385–386.
30. Филоненко Е.В. Флюоресцентная диагностика и фотодинамическая терапия в онкологии: дис. … д-ра мед. наук. М., 2006. 195 с.
31. Цыб А.Ф., Каплан М.А., Романко Ю.С., Попучиев В.В. Клинические аспекты фотодинамической терапии. Калуга: Издательство научной литературы Н.Ф. Бочкаревой, 2009. 204 с.
32. Шостак Н.А. Ревматоидный артрит – современный взгляд на проблему //Медицинский совет. № 4. 2012. С. 89–91.
33. Andreu G., Leon A., Heshmati F. et al. Extracorporeal photochemotherapy: evaluation of two techniques and use in connective tissue disorders //Transfus Sci. 1994. V. 15, N 4. Р. 443–454.
34. Bagdonas S., Kirdaite G., Streckyte G. et al. Spectroscopic study of ALA-induced endogenous porphyrins in arthritic knee tissues: targeting rheumatoid arthritis PDT //Photochem. Photobiol. Sci. 2005. V. 4, N 7. Р. 497–502.
35. Beischer A.D., Bhathal P., de Steiger R. et al. Synovial ablation in a rabbit rheumatoid arthritis model using photodynamic therapy //ANZ J. Surg. 2002. V. 72, N 7. Р. 517–522.
36. Chowdhary R.K., Ratkay L.G., Canaan A.J. et al. Uptake of verteporfin by articular tissues following systemic and intra-articular administration //Biopharm. Drug Dispos. 1998. V. 19, N 6. Р. 395–400.
37. Dall’Amico R., Zulian F., Montini G. et al. Applications of extracorporeal photochemotherapy in «non-oncological» diseases //Int. J. Artif. Organs. 1993. V. 16, Suppl. 5. Р. 168–172..
38. Dasgupta B., Fernandes L., Darley C. Photochemotherapy for rheumatoid arthritis //Br. J. Rheumatol. 1990. V. 29, N 5. Р. 396–397.
39. Edelson R., Berger C., Gasparro F. et al. Treatment of cutaneous T-cell lymphoma by extracorporeal photochemotherapy. Preliminary results //N. Engl. J. Med. 1987. V. 316, N 6. Р. 297–303.
40. Funke B. Jungel A., Schastak S. et al. Transdermal photodynamic therapy—a treatment option for rheumatic destruction of small joints? //Lasers Surg. Med. 2006. V. 38, N 9. Р. 866–874.
41. Gabriel D., Busso N., So A. et al. Thrombin-sensitive photodynamic agents: a novel strategy for selective synovectomy in rheumatoid arthritis //J. Control Release. 2009. V. 138, N 3. Р. 225–234.
42. Ghosh P., Smith M. Synovial ablation in a rabbit rheumatoid arthritis model using photodynamic therapy //ANZ J. Surg. 2002. V. 72, N 7. Р. 461.
43. Hansch A., Frey O., Gajda M. et al. Photodynamic treatment as a novel approach in the therapy of arthritic joints //Lasers Surg. Med. 2008. V. 40, N 4. Р. 265.
44. Hendrich C., Huttmann G., Lehnert C., Diddens H., Siebert W.E. Photodynamic laser therapy for rheumatoid arthritis. Cell culture studies and animal experiments //Knee. Surg. Sports Traumatol. Arthrosc. 1997. V. 5, N 1. Р. 58–63.
45. Hendrich C., Huttmann G., Vispo-Seara J.L. et al. Experimental photodynamic laser therapy for rheumatoid arthritis with a second generation photosensitizer //Arthrosc. 2000. V. 8, N 3. Р. 190–194.
46. Hendrich C., Siebert W.E. Photodynamic therapy for rheumatoid arthritis? //Lasers Surg. Med. 1997. V. 21, N 4. Р. 359–364.
47. Hilliquin P., Andreu G., Heshmati F., Menkes C.J. Treatment of refractory rheumatoid polyarthritis by extracorporeal photochemotherapy //Rev. Rhum. Ed. Fr. 1993. V. 60, N 2. Р. 125–130.
48. Van Iperen H.P., Beijersbergen van Henegouwen G.M. Clinical and mechanistic aspects of photopheresis //J. Photochem. Photobiol. B. 1997. V. 39, N 2. Р. 99–109.
49. Kirdaite G., Lange N., Busso N. et al. Protoporphyrin IX photodynamic therapy for synovitis //Arthritis Rheum. 2002. V. 46, N 5. Р. 1371–1378.
50. Malawista S.E., Trock D.H., Edelson R.L. Treatment of rheumatoid arthritis by extracorporeal photochemotherapy. A pilot study //Arthritis Rheum. 1991. V. 34, N 6. Р. 646–654.
51. Neupane J., Ghimire S., Shakya S. et al. Effect of light emitting diodes in the photodynamic therapy of rheumatoid arthritis //Photodiagnosis Photodyn. Ther. 2010. V. 7, N 1. Р. 44–49.
52. Ratkay L.G., Chowdhary R.K., Neyndorff H.C. et al. Photodynamic therapy; a comparison with other immunomodulatory treatments of adjuvant-enhanced arthritis in MRL-lpr mice //Clin. Exp. Immunol. 1994. V. 95, N 3. Р. 373–377.
53. Ratkay L.G., Waterfield J.D., Hunt D.W. Photodynamic therapy in immune (non-oncological) disorders: focus on benzoporphyrin derivatives //BioDrugs. 2000. V. 14, N 2. Р. 127–135.
54. Romanko Yu.S., Tsyb A.F., Kaplan M.A., Popuchiev V.V. Effect of photodynamic therapy with photodithazine on morphofunctional parameters of M–1 sarcoma /Bulletin of Experimental Biology and Medicine. 2004. V. 138, N 6. С 584–589.
55. Romanko Yu.S., Tsyb A.F., Kaplan M.A., Popuchiev V.V. Relationship between antitumor efficiency of photodynamic therapy with photoditasine and photoenergy density //Bulletin of Experimental Biology and Medicine. 2005. V. 139, N 4, P. 460–464.
56. Schmitt F., Lagopoulos L., Kauper P. et al. Chitosan-based nanogels for selective delivery of photosensitizers to macrophages and improved retention in and therapy of articular joints //J. Control Release. 2010. V. 144, N 2. Р. 242–250.
57. Torikai E., Kageyama Y., Kohno E. et al. Photodynamic therapy using talaporfin sodium for synovial membrane from rheumatoid arthritis patients and collagen-induced arthritis rats //Clin. Rheumatol. 2008. V. 27, N 6. Р. 751–761.
58. Trauner K.B., Gandour-Edwards R., Bamberg M. et al. Photodynamic synovectomy using benzoporphyrin derivative in an antigen-induced arthritis model for rheumatoid arthritis //Photochem. Photobiol. 1998. V. 67, N 1. Р. 133–139.
59. Yu C.Q., Huang N.Y., Zhao H.Y. et al. The simultaneous measurements of time-dependent laser-induced fluorescence intensity of hematoporphyrin monomethyl ether in animal tissues with rheumatoid arthritis //Guang Pu Xue Yu Guang Pu Fen Xi. 2004. V. 24, N 2. Р. 138–141.
60. Zic J.A., Miller J.L., Stricklin G.P., King L.E. The North American experience with photopheresis //Jr. Ther. Apher. 1999. V. 3, N 1. Р. 50–62.
Полная версия статьи
Источник
Фотодинамическая терапия (ФДТ) — один из нехирургических способов лечения рака и предраковых состояний. Во всем мире ФДТ активно используется с конца 70-х годов прошлого века, в России — уже в течение 10 лет.
В основе фотодинамической терапии лежит использование специальных веществ-фотосенсибилизаторов, избирательно накапливающихся в патологических клетках и повышающих их чувствительность к свету. Под действием световых волн определенной длины эти вещества вызывают фотохимическую реакцию и в результате приводят к образованию активных форм кислорода, уничтожающих злокачественные клетки. Затем погибшие клетки поглощаются «санитарами» организма — фагоцитами.
Кроме того, в процессе фотодинамической терапии повреждаются кровеносные сосуды, идущие к опухоли, что нарушает доставку питательных веществ и кислорода, и также способствует ее гибели. Под действием ФДТ активируются иммунные механизмы, они тоже помогают бороться с патологическим образованием.
Когда используют фотодинамическую терапию?
Фотодинамическая терапия показана при разных формах рака и предраковых состояниях, а также при заболеваниях кожи, глаз, ревматоидном артрите. Она хорошо переносится пациентами в любом возрасте и может использоваться как самостоятельный способ лечения. ФДТ применяют при сопутствующих тяжелых заболеваниях, при неэффективности традиционных способов или необходимости паллиативного лечения.
Основные показания к применению данного вида терапии:
- Актинический кератоз — предраковое состояние, которое развивается в результате длительного воздействия на кожу солнечного света.
- Базальноклеточный и плоскоклеточный рак кожи.
- Пищевод Барретта — состояние, при котором в слизистой оболочке пищевода появляются «неправильные» клетки. Плоский многослойный эпителий, который должен здесь быть в норме, замещается цилиндрическим. Впоследствии может произойти злокачественное перерождение. Как правило, пищевод Барретта является осложнением гастроэзофагеальной рефлюксной болезни (ГЭРБ).
- Злокачественные опухоли пищевода, ротовой полости, легких на ранней стадии.
- Болезнь Боуэна — редкая разновидность поражения кожи, относится к плоскоклеточным карциномам кожи 0 стадии.
- Дегенерация желтого пятна — участка сетчатки глаза, который обладает наибольшей остротой зрения. Это заболевание является наиболее распространенной причиной слепоты.
Применение фотодинамической терапии имеет существенное ограничение: её проводят только в тех местах, куда можно подвести свет. К доступным областям относятся: кожа, глаза, ротовая полость, пищевод и дыхательные пути.
Преимущества и недостатки фотодинамического метода лечения
К преимуществам фотодинамического лечения относится то, что после него не остается шрамов и рубцов. Кроме того, фотодинамическую терапию можно применять при труднодоступной локализации рака, когда операцию провести затруднительно — например, на губе, языке, ушной раковине и др.
Однако, как мы упомянули, с помощью ФДТ можно лечить патологии только в определенных органах. Лучи лазера могут проникать только на определенную глубину — до 1 см. Метод не подходит при крупных новообразованиях.
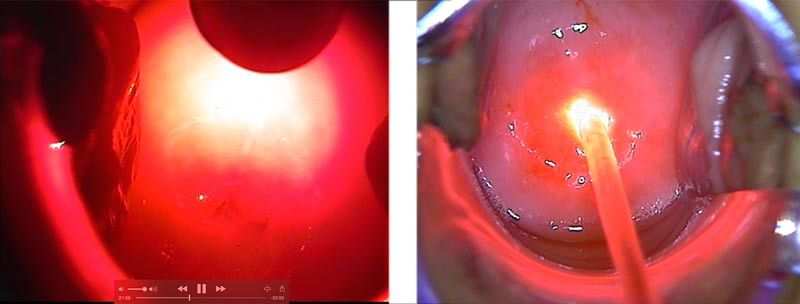
Фотодинамическая терапия при поражении шейки матки
Используемые препараты
В настоящее время существует довольно много фотосенсибилизаторов, одобренных для проведения ФДТ. В России доступны такие препараты для фотодинамической и радиационной терапии, как Радахлорин, Фотодитазин, Фотолон, Фоторан Е6, Фотосенс.
Рекомендации перед проведением ФДТ
Специальной подготовки перед процедурой не требуется. Врач осматривает пациента, назначает обследование, определяет, будет ли ФДТ оптимальным методом лечения в данном случае. Подбирают препарат, определяют интенсивность излучения и длительность воздействия.
Этапы терапии
ФОТ проводят в два этапа:
- Препараты-фотосенсибилизаторы вводят в вену или местно в области опухоли (способом аппликации). В течение 1–2 суток они накапливаются в раковых клетках, повышая их чувствительность к свету.
- Затем целевую область в течение нескольких минут облучают лазером. В пищевод и легкие свет подводят с помощью оптоволоконного кабеля.
Гибель опухоли продолжается 2–3 месяца, здоровые окружающие ткани при этом не повреждаются. Как правило, одной такой процедуры бывает достаточно, но при необходимости можно проводить и повторные сеансы.
Чаще всего ФДТ проводят амбулаторно, для этого не требуется госпитализация в стационар. При необходимости метод можно сочетать с хирургическим лечением, лучевой терапией, химиотерапией.
Восстановление организма после ФДТ
После процедуры на место воздействия накладывают повязку, обычно её снимают через сутки. В течение некоторого времени нужно избегать солнечных лучей, травм области, подвергнутой воздействию лазера. Мыться можно, но нужно насухо вытирать обработанную кожу. Обычно полное заживление происходит через 2–6 недель.
Противопоказания к ФДТ
Фотодинамическая терапия противопоказана при заболеваниях печени, почек и сердца в стадии декомпенсации, во время беременности и кормления грудью, а также людям с повышенной чувствительностью к фотосенсибилизаторам.
Источник
