Генная инженерия при псориатическом артрите

В статье представлен российский опыт использования и результаты лечения секукинумабом пациента с распространенным вульгарным псориазом и псориазом ногтей.

Псориаз является хроническим рецидивирующим воспалительным заболеванием, которым страдают около 125 млн человек по всему миру [1]. В Российской Федерации заболеваемость псориазом составляет 65,8 на 100 тыс. населения, причем отмечается большой удельный вес тяжелых и среднетяжелых форм в структуре заболеваемости [2]. В последние годы заболевание рассматривается как системный процесс, который поражает не только кожу, но и другие производные соединительной ткани (суставы, энтезисы).
Почему же при псориазе, особенно при его тяжелых формах, мы все чаще обращаем внимание именно на ногти? Ногти считаются эпидермальным придатком и действительно чаще всего поражаются у больных псориазом. Поражение опорно-двигательного аппарата при псориазе начинается в первую очередь с вовлечения в патологический процесс энтезисов, которыми изобилуют ногти. Часто этот процесс происходит незаметно. Сегодня ногти рассматриваются в качестве видимой части энтезисов (рис. 1, адаптировано из [3]). В итоге поражение ногтей при псориазе является четким предиктором дальнейшего развития псориатического артрита.
![Рис. 1. Анатомические связи ногтя и дистального межфалангового экстензорного тензора (адаптировано из [3]) Рис. 1. Анатомические связи ногтя и дистального межфалангового экстензорного тензора (адаптировано из [3])](https://www.rmj.ru/upload/medialibrary/a55/60-1.png)
Псориаз может поражать две структуры ногтей — матрикс и ногтевое ложе. Поражение матрикса ногтя может привести к таким изменениям, как лейконихия, симптом наперстка, разрушение ногтевой пластины. Вовлечение же ногтевого ложа в патологический процесс может привести к онихолизису, подногтевому гиперкератозу и кровоизлияниям. Поражения ногтей не только вызывают эстетические и функциональные нарушения, но и свидетельствуют о более тяжелых формах псориаза.
Считается, что поражение ногтей встречается у 80–90% пациентов с псориазом [3]. По другим источникам, распространенность псориаза ногтей составляет около 50% [4–6]. Исследования, проведенные в Германии в 2010 г. с участием 3531 больного псориазом, установили, что псориаз ногтей в большей степени распространен среди пациентов мужского пола (11,2%) [7]. Есть данные, что среди пациентов с псориатическим артритом распространенность поражения ногтей составляет 80,5% [7, 8]. При этом у 15% пациентов изменения ногтей могут наблюдаться при отсутствии кожных поражений [8–10].
Несмотря на свои эстетические и функциональные последствия, псориаз ногтей мало рассмотрен в литературе. Кроме того, по данной теме проведено лишь несколько эпидемиологических и клинических исследований.
Лечение псориаза
Терапия среднетяжелого и тяжелого псориаза с помощью метотрексата, циклоспорина, ароматических ретиноидов, фототерапии не всегда позволяет контролировать течение как самого дерматоза, так и поражения ногтей.
Системная терапия рекомендуется при сочетанном поражении кожи и ногтей. Несмотря на то что эффективность метотрексата в лечении кожного псориаза была описана в многочисленных исследованиях, а его применение у пациентов с псориазом ногтей малоизучено, Европейский консенсус по лечению псориаза ногтей при тяжелых формах болезни рекомендует комбинацию метотрексата с топической терапией [11, 12]. Активное изучение влияния генно-инженерной биологической терапии (ГИБТ) на течение псориаза и псориатического артрита началось после того, как было доказано, что псориаз и псориатический артрит являются Т-клеточно опосредованными заболеваниями, при которых происходит активация клеточного иммунитета в коже и синовии с гиперпродукцией и дисбалансом противо- и провоспалительных цитокинов. После получения вдохновляющих данных по эффективности ГИБТ стало понятно, что появился реальный шанс помочь пациентам с этим тяжелым недугом.
Инфликсимаб — первый хорошо изученный иммунобиологический агент. Исследования доказали его эффективность как при псориазе гладкой кожи, так и при псориазе ногтей [13, 14]. Адалимумаб, этанерцепт, устекинумаб также оказались эффективными средствами в лечении пациентов с псориазом кожи и ногтей [15–17]. Важно отметить что все исследования были проведены в когорте пациентов с комбинированным поражением ногтей и кожи.
В 2016 г. в России зарегистрирован препарат, относящийся к группе ингибиторов интерлейкина-17 А (IL-17 А) —
секукинумаб [18]. Секукинумаб (Козэнтикс, Новартис Фарма АГ, Швейцария) — препарат для лечения псориаза среднетяжелой и тяжелой степени у взрослых пациентов, которым показана системная терапия или фототерапия, представляет собой полностью человеческое моноклональное антитело к человеческому иммуноглобулину G1κ (IgG1κ) и обладает селективным действием в отношении IL-17А.
В результате исследований выявлено, что IL-17А является ключевым цитокином, определяющим патогенез псориаза, и действует непосредственно на кератиноциты, стимулируя секрецию провоспалительных медиаторов [19, 20].
В настоящее время относительно безопасности, эффективности и влияния терапии секукинумабом на качество жизни пациентов с псориазом различных локализаций (в т. ч. устойчивым к стандартным методам лечения и проблемной локализации — ладонно-подошвенным псориазом, псориазом волосистой части головы, псориатической ониходистрофией) и псориатическим артритом опубликованы результаты 11 масштабных прямых сравнительных клинических исследований (4 — II фазы, 7 — III фазы). Наиболее крупными из них были FIXTURE (n=1306), SCUPLTURE (n=965), ERASURE (n=738), CLEAR (n=669), TRANSFIGURE (n=198), SCALP (n=102), FEATURE (n=177), JUNCTURE (n=182), GESTURE (n=205) и др. [21–28].
Следует отметить, что результаты всех исследований показали очень высокую скорость регресса кожных проявлений, что является несомненным преимуществом препарата [29]. По результатам двойных слепых плацебо-контролируемых исследований, в которых проводилось сравнение секукинумаба с этанерцептом и устекинумабом, секукинумаб показал доказанно лучшие результаты по эффективности влияния на состояние кожи, улучшению качества жизни как в кратковременной, так и в длительной перспективе, а также благоприятный сопоставимый профиль безопасности [30, 31]. Согласно PASI 90 (Psoriasis Area and Severity Index — индекс распространенности и тяжести псориаза), уже на 16-й неделе наблюдения секукинумаб показал эффективность на 20% выше по сравнению с устекинумабом [21]. Кроме того, в клинических исследованиях получены неоспоримые доказательства эффективности секукинумаба при псориазе ногтей, волосистой части головы, а также ладонно-подошвенном и пустулезном псориазе. С точки зрения форм псориаза, плохо поддающихся лечению, таких как ладонно-подошвенный, псориаз ногтей и др., новые инновационные средства представляют особый интерес. Результаты исследования TRANSFIGURE [21], в котором изучалась эффективность секукинумаба при псориазе ногтей, ярко демонстрирует прекрасные результаты лечения. Пациенты, включенные в это исследование, более 10 лет страдали от псориаза ногтей. Фото пациента, представленные в статье, наглядно демонстрируют новые возможности терапии псориаза ногтей (рис. 2а, б, в). Особенно важно отметить, что результаты терапии появлялись в короткие сроки.
![Рис. 2. Результаты терапии псориаза ногтей секукинумабом (из [3]): а – до лечения (PASI: 15.00; NAPSI: 38; ppIGA: 0); б – 16-я неделя лечения (PASI: 15.60; NAPSI: 74; ppIGA: 4); в – 80-я неделя лечения (PASI: 0; NAPSI: 4; ppIGA: 0) Рис. 2. Результаты терапии псориаза ногтей секукинумабом (из [3]): а – до лечения (PASI: 15.00; NAPSI: 38; ppIGA: 0); б – 16-я неделя лечения (PASI: 15.60; NAPSI: 74; ppIGA: 4); в – 80-я неделя лечения (PASI: 0; NAPSI: 4; ppIGA: 0)](https://www.rmj.ru/upload/medialibrary/241/60-2.png)
Приводим пример клинической эффективности и переносимости терапии препаратом секукинумаб (Козэнтикс) в лечении пациента с вульгарным псориазом и псориазом ногтевых пластин.
Клиническое наблюдение
Пациент М., 38 лет, был направлен с диагнозом: вульгарный псориаз, распространенная форма, прогрессивная стадия. Псориаз ногтевых пластин.
Впервые обратился в 2014 г. с жалобами на высыпания на коже туловища (грудь, спина, живот), верхних и нижних конечностей, умеренный зуд в течение дня. Считает себя больным в течение 10 лет, когда впервые заметил бляшечные элементы в области разгибательных поверхностей верхних конечностей. Пациент неоднократно получал амбулаторное лечение наружными гклюкокортикостероидами совместно с физиотерапией с временным эффектом. С 2016 г. получал препарат метотрексат, начальная дозировка 25 мг/нед., совместно с фолиевой кислотой, при стабильном эффекте доза была снижена до 17,5 мг/нед.
На данной терапии был стабильный положительный эффект в течение года. С 2017 г. произошло ухудшение кожного процесса, возникла болезненность мелких суставов. В связи с резистентностью к данному виду терапии консилиум принял решение о применении ГИБП.
Хронические заболевания: хронический холецистит, ремиссия. Хронический тонзиллит, К-форма, стадия ремиссии, хронический ринофарингит, неполная ремиссия.
Заключение терапевта (от 02.11.2017): терапевтически здоров. На момент осмотра, лечение секукинумабом (Козэнтикс) не противопоказано.
С ноября 2017 г. начато этапное лечение секукинумабом. Перед началом терапии пациент прошел стандартные обследования для выявления возможных противопоказаний к применению ГИБП: обследования на ВИЧ, гепатиты В, С, туберкулез (рентгенография органов грудной клетки, консультация фтизиатра), исключение онкологического процесса, клинические анализы крови и мочи, биохимическое исследование крови (уровень глюкозы, аланинаминотрансферазы — АЛТ, аспартатаминотрансферазы — АСТ, гамма-глутамилтрансферазы, креатинина, С-реактивного белка, липидный профиль). При обследовании исключены туберкулез и другие инфекционные заболевания, данных за онкологические заболевания не выявлено. До начала лечения в клиническом анализе крови отклонений от нормы не выявлено, в биохимическом анализе крови: билирубин общий — 10,3 мкмоль/л; АЛТ — 22,1 Ед/л; АСТ — 19,5 Ед/л; щелочная фосфатаза — 125 Ед/л; холестерин — 4,16 ммоль/л; глюкоза — 7,75 ммоль/л; креатинин — 63,6 мкмоль/л; мочевина — 5,45 ммоль/л; общий белок — 72,5 г/л.
Препарат секукинумаб назначен в дозе 300 мг согласно инструкции по применению препарата в виде подкожных инъекций. Инициирующий курс составил 4 еженедельные инъекции. В дальнейшем терапия продолжена в виде ежемесячных инъекций.
Status localis на момент начала терапии: на коже волосистой части головы (височные, затылочная область), туловища (грудь, спина, живот), верхних конечностей (разгибательные поверхности предплечий, локтевых суставов), нижних конечностей (передние и задние поверхности бедер, голеней, разгибательные поверхности коленных суставов) — множественные, инфильтрированные по периферии бляшки розового цвета, покрытые частично прилегающими серебристыми чешуйками на поверхности. Триада Ауспитца положительная. Вокруг элементов венчик Пильнова. На ногтевых пластинах кистей определяются симптомы наперстка и масляного пятна (рис. 3а, 4а и 5а). Деформация суставов, отечность не определялись.
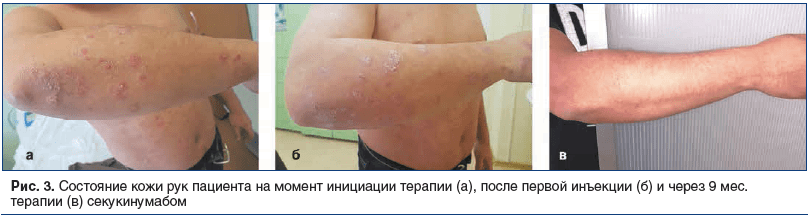

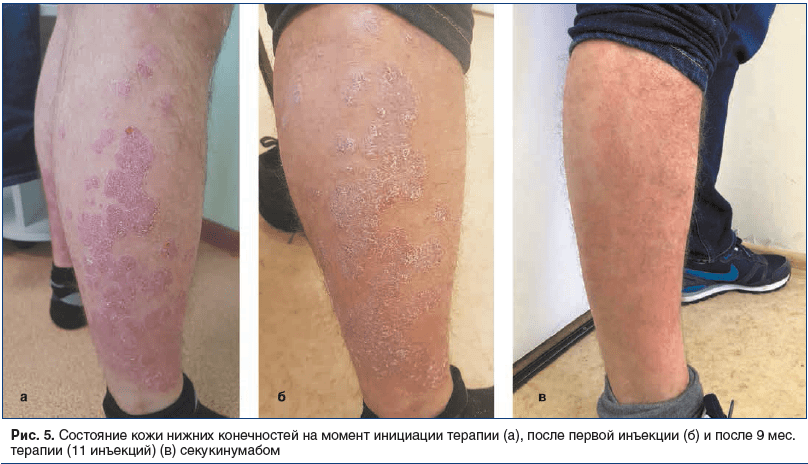
Результаты терапии. На фоне начала терапии уже в течение 7 дней после первой проведенной инъекции секукинумаба отмечена положительная динамика (рис. 3б, 5б). После проведения 4-недельного инициирующего курса отмечен практически полный регресс высыпаний. На коже туловища и конечностей не было появления новых элементов, зуд был полностью купирован, оставались множественные пятна поствоспалительной гиперпигментации в местах бывших высыпаний, незначительное шелушение на поверхности неплотно прилегающими чешуе-корками. Уже через 8 нед. от начала терапии секукинумабом отмечалась зона отрастания неизмененных ногтевых пластин примерно на 0,5 см.
После 6 инъекций на коже туловища (грудь, спина, живот), верхних конечностей (разгибательные поверхности предплечий, локтевых суставов), нижних конечностей (передние и задние поверхности бедер, голеней, разгибательные поверхности коленных суставов) оставались только пятна поствоспалительной пигментации, чешуе-корок нет.
После 9 инъекций наступил полный регресс клинической картины (кожа чистая, ногтевые пластины чистые; симптомы масляного пятна и наперстка отсутствуют).
В настоящее время (после 11 инъекций) сохраняется полная ремиссия. Ногтевые пластины без патологических изменений, кожные покровы без высыпаний и шелушений, пигментные пятна полностью разрешились (рис. 3в, 4б, 5в). Динамика всех показателей менялась в короткие сроки от начала терапии. Данные показателей представлены подробно в таблице 1.
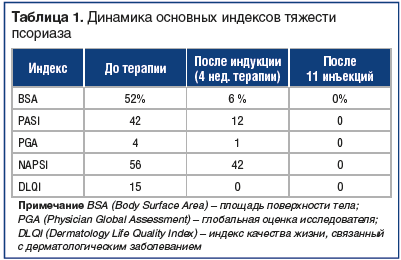
Влияние на качество жизни. Следует отметить, что до лечения индекс DLQI (Dermatology Life Quality Index) составлял 15 баллов, что отражает очень сильное влияние кожного заболевания на качество жизни пациента. После первой инъекции данный показатель составил 15 баллов, после второй — 11 баллов, после третьей — 10 баллов, после четвертой — 0 баллов. То есть заболевание перестало негативно воздействовать на повседневную жизнь пациента.
Курс лечения секукинумабом составил 9 мес. и будет продолжен.
Лабораторный контроль в течение первого месяца терапии проводился 1 раз в 7 дней, далее 1 р./мес. В клиническом анализе крови отклонений не выявлено. Результаты биохимического анализа крови и клинического анализа мочи — без отрицательной динамики, показатели стабильны.
Заключение
Представленное наблюдение демонстрирует высокую клиническую эффективность препарата Козэнтикс (секукинумаб) в терапии пациента с вульгарным псориазом и псориазом ногтей. Достигнута быстрая и сохраняется стабильная нормализация всех показателей: PASI, ВSA, PGA и DLQI.
Лечение переносится хорошо, нежелательных явлений в течение терапии не выявлено.
Можно сделать вывод, что препарат полностью контролирует заболевание и улучшает качество жизни пациентов с псориазом ногтей.
Таким образом, на сегодняшний день есть уверенность в том, что можно контролировать развитие таких тяжелокурабельных форм псориаза, как псориаз ногтей, прогрессирование которого является определенным предиктором развития псориатического артрита и инвалидизации. Раннее начало применения ГИБП позволит вовремя предупредить развитие псориатического артрита.
Источник
За последние десятилетия в ревматологии произошли существенные изменения, которые связанны с активным внедрением в клиническую практику генно–инженерных биологических препаратов (ГИБП). Их действие направлено на специфические компоненты механизма развития ревматических заболеваний. Ревматологи Юсуповской больницы применяют ГИБП препараты, зарегистрированные в РФ.
Лечение назначают после комплексного обследования пациентов с помощью новейшей аппаратуры ведущих мировых производителей и точных методов лабораторной диагностики. Тяжёлые случаи заболеваний обсуждают на заседании Экспертного Совета. Доктора и кандидаты медицинских наук, врачи высшей категории коллегиально вырабатывают тактику ведения каждого пациента.
Для лечения аутоиммунных заболеваний, особенно ревматоидного артрита ревматологи применяют генно-инженерные биологические препараты (ГИБП). Они представляют собой моноклональные антитела и рекомбинантные белковые молекулы, которые подавляют активность важнейших факторов, которые принимают участие в развитии аутоиммунного воспалительного процесса. В настоящее время список ГИБП пополнил новый точечный ингибитор киназы (ингибитор JAK-киназы). Врачи Юсуповской больницы применяют генно-инженерные биологические препараты в ревматологии. Цена препаратов высокая, но они обладают высокой эффективностью.

Классификация
Генно-инженерные биологические препараты представлены следующими лекарственными средствами:
- Ингибиторами фактора некроза опухоли-альфа (ФНО-альфа);
- Моноклональные антитела к рецепторам интерлейкин;
- Анти В-клеточные моноклональные антитела;
- Блокатор КО-стимуляции Т-лимфоцитов;
- Ингибитор протеинкиназы.
К ингибиторам ФНО-альфа относится инфликсимаб (ремикейд). Препарат оказывает селективное иммуномодулирующее действие. Лекарственное средство применяют при следующих ревматических заболеваниях:
- Ревматоидном артрите;
- Анкилозирующем спондилоартрите;
- Ювенильном ревматоидном артрите.
- Псориатическом артрите.
Адалимумаб (хумира) – селективный иммунодепрессант, рекомбинантное человеческое моноклональное антитело. По пептидной последовательности идентичен иммуноглобулинам Ig. Лекарственное средство применяют при среднетяжёлом и тяжёлом ревматоидном артрите в виде монотерапии или в сочетании с метотрексатом, ГИБП. Хумира применяется для лечения псориатического артрита, активного анкилозирующего спондилита.
Этанерцепт (Энбрел) тормозит биологические эффекты ФНО-α. Препарат представляет собой гибридную молекулу, которая состоит из ФНО-рецептора, соединённую с Fс-фрагментом IgG человека. Состоит из 934 аминокислот. Димерная структура ФНОР в молекуле этанерцепта обеспечивает более высокое взаимодействие препарата к ФНО-α, чем с мономерный рФНОР.
Препарат эффективен в лечении ревматоидного артрита, хорошо переносится пациентами даже при длительном применении. Комбинированная терапия этанерцептом и метотрексатом значительно превосходит монотерапию энбрелом у пациентов как с ранним, так и развёрнутым ревматоидным артритом. Потенциальными преимуществами этанерцепта перед другими ингибиторами ФНО-α является сохранение эффекта терапии в процессе длительного лечения и меньший риск активации туберкулёза.
Цертолизумаб пэгол – моноклональное антитело, ингибитор ФНО-α. Препарат нейтрализует мембранные и растворимые рецепторы фактора некроза опухоли альфа. Ревматологи назначают цертолизумаб пациентам, страдающим ревматоидным артритом средней и высокой активности у взрослых. Препарат применяют для монотерапии или в комбинации с другими базисными средствами.
Голимумаб (симпони) – это человеческие моноклональные антитела класса IgG1k. Они образуют стабильные комплексы «антиген-антитело» с растворимыми и с трансмембранными биоактивными формами фактора некроза опухоли альфа, предотвращая связывание ФНОα с его рецепторами. У больных с аутоиммунными ревматическими заболеваниями голимумаб оказывает эффективное модулирующее действие.
Препарат назначают для лечения ревматоидного артрита в комбинации с метотрексатом при неэффективности других базисных средств, а также для терапии пациентов с тяжёлым прогрессирующим течением ревматоидного артрита, которые ранее не получали метотрексат. Показанием к применению препарата является псориатический артрит, тяжелый, прогрессирующий анкилозирующий спондилит без ответа на стандартную терапию.
Моноклональное антитело к рецепторам интерлейкин – устекинумаб (стелара). Это человеческие моноклональные антитела (класса Ig-G/к). Применяется для лечения псориаза, псориатического артрита. Ревматологи назначают устекинумаб в виде монотерапии и в сочетании с метотрексатом.
Анакинра (Кинерет) – рекомбинантный антагонист рецептора ИЛ-1, медиатора воспаления, который присутствует в синовиальной жидкости и плазме пациентов, страдающих ревматоидным артритом. Применяют для терапии пациентов, страдающих среднетяжелыми и тяжёлыми формами ревматоидного артрита, резистентных к метотрексату и действию других базисных средств. Препарат эффективен при острой и подострой формах подагры. Значительно облегчает боль, особенно у тех пациентов, кто не переносит стандартные противовоспалительные средства.
Тоцилизумаб – рекомбинантное гуманизированное моноклональное антитело к человеческому рецептору интерлейкина-6 из подкласса иммуноглобулина Ig-G. Избирательно связывается и подавляет растворимые и мембранные рецепторы интерлейкина 6. Применяется для лечения ревматоидного артрита со средней или высокой степенью активности в виде монотерапии и в комбинации с другими базисными средствами. Особенно эффективно тормозит рентгенологически доказанную деструкцию суставов. Препарат используют в терапии активного полиартикулярного ювенильного идиопатического артрита и активного системного ювенильного идиопатического артрита.
Анти В-клеточные моноклональные антитела представлены препаратом ритуксимаб-РТМ (мабтера). Это синтетическое (генно-инженерное) химерное моноклональное антитело мыши или человека. Оно по структуре относится к иммуноглобулинам класса G1 (IgG1 каппа).
Ритуксимаб обладает высокой эффективностью при лечении пациентов, страдающих системной красной волчанкой с активными внепочечными проявлениями (серозитом, полиартритом, поражением кожи, стоматитом, лихорадкой, анемией), прогрессирующим волчаночным нефритом. Он является быть препаратом выбора для терапии системной красной волчанки, протекающей критически.
Ритуксимаб ревматологи применяют при мультиорганном тромбозе, связанном с катастрофическим антифосфолипидным синдромом. Препарат успешно применяют для лечения следующих заболеваний:
- Синдрома Шегрена;
- Полимиозита;
- Дерматомиозита;
- Гранулематоза Вегенера.
Ритуксимаб успешно применяют при пузырчатке – потенциально смертельном аутоиммунном заболевании, в основе которого лежит выработка аутоантител, реагирующих с десмоглеином 1 и 3 и молекулами адгезии эпидермиса. Ритуксимаб является родоначальником нового направления в лечении аутоиммунных заболеваний человека. Он модулирует В-клеточное звено иммунитета.
Блокатор КО-стимуляции Т-лимфоцитов абатацепт (оренсия) продуцируется путём технологии рекомбинантной ДНК на клетках яичников китайского хомячка. Препарат назначают пациентам с ревматоидным артритом при непереносимости и неэффективности других средств базисной терапии совместно с метотрексатом. Не сочетают с другими базисными препаратами, в том числе ингибиторами ФНО-α, анакинрой, ритуксимабом.
Тофацитиниб (Яквинус) – мощный избирательный ингибитор янус-киназы. Обладает высокой избирательностью в отношении янус-киназы 1, 2, 3. Препарат применяют при умеренном или тяжёлом активном ревматоидном артрите у взрослых с неадекватным ответом на один или несколько базисных средств.
Осложнения
Невзирая на высокую эффективность, ГИБП оказывают побочные действия. Тяжёлым осложнением терапии генно-инженерными биологическими препаратами ревматологи считают инфекции, ассоциированные с ГИБП. Ситуация осложняется тем, что лечение ревматических заболеваний требует применения иных антиревматических препаратов, которые обладают иммуносупрессивным действием.
При лечении ГИБП могут развиться следующие инфекционные осложнения:
- Септический артрит;
- Остеомиелит;
- Инфекции;
- Кожи и мягких тканей;
- Пневмония.
Основными прогностическими критериями развития инфекций при ревматических заболеваниях являются лейкопения, хронические заболевания лёгких, внесуставные проявления болезни, увеличение СОЭ, наличие ревматоидного фактора, лечение глюкокортикоидами. Применение метотрексата у больных ревматоидным артритом приводит к достоверному повышению общего числа вторичных инфекций.
Чтобы свести к минимуму риск развития инфекционных осложнений, связанных с терапией генно-инженерными биологическими препаратами, ревматологи Юсуповской больницы проводят тщательный отбор больных в строгом соответствии с показаниями, не назначают ГИБП пациентам, страдающим клинически значимой инфекцией в активной форме. Врачи проводят тщательное обследование пациентов с целью выявления латентной инфекции, соответствующее лечение в случае её обнаружения, откладывают начало терапии ГИБП. Крайнюю осторожность проявляют при решении вопроса о лечении ГИБП у пациентов с повышенной восприимчивостью к инфекциям, с наличием в анамнезе рецидивирующих инфекций или страдающим хроническим инфекционным заболеванием.
Во время и после лечения информируют пациентов о том, что ГИБП могут повышать способность к развитию инфекций. Ревматологи проводят инструктаж больных о необходимости немедленного обращения к врачу при появлении во время или после лечения ГИБП симптомов инфекции (повышения tº тела, общей слабости, кашля или гриппоподобных симптомов) или признаков, которые позволяют заподозрить туберкулёз (субфебрилитета, длительно сохраняющегося кашля, снижения массы тела).
Врачи Юсуповской больницы проводят тщательное наблюдение как минимум в течение шести месяцев после окончания лечения ГИБП. При развитии тяжёлой инфекции терапию генно-инженерными биологическими препаратами прекращают, проводят в связи с этим соответствующее обследование и лечение

Терапия остеопороза при ревматоидном артрите
Ревматоидный артрит является центральной проблемой современной ревматологии. Это хроническое прогрессирующее заболевание с постепенно нарастающей деструкцией мягких тканей, хряща и костей. Наиболее часто встречающееся и тяжелое проявление ревматоидного артрита – остеопороз. Он может быть обусловлен активностью самого заболевания и побочным действием проводимой терапии.
Деструкцию костной ткани вызывают медиаторы воспалительного и иммунного процессов — провоспалительные цитокины, которые вырабатываются субпопуляцией Т-лимфоцитов. К ним относят:
- Фактор некроза опухоли а (ФНО-а);
- Интерлейкины 1, 2, 12, 17;
- Интерферон;
- Простагландины;
- Протеолитические ферменты.
Генно-инженерные биологические препараты (ГИБП), которые применяют для лечения ревматоидного артрита, уменьшают воспалительные изменения суставов, сдерживают развитие деструкции и развитие остеопороза. При применении ГИБП наблюдается стабилизация или повышение минеральной плоскости кости. У пациентов повышается образование костной ткани и снижается рассасывание кости. Препараты способствуют замедлению деструкции суставов при ревматоидном артрите. Для того чтобы пройти комбинированную терапию ревматических заболеваний, в том числе генно-инженерными биологическими препаратами, по доступной цене, звоните в контакт центр Юсуповской больницы.
Источник
