Хеликобактер и ревматоидный артрит

Представлены результаты исследования частоты инфицированности и оценки эффективности альтернативной схемы эрадикационной терапии Helicobacter pylori у больных ревматическими заболеваниями
Helicobacter pylori (H. pylori) – самая распространенная инфекция человека: не менее половины жителей Земли являются носителями этой бактерии. Взаимодействие H. pylori и иммунной системы формирует широкий спектр биологических реакций, от относительно спокойного сосуществования микро- и макроорганизма до выраженного воспалительного процесса и серьезных аутоиммунных нарушений. Эта бактерия известна как основной этиологический фактор хронического гастрита, язвы желудка и двенадцатиперстной кишки, а также аденокарциномы желудка [1, 2]. Кроме того, инфекция H. pylori ассоциируется с развитием ряда аутоиммунных заболеваний, таких как аутоиммунная гемолитическая анемия, тромбоцитопеническая пурпура, IgA-нефропатия и др. (всего более 90 наименований). Имеются данные, свидетельствующие о взаимосвязи H. pylori и развитии ревматических заболеваний (РЗ) – ревматоидного артрита, прогрессирующего системного склероза, синдрома Шегрена [3]. Однако для ревматологов клиническое значение H. pylori, прежде всего, определяется его ролью в развитии лекарственных осложнений противоревматической терапии.
Речь пойдет о НПВП-гастропатии – поражении верхних отделов желудочно-кишечного тракта (ЖКТ), которое возникает на фоне приема нестероидных противовоспалительных препаратов (НПВП). Хотя НПВП и H. pylori считаются независимыми факторами развития эрозивно-язвенных изменений ЖКТ, имеется ряд исследований, показывающих их негативный синергизм. Согласно последним международным рекомендациям по диагностике и лечению H. pylori-ассоциированной патологии (Маастрихтское соглашение V), выявление и эрадикация этого микроорганизма настоятельно рекомендуется в случае развития НПВП-гастропатии. Тестирование на H. pylori и проведение курса антихеликобактерной терапии также показано лицам, нуждающимся в приеме НПВП и имеющим такие факторы риска, как язвенный анамнез, выраженная диспепсия и сопутствующий прием препаратов, влияющих на свертывание крови [4].
К сожалению, российские ревматологи и терапевты не так часто проводят эрадикацию H. pylori в своей повседневной практике, передавая решение вопроса о целесообразности данной терапии «узким специалистам» – гастроэнтерологам. В определенной степени это связано с недостаточными знаниями проблемы заболеваний и состояний, ассоциированных с H. pylori. С другой стороны, многие российские врачи избегают назначения комбинированной антибактериальной терапии, опасаясь известных нежелательных реакций (НР) – прежде всего, развития дисбиоза кишечника и диареи, связанной с избыточным ростом условно-патогенной флоры.
Решить проблему может альтернативный режим эрадикации H. pylori. В частности, большой интерес представляет схема антибактериальной терапии, включающая нифурател и предложенная Научным обществом гастроэнтерологов России в рамках национальных российских рекомендаций по лечению заболеваний, ассоциированных с H. pylori [5].
Нифурател – производное нитрофурана, препарат широкого спектра действия, активный в отношении H. pylori; кроме антибактериальной активности, он также обладает противогрибковым и противопротозойным эффектом. Принципиальным достоинством нифуратела является способность подавлять условно-патогенную флору кишечника, не нарушая при этом микробного равновесия. Собственно, этот препарат активно используется в качестве системного кишечного антисептика. Поэтому риск развития НР со стороны кишечника при использовании такой схемы антихеликобактерной терапии может быть существенно меньше в сравнении со стандартными схемами, включающими макролиды. При этом также снижается необходимость в назначении пробиотиков для восстановления биоценоза кишечника [6–8].
С целью изучения влияния H. pylori на развитие НПВП-гастропатии и оценки эффективности альтернативной схемы эрадикационной терапии, содержащей нифурател (Макмирор®), нами проведено открытое исследование ГРАНАТ («Геликобактер в Ревматологии: Апробация Нифуратела при Антигеликобактерной Терапии»).
Материал и методы
На первом этапе исследования был проведен скрининг для определения частоты инфекции H. pylori у больных РЗ, регулярно принимавших НПВП. С этой целью всем пациентам, находившимся на стационарном лечении в клинике ФГБНУ «НИИР им. В.А. Насоновой» в период с 01.02.2017 по 31.03.2017 (2 календарных месяца) и направленным для проведения эзофагогастродуоденоскопии (ЭГДС), было выполнено тестирование на инфицированность данным микроорганизмом. Критериями включения в исследование принимались общие показания к ЭГДС (наиболее часто – регулярный прием НПВП, диспепсия или патология ЖКТ в анамнезе), регулярное, не менее 2-х недель, использование НПВП до момента направления на ЭГДС, а также подписанное информированное согласие.
Всего тестирование на H. pylori проведено 109 больным. Характеристика исследуемой группы представлена в таблице 1. В исследуемой группе преобладали женщины среднего возраста, страдающие ревматоидным артритом. Из НПВП пациенты в основном получали нимесулид, диклофенак и мелоксикам; существенная часть из них, кроме того, получали глюкокортикоиды и базисные противовоспалительные препараты (БПВП), в основном метотрексат. Серьезные факторы риска НПВП-гастропатии, такие как наличие язвенного анамнеза и прием низких доз аспирина, имелись менее чем у 10% обследованных. 
При выполнении ЭГДС оценивалось наличие эрозий (поверхностные дефекты слизистой, не имеющие видимой глубины) и язв желудка и/или дефекта стенки желудка/двенадцатиперстной кишки с видимой глубиной, ≥5 мм в диаметре.
H. pylori выявляли путем «настольного» уреазного теста. Предварительно всем больным во время ЭГДС выполнялась биопсия слизистой антрального отдела и нижней трети тела желудка (по 1 образцу); затем эти образцы помещались на специальную пластинку (ХЕЛПИЛ-бланк). Положительная уреазная реакция проявляется ярко-синей окраской индикатора ХЕЛПИЛ-бланка. Тест считался положительным при явном изменении окраски индикатора после контакта с биоптатом слизистой из любого участка желудка.
На втором этапе исследования оценивали эффективность режима эрадикационной терапии с применением нифуратела: омепразол 20 мг 2 р./сут + амоксициллин 1000 мг р./сут + нифурател (Макмирор®) 400 мг 2 р./сут в течение 10 дней. Это лечение проводилось всем больным, инфицированным H. pylori, у которых при выполнении эндоскопического исследования были выявлены эрозии и/или язвы желудка или имелся язвенный анамнез (всего 32 пациента).
Результат лечения оценивался спустя 6 нед. после курса антибактериальной терапии. Для оценки эрадикации (отсутствия) H. pylori в организме больных проводилась полимеразная цепная реакция (ПЦР) в кале.
Все данные, полученные в ходе исследования, с согласия больных вносились в анонимные исследовательские карты. Электронная база данных была создана при помощи программы Microsoft Office Excel 2011, статистический анализ проводился с использованием программы SPSS 17.0. Средние значения приведены в формате M+m. Для оценки статистической значимости отличия количественных параметров применен t-тест Стьюдента, качественные параметры оценивались с помощью показателя χ2, точного теста Фишера и показателя отношения шансов (ОШ).
Проведение настоящего исследования одобрено комитетом по этике при ФГБНУ «НИИР им. В.А. Насоновой» (протокол № 26 от 03.11.2016).
Результаты исследования
Уреазный тест оказался положительным у 61 больного (56,0%). Эрозии и язвы верхних отделов ЖКТ выявлены у 40 пациентов (36,7%), причем единичные эрозии (менее 10) – у 23 (21,1%), множественные эрозии (более 10) – у 8 (7,3%), язвы желудка – у 9 больных (8,3%).
Группы больных, инфицированных и не инфицированных H. pylori, достоверно не различались по среднему возрасту и полу (p<0,05). Имелась четкая достоверная разница в частоте эрозий и язв у больных, инфицированных и не инфицированных H. pylori (рис. 1). Как видно, эти изменения гораздо чаще отмечались у пациентов с положительным уреазным тестом (p<0,001). В частности, язвы желудка были выявлены у 7 инфицированных больных и лишь у 2-х неинфицированных. 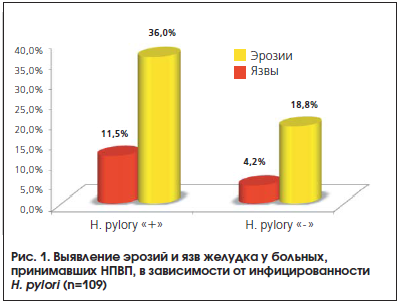
Суммарно риск (ОШ) выявления эрозии и/или язвы желудка у больных, инфицированных H. pylori, составил 3,68 (95% ДИ 1,56–8,68). Следует также отметить, что наличие гастралгий существенно чаще отмечалось у больных с H. pylori – у 19 (31,1%), чем у больных с отрицательным уреазным тестом – у 7 (14,6%), p=0,027.
Эрадикация H. pylori проводилась у 32 больных. Полный курс антибиотиков проведен практически у всех пациентов, лишь у одного из них лечение было прервано из-за развития кожной аллергической реакции. Кроме этого случая, других значимых НР не отмечено.
Через 6 нед. после окончания антихеликобактерной терапии эрадикация H. pylori (отрицательная ПЦР) была достигнута у подавляющего большинства больных (рис. 2). Инфицированность этим микроорганизмом сохранилась лишь в 4-х случаях. Результаты лечения еще 2-х пациентов остались неизвестными. 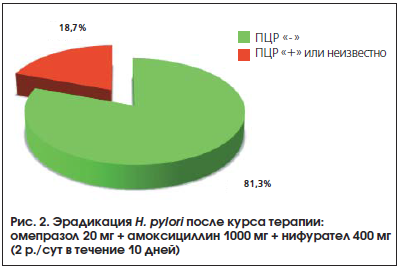
Обсуждение
Согласно полученным данным, H. pylori выявлен более чем у половины больных РЗ, принимавших НПВП. Надо признать, что небольшие размеры исследуемой группы не позволяют делать какие-либо выводы о реальной распространенности этой инфекции среди российских пациентов, тем более что ряд российских исследований демонстрируют существенно более высокий уровень инфицированности H. pylori в российской популяции – до 80–90% [9, 10].
Следует принять во внимание особенности контингента больных, включенных в наше исследование. На госпитализацию в клинику ФГБНУ «НИИР им. В.А. Насоновой» направляются пациенты из самых разных регионов нашей страны, причем обычно в состоянии обострения основного заболевания. Многие из них ранее получали антибиотики, а также ингибиторы протонной помпы (ИПП) в качестве гастропротекторов. Хорошо известно, что антибактериальная терапия и прием ИПП способны подавлять уреазную активность H. pylori, тем самым определяя ложноотрицательные результаты уреазного теста. Тем не менее обнаружение H. pylori более чем у 50% обследованных лиц указывает на серьезность данной проблемы и необходимость ее дальнейшего изучения.
Полученные нами результаты демонстрируют четкую взаимосвязь между наличием H. pylori и выявлением эрозий и язв желудка. Эти данные соответствуют литературным. Так, в 2002 г. J. Huang et al. провели метаанализ 16 рандомизированных контролируемых исследований (РКИ) (n=1625), в которых изучалась частота развития неосложненных и осложненных язв у пациентов, принимавших НПВП. Суммарно язвы были выявлены у 341 из 817 (41,7%) инфицированных H. pylori и у 209 из 808 (25,9%) неинфицированных (ОШ 2,12; 95% ДИ 1,68–2,67). Расчет показал, что сочетание H. pylori и приема НПВП повышало риск развития ЖКТ-кровотечения в 6,13 раза [11].
Похожие данные получены в относительно недавнем исследовании С. Sostres et al., которые исследовали причины развития язвенного кровотечения у 666 пациентов. Соответствующий по полу и возрасту контроль также составил 666 человек. H. pylori выявлен у 74,3% и 54,8% (ОШ 2,6; 95% ДИ 2,0–3,3), прием НПВП зарегистрирован у 34,5% и 13,4% (ОШ 4,0; 95% ДИ 3,0–5,4). В случае сочетания H. pylori и приема НПВП риск развития кровотечения резко возрастал (ОШ 8,0; 95% ДИ 5,0–12,8) [12].
Как уже отмечено выше, тестирование на H. pylori и проведение эрадикации при его выявлении у больных с высоким риском развития НПВП-гастропатии четко рекомендуется Маастрихтским соглашением V [4]. Это обосновано серией исследований, подтвердивших снижение риска серьезных ЖКТ-осложнений у пациентов, которым до назначения НПВП проводилась успешная антихеликобактерная терапия. С другой стороны, у лиц с уже развившейся патологией эрадикация H. pylori не снижает риска рецидивов язв и ЖКТ-кровотечения, если терапия НПВП продолжается, а дополнительная профилактика гастропротекторами не проводится.
Такой вывод подтверждают два метаанализа. Первый из них был представлен в 2005 г. М. Vergara et al., которые оценили результаты 5 РКИ (n=939). Согласно полученным данным, язвы желудка на фоне приема НПВП развились суммарно у 7,4% пациентов, прошедших эрадикацию, и у 13,3% – в группах контроля (ОШ 0,43; 95% ДИ 0,20–0,93). Необходимо отметить, что эрадикация обеспечила не только снижение частоты язв, но и снижение ЖКТ-кровотечений: их число составило 0 и 4 случая (ОШ 0,13; 95% ДИ 0,02–0,92). Однако анализ эффективности эрадикации H. pylori показал четкие различия в подгруппах пациентов, до включения в исследование еще не принимавших НПВП («НПВП-наивных») и уже получавших эти препараты. У первых эрадикация обеспечила значительное снижение риска развития НПВП-гастропатии (ОШ 0,26; 95% ДИ 0,14–0,49), у вторых же не да-вала положительного результата (ОШ 0,95; 95% ДИ 0,53–1,72) [13].
Более поздняя работа С. Tang et al. показала схожие результаты. По данным 7 РКИ, у больных после эрадикации и без нее число язв составило 6,4% и 11,8% соответственно (ОШ 0,50; 95% ДИ 0,36–0,74). Но также было отмечено существенное отличие между «НПВП-наивными» больными и лицами, длительно принимавшими НПВП. Если у первых эрадикация была однозначно эффективна для снижения частоты НПВП-гастропатии (ОШ 0,26; 95% ДИ 0,14–0,49), то у вторых достоверного уменьшения риска ЖКТ-осложнений не отмечено (ОШ 0,74; 95% ДИ 0,46–1,20) [14].
Яркими примерами отсутствия влияния эрадикации H. pylori на частоту рецидивов НПВП-индуцированных язв (после их успешного заживления) при продолжении НПВП-терапии могут служить классическое РКИ HELP-NSAID [15] и меньшее по масштабу открытое российское исследование [16].
Поэтому все больные, у которых развилась НПВП-гастропатия, в дальнейшем (после успешного заживления эрозий и язв желудка), при использовании НПВП, должны в качестве профилактики получать эффективный гастропротектор, например ИПП. Это положение четко отмечено в Маастрихтском соглашении V: «Утверждение 8. Тестирование на H. pylori следует выполнять у принимающих аспирин и НПВП с язвенным анамнезом… Таким образом, лечение ИПП является обязательным для тех, кто получает НПВП, коксибы или даже низкую дозу аспирина после язвенного кровотечения и эрадикации H. pylori при положительном тесте на эту инфекцию» [4].
Проводить эрадикацию H. pylori у больных, у которых на фоне приема НПВП развились язвы или ЖКТ-кровотечение, конечно же, необходимо. Ведь негативное действие инфекции H. pylori не исчерпывается только развитием НПВП-гастропатии. Нельзя забывать о хроническом гастрите и риске аденокарциномы, а также возможности заражения других лиц. В частности, до сих пор неизвестно, как протекает инфекция H. pylori на фоне снижения иммунитета, вызванного приемом синтетических и биологических БПВП для лечения ревматоидного артрита.
Необходимо отметить, что большинство пациентов с наиболее распространенными РЗ, такими как ревматоидный артрит и остеоартрит, не используют НПВП постоянно. На фоне активной патогенетической терапии основного РЗ потребность в обезболивающих средствах может быть сведена до минимума или вовсе исчезнуть. Если у пациента развилась НПВП-гастропатия и при этом выявлен H. pylori, устранение обоих этих факторов (отмена НПВП и эрадикация H. pylori) позволит в дальнейшем снизить риск развития патологии верхних отделов ЖКТ до минимума. В том случае, если потребность в НПВП возникнет вновь, отсутствие H. pylori станет важным фактором предупреждения рецидива поражения ЖКТ.
Наше исследование показало хороший результат применения альтернативной схемы эрадикации H. pylori с использованием нифуратела. Позитивный результат достигнут у 80% больных. При этом переносимость терапии оказалась благоприятной: лишь у одного пациента возникла аллергическая реакция, которая потребовала отмены лечения. Конечно, небольшой размер исследуемой группы и открытый характер исследования ограничивают оценку полученных результатов. Тем не менее, полученные данные представляют интерес как первый опыт применения альтернативной схемы антихеликобактерной терапии у пациентов с РЗ.
Наши результаты подтверждают данные о хорошей эффективности эрадикационных схем на основе нифуратела, показанные, в частности, в детской практике [7, 17]. Так, в работе О.Г. Шадрина и соавт. частота эрадикации H. pylori при использовании этого препарата достигала почти 90% [18].
Как уже отмечено выше, нифурател имеет серьезное преимущество в сравнении с другими антихеликобактерными средствами – он обладает свойствами кишечного антисептика. Нифурател относится к производным нитрофурана и имеет широкий спектр действия; важно, что к нему очень редко формируется устойчивость микроорганизмов. Подавление условно-патогенной флоры и пробиотическое действие нифуратела позволяют избежать развития дисбиотических нарушений и поддерживать нормальное состояние микробиоты кишки. Это принципиально важно при лечении ЖКТ-осложнений, вызванных НПВП. Дело в том, что негативное действие этих препаратов не ограничивается только верхними отделами ЖКТ. У больных, регулярно принимающих НПВП, нередко развивается поражение тонкой кишки – НПВП-энтеропатия. Данная патология относительно редко проявляет себя в виде манифестных форм – кишечного кровотечения, перфорации или формирования стриктур, но часто становится причиной развития медленно прогрессирующей железодефицитной анемии [19]. Имеются данные, что прием антибиотиков и ИПП – это основные компоненты «стандартной» эрадикационной терапии – существенно повышает риск развития НПВП-энтеропатии [20]. Напротив, кишечные антисептики, подавляющие условно-патогенную флору кишки (контаминация этих микроорганизмов играет ключевую роль в развитии энтеропатии), способны предотвращать развитие НПВП-энтеропатии [21]. Поэтому включение в схему эрадикационной терапии нифуратела представляется ценным элементом комплексной защиты ЖКТ от негативного действия НПВП.
Необходимы дальнейшие исследования в этом направлении. Однако полученные данные уже сейчас можно рассматривать как серьезное подтверждение целесообразности более широкого применения нифуратела для лечения и профилактики лекарственных осложнений в ревматологической практике.
Источник
Еще не так давно считалось, что гастрит вызывают неправильное питание, еда всухомятку, стрессы и отсутствие горячего супа на обед. Потом ученые обнаружили связь этой болезни с бактерией хеликобактер пилори — и с тех пор подход к лечению заболеваний ЖКТ кардинально изменился.
Можно ли заразиться через посуду в ресторане, вызывает ли хеликобактер рак и нужно ли избавляться от бактерии, которая живет в организме 80% белорусов, рассказал врач-гастроэнтеролог с 40-летним опытом работы Георгий Матвеевич Усов.
Георгий Усов,
врач-гастроэнтеролог высшей категории
Минского клинического консультативно-диагностического центра,
кандидат медицинских наук
— Что такое хеликобактер? Это патогенная бактерия или условно-патогенная?
— Хеликобактер пилори (Helicobacter pylori) — бактерия, которая была открыта австралийскими учеными Робином Уорреном и Барри Маршаллом. За это открытие в 2005 году они получили Нобелевскую премию.
Хеликобактер — патогенная бактерия. Наличие ее в организме человека приводит к поражению слизистой оболочки желудка и двенадцатиперстной кишки и развитию таких заболеваний, как хронический гастрит, язва желудка и двенадцатиперстной кишки, рак желудка, мальтома желудка.
Сегодня хеликобактер — самая распространенная хроническая инфекция в мире.
— Какие факторы в таком случае провоцируют развитие гастрита, язвы, рака? И могут ли эти болезни возникнуть без участия хеликобактера?
— При наличии хеликобактера у всех людей выявляется какое-либо заболевание желудка. Выявление конкретного заболевания зависит от штамма хеликобактера. Штаммы H. руlori, имеющие в своем составе определенные генотипы, предрасполагают к развитию язвенной болезни и рака желудка. И если язвой желудка и двенадцатиперстной кишки или онкологическими заболеваниями заболевают не все инфицированные люди, то гастритом — все.
Верно и то, что данные болезни могут возникать и без хеликобактер пилори.
- Кроме гастритов, связанных с хеликобактером, имеются гастриты, связанные с забросом содержимого двенадцатиперстной кишки в желудок, так называемые рефлюксные (химические) гастриты, гастриты, связанные с образованием антител к слизистой оболочке желудка (аутоиммунные гастриты).
- Причиной язв может быть прием нестероидных противовоспалительных препаратов, ацетилсалициловой кислоты, изредка нервные факторы, погрешности в еде.
- Причиной раковых заболеваний могут быть погрешности в питании, канцерогенные вещества, поступающие в пищу, курение, наследственная предрасположенность и др.
— Как передается эта бактерия человеку? Можно ли заразиться от животных? А в ресторане через посуду?
— Путь передачи хеликобактера контактно-бытовой. Бактерия передается:
- через недостаточно чистую посуду, когда люди едят из одной тарелки или пьют из одной чашки, едят пищу друг у друга;
- в семье, когда родители пробуют пищу перед тем, как дать ее ребенку, или облизывают соску малыша;
- в случае использования людьми одной зубной щетки;
- через губную помаду;
- при отсутствии мытья рук после туалета и перед едой;
- через сексуальные поцелуи.
Хеликобактер также выявлен у кошек и собак, вследствие чего существует возможность заражения человека от них. Что касается ресторана, то, если грязная посуда плохо обрабатывается, появляется высокая возможность заражения хеликобактером.
— Какой процент людей в Беларуси живет с хеликобактером? Почему этот показатель выше, чем в Западной Европе и США?
— Качественных эпидемиологических исследований по распространению хеликобактера среди населения Беларуси не проводилось. Проводились лишь относительно небольшие исследования среди населения отдельных областей и отдельных групп населения.
Считается, что распространенность хеликобактера среди белорусов составляет около 70-80%.
Среди населения РФ по ряду исследований в отдельных российских регионах распространенность составляет от 65 до 90%. Данный показатель выше, чем в Западной Европе и США, в связи с недостаточно качественным соблюдением гигиены в нашей стране.
— Какие симптомы должны заставить человека сдать анализ на хеликобактер? Какие из них неочевидные, не связанные напрямую с ЖКТ?
— Диспепсические расстройства (боли, жжение в эпигастральной области — верхних отделах живота, тошнота, плохой аппетит, тяжесть в эпигастральной области, рвота и т. д.) требуют обследования на хеликобактер.
В некоторых случаях хеликобактер может быть причиной также:
- железодефицитной анемии;
- халитоза (плохого запаха изо рта);
- крапивницы.
Однако следует помнить, что данные заболевания могут возникать и по множеству других причин.
— Какие анализы на выявление хеликобактер существуют? Какие из них самые объективные?
— Существует несколько разновидностей анализов.
- Гистологическое исследование биопсийного материала из слизистой желудка, причем следует исследовать слизистую как антрального отдела, так и тела желудка.
- Быстрый уреазный тест. Тест выполняется в момент гастроскопии. Биопсия слизистой берется из полости желудка, помещается в среду, содержащую мочевину и такой индикатор, как феноловый красный. Уреазы преобразуют мочевину в аммиак, вследствие чего повышается рН среды, и желтый цвет образца (отрицательный) меняется на красный (положительный).
- С13-уреазный дыхательный тест на немецкой аппаратуре, достоверность которого более 92%.
- Российская модификация дыхательного теста — хелик-тест, достоверность которого, по данным ряда российских авторов, составляет от 30 до 80%.
- Определение антител к хеликобактеру IgM и IgG в крови.
- Исследование антигенов хеликобактера в кале.
Самыми объективными из анализов являются гистологический тест, С13-уреазный дыхательный тест на аппаратуре немецкой фирмы FAN, исследование антигенов хеликобактера в кале и быстрый уреазный тест. Исследование крови на антитела к хеликобактер пилори приемлемо при первичном исследовании до лечения хеликобактера. В то же время для контрольного исследования оно не годится, так как антитела к хеликобактеру остаются повышенными в течение нескольких лет в крови после излечения от хеликобактера, давая ложноположительный результат.
Хелик-тест из-за низкой достоверности нигде в мире, кроме нескольких стран СНГ, не применяется.
Полезная ссылка Где сдать анализ на хеликобактер Каталог лабораторий в Минске
— Что делать, если анализ положительный? Влияет ли, например, количественное значение антител в крови на степень опасности бактерии для здоровья?
— При положительном анализе на хеликобактер решается вопрос о проведении антихеликобактерной терапии. На степень опасности для здоровья количественное значение хеликобактера существенного значения не имеет, ибо высокая обсемененность хеликобактером в ряде случаев в наших исследованиях приводила к значительно меньшим изменениям слизистой оболочки, чем низкая, или существенно не отличалась. Причина — в индивидуальной резистентности (восприимчивости) организма к хеликобактеру.
При незначительных превышениях IgA желательно провести другой метод исследования хеликобактера, например С13-уреазный дыхательный тест или исследование кала на антигены хеликобактера, чтобы подтвердить или опровергнуть положительный результат.
— Всегда ли положительный анализ говорит о необходимости лечения? В каких случаях хеликобактер не лечат?
— Раньше считалось, что лечение хеликобактера следует проводить, только если имеются клинические проявления заболевания. Сейчас в связи с выявлением существенной роли хеликобактера в развитии рака желудка лечение рекомендуют проводить всем больным с хеликобактерной инфекцией.
В некоторых странах, в частности, Японии, лечение хеликобактера проводится всем больным бесплатно. При этом тем людям, которые отказываются лечиться от хеликобактера, при развитии у них рака желудка не оплачивают страховку.
У лиц с язвами желудка и двенадцатиперстной кишки санация хеликобактера приводит к уменьшению появления новых язв в три раза.
Лечение хеликобактера НЕ проводят:
- больным с аллергией и/или непереносимостью препаратов, предназначенных для лечения хеликобактера;
- тем, у кого все схемы лечения оказались неэффективными;
- отказывающимся от лечения пациентам.
На мой взгляд, больным с хроническим гастритом, у которых имеются лишь незначительные изменения слизистой оболочки желудка, от лечения можно временно воздержаться.
Лечение детей не проводят: существует большая вероятность повторного заражения из-за нахождения в детском коллективе и развития ряда побочных реакций, особенно при повторном лечении. Для детей желательно выделение отдельной посуды и соблюдение правил личной гигиены.
— Какое лечение назначается?
— Излечиться от хеликобактера полностью возможно только при назначении антибиотиков и блокаторов протоновой помпы (антисекреторных лекарственных средств — прим. ред.), усиливающих эффект антибиотиков, в ряде случаев в сочетании с препаратами висмута.
В последнее время выявлено бактерицидное действие некоторых пробиотиков в отношении хеликобактера.
Например, существует препарат, содержащий инактивированные бактерии пробиотического штамма Lactobacillus reuteri. Однако подобные препараты полностью от хеликобактера не излечивают.
— Должны ли параллельно лечиться домашние? Может ли такое быть, что у одного из членов семьи есть хеликобактер, а у остальных — нет?
— Да, лечение взрослых членов семьи при наличии у них хеликобактера должно проводиться, детям из-за указанных выше причин — нет. При этом наличие хеликобактера у всех членов одной семьи необязательно. Это зависит от индивидуальной резистентности организма к бактерии. В исследованиях и клинической практике неоднократно были случаи, когда хеликобактер не обнаруживался у отдельных членов семьи. Поэтому лечению всегда должны предшествовать анализы.
По теме: Как понять, что у вас гастрит? Названы 7 признаков
Источник
