Интерстициальный нефрит при подагре клинически проявляется
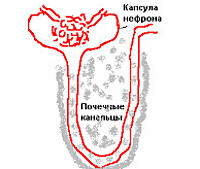
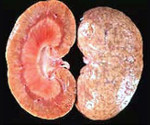
Интерстициальный нефрит — это острое или хроническое негнойное воспаление стромы и канальцев почек, обусловленное гиперергической иммунной реакцией. Проявляется болями в пояснице, нарушением диуреза (олигоанурией, полиурией), интоксикационным синдромом. Диагностируется с помощью общего и биохимического анализов мочи, крови, УЗИ почек, определения β2-микроглобулина, гистологического исследования биоптата. Схема лечения сочетает детоксикацию при отравлениях, этиопатогенетическую терапию основного заболевания с назначением иммуносупрессоров, антигистаминных средств, антикоагулянтов, антиагрегантов. В тяжелых случаях требуется проведение ЗПТ, трансплантация почки.
Общие сведения
Особенностью интерстициального нефрита является вовлечение в патологический процесс межуточной ткани, тубулярных структур, кровеносных и лимфатических сосудов без распространения на чашечно-лоханочную систему и грубой гнойной деструкции органа. Поскольку ведущую роль в патогенезе расстройства играет тубулярная дисфункция, в настоящее время заболевание принято называть тубулоинтерстициальным нефритом (ТИН).
По данным масштабных популяционных исследований, острые варианты интерстициального воспаления составляют до 15-25% всех случаев острого повреждения почек. Распространенность хронических форм заболевания по результатам пункционной нефробиопсии колеблется от 1,8 до 12%. Патология может развиться в любом возрасте, однако чаще наблюдется у 20-50-летних пациентов.

Интерстициальный нефрит
Причины
Поражение ренального канальцевого аппарата и межуточной ткани имеет полиэтиологическую основу, при этом роль отдельных повреждающих факторов отличается в зависимости от характера течения процесса. Основными причинами острого негнойного интерстициального воспаления почек, по наблюдениям специалистов в сфере урологии и нефрологии, являются:
- Прием нефротоксичных препаратов. Более 75% случаев острого тубулоинтерстициального нефрита развивается у чувствительных пациентов после приема антибиотиков, сульфаниламидов, НПВС, реже — тиазидных диуретиков, противовирусных средств, анальгетиков, барбитуратов, иммунодепрессантов.
- Аналогичный эффект могут вызывать вакцины и сыворотки.
- Системные процессы. У 10-15% больных патологические изменения в интерстициальной ткани и канальцах ассоциированы с аутоиммунными болезнями (синдромом Шегрена, СКВ), саркоидозом, лимфопролиферативными заболеваниями. В эту группу причин также входят случаи метаболических нарушений (гиперурикемии, оксалатемии) и острых токсических нефропатий.
- Инфекционные агенты. Хотя воспаление носит негнойный характер, у 5-10% пациентов оно возникает на фоне или после перенесенного инфекционного процесса. Интерстициальные формы нефрита могут осложнить течение бруцеллеза, иерсиниоза, цитомегаловирусной инфекции, лептоспироза, риккетсиоза, шистоматоза, токсоплазмоза, других инфекций, сепсиса.
- Неустановленные факторы. До 10% случаев внезапно развившегося нефрита с поражением интерстиция, канальцев имеют неуточненную этиологию и считаются идиопатическими. У части пациентов острая почечная патология сочетается с клиникой воспаления сосудистой оболочки глаз (синдром тубулоинтерстициального нефрита с увеитом).
Как и острые формы заболевания, хронический тубулоинтерстициальный нефрит может сформироваться на фоне длительного приема нефротоксичных лекарственных средств (в первую очередь НПВС, цитостатиков, солей лития), отравления ядами (солями кадмия, свинца). Патология часто возникает у пациентов с метаболическими расстройствами (подагрой, цистинозом, повышенными уровнями оксалатов, кальция в крови), аллергическими и аутоиммунными болезнями.
Хронический ТИН осложняет течение туберкулеза, заболеваний крови (серповидно-клеточной анемии, синдрома отложения легких цепей). У больных с аутосомно-доминантной тубулоинтерстициальной болезнью негнойный нефрит имеет наследственную основу. При длительной постренальной обструкции мочевыводящих путей (везикоуретеральном рефлюксе, аденоме предстательной железы, мочеточниково-влагалищных свищах и т. п.), атеросклерозе ренальной артерии, гломерулопатиях хроническое интерстициальное воспаление является вторичным.
Патогенез
Механизм развития интерстициального нефрита зависит от характера, интенсивности действия повреждающего фактора. Зачастую воспаление имеет аутоиммунную основу и провоцируется осаждением циркулирующих в крови иммунных комплексов (при лимфопролиферативных процессах, системной красной волчанке, приеме нестероидных противовоспалительных средств) или антител к базальной мембране канальцев (при интоксикации антибиотиками, отторжении трансплантата).
При хронизации процесса важную роль играет патологическая активация макрофагов и T-лимфоцитов, вызывающих протеолиз тубулярных базальных мембран и усиливающих перекисное окисление с образованием свободных радикалов. Иногда канальцевый эпителий повреждается в результате селективной кумуляции и прямого разрушающего действия нефротоксичного вещества, реабсорбируемого из первичной мочи.
Локальное выделение медиаторов воспаления в ответ на действие повреждающего фактора вызывает отек интерстиция и спазм сосудов, который усугубляется их механическим сдавлением. Возникающая ишемия почечной ткани потенцирует дистрофические изменения в клетках, снижает их функциональность, в части случаев провоцирует развитие папиллярного некроза и массивную гематурию.
Из-за повышения давления в канальцах и снижения эффективного плазмотока вторично нарушается фильтрующая способность гломерулярного аппарата, что приводит к почечной недостаточности и увеличению уровня сывороточного креатинина. На фоне отека межуточной ткани и повреждения канальцевого эпителия снижается реабсорбция воды, усиливается мочевыделение.
При остром течении нефрита постепенное уменьшение отека интерстициального вещества сопровождается восстановлением ренального плазмотока, нормализацией скорости клубочковой фильтрации и эффективности канальцевой реабсорбции. Длительное присутствие повреждающих агентов в сочетании со стойкой ишемией стромы на фоне нарушений кровотока влечет за собой необратимые изменения эпителия и замещение функциональной ткани соединительнотканными волокнами.
Склеротические процессы усиливаются за счет стимуляции пролиферации фибробластов и коллагеногенеза активированными лимфоцитами. Существенную роль в возникновении гиперергической воспалительной реакции играет наследственная предрасположенность.
Классификация
При систематизации клинических форм интерстициального нефрита принимают в расчет такие факторы, как наличие предшествующей патологии, остроту возникновения симптоматики, развернутость клинической картины. Если острое межуточное воспаление развивается у ранее здоровых пациентов с интактными почками, процесс считается первичным. При вторичном тубулоинтерстициальном нефрите почечная патология осложняет течение подагры, сахарного диабета, лейкемии и других хронических болезней. Для прогнозирования исхода заболевания и выбора оптимальной терапевтической тактики важно учитывать характер течения воспалительного процесса. Урологи и нефрологи различают две формы интерстициального воспаления:
- Острый нефрит. Возникает внезапно. Сопровождается значительными морфологическими изменениями стромы, канальцев, зачастую – обратимыми. Гломерулы обычно не повреждаются. Протекает бурно с выраженной клинической симптоматикой тубулярного поражения и вторичного нарушения клубочковой фильтрации. Часто наблюдается быстрое двухстороннее снижение или полное прекращение функции почек. Острые формы межуточного нефрита служат причиной 10-25% острой почечной недостаточности. Несмотря на серьезный прогноз, своевременное назначение адекватной терапии позволяет восстановить функциональные возможности органа.
- Хронический нефрит. Морфологические изменения развиваются постепенно, преобладают процессы фиброзирования интерстициальной ткани, атрофии канальцевого аппарата с его замещением соединительной тканью и исходом в нефросклероз. Возможна вторичная гломерулопатия. Симптоматика нарастает медленно, при выраженных склеротических процессах является необратимой. У 20-40% пациентов с хронической почечной недостаточностью нарушение фильтрующей функции почек вызвано именно тубулоинтерстициальным нефритом. Прогноз заболевания серьезный, при возникновении ХПН необходимо проведение ЗПТ и пересадка почки.
При остром воспалении оправдано выделение нескольких вариантов заболевания с разной выраженностью симптомов. Для развернутой формы нефрита характерна классическая клиническая картина. Отличительной особенностью тяжелого воспаления является ОПН с анурией, требующая срочного проведения заместительной почечной терапии. При благоприятно протекающем абортивном воспалении отсутствует олигоанурия, преобладает полиурия, концентрационная функция восстанавливается за 1,5-2 месяца. При развитии интерстициального очагового нефрита симптоматика стертая, превалирует нарушение реабсорбции мочи.
Симптомы интерстициального нефрита
Признаки заболевания неспецифичны, сходны с проявлениями других видов нефрологической патологии. Клиника зависит от особенностей развития воспалительного процесса. При остром нефрите и обострении хронического воспаления наблюдаются нарушения общего состояния — головная боль, ознобы, лихорадка до 39-40° С, нарастающая слабость, утомляемость. Возможно повышение артериального давления. В моче появляется кровь.
Пациент жалуется на сильные боли в пояснице, количество мочи резко уменьшается вплоть до анурии, которая впоследствии сменяется полиурией. При прогредиентном заболевании больного беспокоят тупые боли в области поясницы, незначительное снижение объема суточной мочи, папулезная сыпь. Иногда наблюдается субфебрилитет. О возможном снижении фильтрационной способности органа при хроническом варианте нефрита свидетельствует появление симптомов уремической интоксикации — тошноты, рвоты, кожного зуда, сонливости.
Осложнения
При отсутствии адекватной терапии острый интерстициальный нефрит зачастую переходит в хроническую форму. Изменения в почечном интерстиции со временем приводят к снижению количества функционирующих нефронов. Следствием этого является развитие хронической почечной недостаточности, инвалидизирующей пациента и требующей проведения заместительной терапии. Воспалительный процесс может вызвать активацию ренин-ангиотензин-альдостероновой системы, стимулировать повышенный синтез вазоконстрикторных веществ, что проявляется стойкой артериальной гипертензией, рефрактерной к медикаментозной терапии. Нарушение синтеза эритропоэтинов при хронических нефритах интерстициального типа становится причиной тяжелых анемий.
Диагностика
В связи с неспецифичностью клинической симптоматики при постановке диагноза интерстициального нефрита важно исключить другие причины острой или хронической нефропатии. Как правило, окончательная диагностика заболевания проводится на основании результатов гистологического исследования с учетом вероятных повреждающих факторов. Рекомендованными методами лабораторно-инструментального обследования являются:
- Общий анализ мочи. Характерна протеинурия — от небольшой и умеренной (суточное выделение с мочой 0,5-2 г белка) до нефротической (более 3,5 г белка /сут). У большинства больных определяется эритроцитурия, лейкоцитурия с наличием эозинофилов и лимфоцитов в моче. Возможна цилиндрурия. В анализе отсутствуют бактерии. Плотность мочи зависит от формы и стадии нефрита.
- УЗИ почек. Для острого интерстициального процесса типичны нормальные или несколько увеличенные размеры почек, повышение кортикальной эхогенности. При хроническом нефрите органы уменьшены, эхогенность усилена, у некоторых пациентов отмечается деформация контура. Исследование дополняют УЗДГ почек, выявляющим нарушение ренальной гемодинамики.
- Биохимический анализ крови. Результаты показательны при возникновении почечной недостаточности. Характерными признаками нарушения гломерулярной фильтрации служат повышение сывороточных уровней креатинина, мочевой кислоты, азота. Соответствующие изменения выявляются при проведении нефрологического комплекса и подтверждаются пробой Реберга.
- Бета-2-микроглобулин. Специфическим маркером нарушения реабсорбции в тубулярном аппарате является повышение экскреции β2-микроглобулина с мочой и снижение его уровня в крови. При межуточном нефрите сывороточная концентрация белка, определенная иммунохемилюминесцентным методом, не превышает 670 нг/мл, а его содержание в моче составляет более 300 мг/л.
- Пункционная биопсия почек. При остром процессе исследование биоптата позволяет обнаружить отек интерстиция, его инфильтрацию эозинофилами, плазмоцитами, мононуклеарные инфильтраты в перитубулярном пространстве, вакуолизацию канальцевого эпителия. О хроническом нефрите свидетельствует лимфоцитарная инфильтрация, атрофия канальцев и склероз стромы.
При хроническом интерстициальном воспалении наблюдается значительное снижение уровня эритроцитов и гемоглобина в общем анализе крови, при остром варианте нефрита возможна эозинофилия. Соответственно тяжести нарушений могут изменяться показатели электролитного баланса крови: увеличиваться или уменьшаться содержание калия, снижаться концентрации кальция, магния, натрия. При подозрении на возможную связь нефрита с системными заболеваниями дополнительно назначают анализы на выявление волчаночного антикоагулянта, антител к ds-ДНК, рибосомам, гистонам и другим нуклеарным компонентам. Часто определяется повышение уровней иммуноглобулинов — IgG, IgM, IgE.
Дифференциальная диагностика проводится между различными патологическими состояниями, которые осложняются интерстициальным воспалением. Заболевание также дифференцируют с острым, хроническим и быстропрогрессирующим гломерулонефритом, пиелонефритом, мочекаменной болезнью, опухолями почек. Кроме уролога и нефролога больным с подозрением на интерстициальный иммуновоспалительный процесс могут быть показаны консультации ревматолога, аллерголога-иммунолога, токсиколога, инфекциониста, фтизиатра, онколога, онкогематолога.
Лечение интерстициального нефрита
План ведения пациента определяется клинической формой и этиологическим фактором нефрологической патологии. Больных с симптоматикой острого межуточного нефрита экстренно госпитализируют в палату интенсивной терапии урологического или реанимационного отделения. При хроническом течении воспаления рекомендована плановая госпитализация в нефрологический стационар.
Основными терапевтическими задачами являются прекращение поступления и вывод из организма химического вещества, спровоцировавшего токсическое повреждение или гиперергическую иммуновоспалительную реакцию, десенсибилизация, детоксикация, стабилизация основного заболевания при вторичных формах нефрита, коррекция метаболических расстройств. С учетом стадии и течения болезни назначаются:
- Этиопатогенетическая терапия основного заболевания. Устранение причины, вызвавшей тубулоинтерстициальное воспаление, при отсутствии необратимых изменений канальцев и стромы позволяет быстрее нормализовать реабсорбционную и фильтрующую функции. При острых процессах, спровоцированных токсическими воздействиями, эффективны антидоты, энтеросорбенты, методы экстракорпоральной детоксикации. Грамотное лечение системных процессов направлено на предупреждение раннего развития ХПН.
- Иммуносупрессоры. При неэффективности детоксикационной терапии интерстициального медикаментозного нефрита, идиопатических формах заболевания, аутоиммунных болезнях часто применяют кортикостероиды в комбинации с антигистаминными средствами. Глюкокортикостероиды уменьшают отек межуточного вещества, ослабляют активность иммунного воспаления, противогистаминные препараты снижают выраженность гиперергического ответ. При дальнейшем нарастании симптоматики назначают цитостатики.
- Симптоматическое лечение. Поскольку острая почечная дисфункция зачастую сопровождается метаболическими расстройствами, пациентам с тубулоинтерстициальным нефритом показана интенсивная инфузионная терапия. Обычно под контролем диуреза вводят коллоидные, кристаллоидные растворы, препараты кальция. При аутоиммунных заболеваниях рекомендован прием антикоагулянтов, антиагрегантов.
- Для купирования возможной артериальной гипертензии используют блокаторы рецепторов ангиотензина.
При нарастании почечной недостаточности для предотвращения тяжелых уремических расстройств проводится заместительная терапия (перитонеальный диализ, гемодиализ, гемофильтрация, гемодиафильтрация). Больным с исходом хронического воспаления в выраженные склеротические изменения интерстициального вещества, атрофию канальцев и гломерул требуется трансплантация почки.
Прогноз и профилактика
При ранней диагностике и назначении адекватной этиотропной терапии полное выздоровление наступает более чем у 50% больных. Прогноз при интерстициальном нефрите благоприятный, если у пациента сохраняются нормальные показатели скорости гломерулярной фильтрации. Для предупреждения развития заболевания необходимо своевременное лечение инфекционных болезней почек, системных поражений соединительной ткани, ограничение приема нефротоксических препаратов (НПВС, антибиотиков из группы тетрациклина, петлевых диуретиков).
Меры индивидуальной профилактики нефрита включают употребление достаточного количества жидкости, отказ от самостоятельного приема лекарственных препаратов, прохождение регулярных медицинских осмотров, особенно при работе с производственными ядами.
Источник
Подагрическая нефропатия — это поражение почек, возникающее у больных подагрой. Может проявляться в разных вариантах, зачастую длительное время протекает бессимптомно. В последующем возможны почечные колики, дизурия, никтурия, олигурия, гематурия, боли в пояснице, артериальная гипертензия, спонтанное отхождение камней. Диагностируется с помощью определения уровня мочевой кислоты в моче и крови, УЗИ почек, исследования синовиальной жидкости, биоптатов суставных тканей и тофусов. Для лечения используют урикодепрессивные, урикозурические, урикоразрушающие препараты. По показаниям проводится массивная инфузионная терапия, заместительная терапия, хирургическое удаление камней.
Общие сведения
Подагрическая (мочекислая, уратная) нефропатия развивается у 30-70% пациентов с подагрой. Относится к категории собирательных понятий, объединяет все виды почечной патологии подагрического происхождения. Наиболее распространенной формой заболевания считается хронический интерстициальный нефрит, который у 17% больных на начальных этапах характеризуется эпизодами острой мочекислой обструкции почек и в 52% случаев сочетается с нефролитиазом.
В 30-40% урологическая патология является единственным проявлением нарушений метаболизма пуринов и служит «почечной» маской подагры. Как и основное заболевание, подагрическая нефропатия чаще выявляется у пациентов мужского пола. Актуальность своевременной диагностики нефрологического заболевания у больных, страдающих подагрой, связана с высоким риском развития ХПН.
Подагрическая нефропатия
Причины
Поражение почек при подагре провоцируется типичными для этого заболевания метаболическими нарушениями. Ключевым повреждающим фактором становится мочевая кислота, которая усиленно производится организмом больного из-за генетически обусловленной недостаточности фермента гипоксантин-гуанинфосфорибозилтрансферазы. Непосредственными причинами нефропатии являются:
- Гиперурикемия и урикозурия. Соли мочевой кислоты оказывают прямое токсическое воздействие на почечную паренхиму и вызывают обструкцию почечных канальцев, откладываясь в их просвете. Гиперурикемия также потенцирует усиление секреции ренина, фактора пролиферации сосудистых гладкомышечных волокон, тромбоксана.
- Кислая реакция мочи. При значительной урикозурии pH мочи может снижаться до 4,5-5,8, что облегчает преципитацию уратов в почках. Кислая моча усиливает дистрофию почечного эпителия, формирующуюся на фоне его постоянной травматизации камнями, становится питательной средой для размножения микроорганизмов.
Риск нефропатии при подагрическом процессе повышается у пациентов, которые злоупотребляют алкоголем, допускают погрешности в диете, употребляя в больших количествах мясо, бобовые и другие продукты, содержащие пурины. Уратное поражение почек чаще наблюдается у больных с абдоминальным ожирением, инсулинорезистентностью, сахарным диабетом. Провоцирующими факторами также могут стать длительное голодание, интенсивные тренировки и тяжелый физический труд, сопровождающиеся массивной анаэробной деструкцией белковых волокон. Уровень мочевой кислоты повышается при приеме салицилатов, диуретиков, ряда других лекарственных средств.
Патогенез
Механизм развития подагрической нефропатии основан на дисбалансе между высокой концентрацией мочевой кислоты и способностью к ее безопасной элиминации из организма. На фоне усиленного выделения мочевой кислоты клубочками и снижения pH мочи ураты начинают кристаллизоваться в почечных канальцах. В результате нарушается внутрипочечный пассаж мочи, усиливаются застойные явления, что опосредованно влияет на фильтрующую способность почек. Формирование и рост уратных конкрементов провоцируют дистрофические процессы в почечном эпителии.
Проникновение уратов в тубулоинтерстиций сопровождается воспалительной реакцией, усилением фиброгенеза, склерозированием паренхимы за счет образования соединительной ткани с последующим развитием почечной недостаточности. У части пациентов определенную роль в патогенезе нефропатии подагрического типа играют образование аутоиммунных комплексов, повреждающих мембраны клубочков, а также активация ренин-ангиотензиновой системы с возникновением артериальной гипертензии и нефроангиосклероза.
Классификация
Ключевыми критериями современной систематизации форм поражения почечных тканей при подагре являются тип морфологических изменений, острота течения и клиническая форма патологического процесса, этапность развития заболевания. У половины больных мочекислая нефропатия протекает по латентному типу с преимущественным поражением стромы, поздним появлением и медленным нарастанием симптоматики, у 30% — по острому или хроническому уролитиазному с повреждением канальцев, у 20% — по протеинурическому с преимущественным аутоиммунным поражением клубочкового аппарата.
Подагрическая нефропатия бывает острой и хронической. При остром уролитиазном процессе в канальцах, собирательных трубочках и почечных лоханках в большом количестве осаждаются кристаллы, что приводит к возникновению острой обструкции почек, болевому синдрому, в тяжелых случаях — острой почечной недостаточности. При подобном течении речь обычно идет об острой обструктивной мочекислой нефропатии.
Клинические варианты хронической подагрической почки соответствуют трем типам морфологических изменений почечной ткани. Соответственно специалисты в сфере урологии и нефрологии различают хронический тубулоинтерстициальный нефрит, уратный вариант мочекаменной болезни, подагрический гломерулонефрит. Более редкими формами нефрологической патологии у больных, которые страдают подагрой, являются тофусоподобные включения уратов в мозговое вещество почки и амилоидоз.
С лечебной и прогностической целью уточняют стадию хронического процесса. Постепенное нарушение функциональной состоятельности фильтрующего аппарата снижает компенсаторные возможностей почек по поддержанию нормальной концентрации мочевой кислоты, ухудшая прогноз заболевания. С учетом состояния клубочковой фильтрации выделяют три стадии развития хронической уратной нефропатии:
- I — подагрическая гиперурикозурия. Фильтрующая функция сохранена. В моче содержание мочевой кислоты обычно увеличенное, в крови — нормальное или слегка повышенное. Возможна микроальбуминурия. При правильно выбранной терапевтической тактике удается добиться стойкой коррекции состояния пациента.
- II — подагрическая гиперурикемия. Почки не справляются с повышенной уратной нагрузкой, нарушается осморегулирующая функция. Экскреция мочевой кислоты нормальная или незначительно повышена, ее содержание в крови существенно увеличено. Снижается плотность мочи. Прогноз становится более серьезным.
- III — подагрическая азотемия. Терминальная стадия заболевания, характеризующаяся наличием хронической почечной недостаточности. Лабораторное обследование выявляет высокую гиперурикемию, снижение суточной экскреции мочевой кислоты, повышение уровня креатинина в плазме крови.
Симптомы подагрической нефропатии
У 50% пациентов патология продолжительное время протекает латентно. Клиника зависит от формы и варианта течения мочекислой нефропатии. Для острой уратной обструкции характерно внезапное начало с возникновением интенсивной боли и тяжести в поясничной области, дизурическими явлениями, макрогематурией, резким уменьшением количества мочи. Почечная симптоматика нередко сочетается с подагрической суставной атакой. При уратном нефролитиазе с постепенным отложением солей и формированием камней периодически наблюдаются двухсторонние почечные колики с острой болью в области поясницы, иррадиирующей в бедро и пах, тошнотой и рвотой, напряжением мышц передней брюшной стенки, лихорадкой. Возможно спонтанное отхождение конкрементов.
При хроническом интерстициальном нефрите или гломерулонефрите основными проявлениями становятся стойкое повышение артериального давления, выявляемое у 70% пациентов, увеличение количества суточной мочи, усиление диуреза в ночное время. Изредка в моче появляется кровь. Симптоматика усугубляется при снижении фильтрующей функции подагрической почки: больных беспокоят постоянные ноющие боли, отмечаются расстройства мочеиспускания, гематурия, снижение объема мочи, выделенной за сутки. Важным признаком является красновато-бурый цвет мочи за счет окрашивания кристаллами мочекислого аммония.
Осложнения
При обструкции камнем мочеточника и затруднении пассажа мочи зачастую развивается гидронефроз с расширением чашечно-лоханочной системы и атрофией паренхимы почки. Повышенная продукция ренина при нефропатии приводит к стойкой артериальной гипертензии, которая с трудом поддается лечению. Вследствие застоя мочи происходит обсеменение мочевыделительного тракта микроорганизмами, у 75% больных возникает вторичный пиелонефрит. Серьезными осложнениями являются острая почечная недостаточность, требующая экстренной терапии, и нарастающая хроническая почечная недостаточность.
Диагностика
Диагностический поиск при подозрении на подагрическую нефропатию направлен на выявление характерных метаболических нарушений, возможных признаков уролитиаза, оценку функциональной состоятельности почек, исключение гиперурикемических расстройств неподагрического происхождения. Наиболее информативными для постановки диагноза являются:
- Определение содержания мочевой кислоты. Соответственно стадии уратной нефропатии может определяться гиперурикозурия (> 1100 мг/сут), гиперурикемия (> 500 мкмоль/л). Исследование дополняют общим анализом мочи, в котором выявляется стойко-кислая pH. У 67% пациентов снижена относительная плотность мочи (<1018), у 71% наблюдается протеинурия (<1г/л), у 37% — микрогематурия. Возможна лейкоцитурия, кристаллурия.
- УЗИ. При ультразвуковом исследовании почек эхо-признаки повреждения почечных структур обнаруживаются у 78,5% больных. Наиболее часто визуализируются конкременты, причем в трети случаев подагрический нефролитиаз является двухсторонним. Иногда просматривается от 1 до 3 почечных кист диаметром 0,5-4,0 см. Диагностическая ценность сонографии особенно высока с учетом рентген-негативности уратных камней.
- Исследование синовиальной жидкости. Метод поляризационной микроскопии применим при наличии суставной симптоматики. С его помощью в биологическом материале удается выявить внутриклеточные кристаллы мочевой кислоты, а также исключить другие причины болевого синдрома. Иногда более информативными оказываются биопсия тофусов (при их наличии), синовиальной оболочки и хряща пораженного сустава.
Для оценки фильтрующей функции проводится проба Реберга, назначается комплексный биохимический анализ крови (определение содержания креатинина, мочевины, калия, кальция, натрия, неорганического фосфора в сыворотке крови), лабораторный нефрологический комплекс (почечные пробы в моче). Из инструментальных методов могут применяться нефросцинтиграфия, экскреторная урография.
Подагрический вариант нефропатии дифференцируют с поражением почек при вторичных гиперурикемиях, вызванных бериллиозом, хронической свинцовой интоксикацией, саркоидозом, цистинозом, поликистозной болезнью, распространенным псориазом, миелопролиферативной болезнью, гипотиреозом, алкогольной зависимостью. Исключаются лекарственно-индуцированные гиперурикемические состояния, связанные с приемом тиазидных и петлевых диуретиков, нестероидных противовоспалительных средств, антибиотиков, цитостатиков, некоторых других препаратов. Кроме уролога или врача-нефролога по показаниям пациента консультирует ревматолог, дерматолог, эндокринолог, инфекционист, онколог, онкогематолог, токсиколог.
Лечение подагрической нефропатии
Основными терапевтическими задачами являются уменьшение синтеза мочевой кислоты, нефропротекция, улучшение почечной микроциркуляции, замедление прогрессирующего нефросклероза. Медикаментозное лечение обязательно дополняют коррекцией двигательного активности, питьевого режима и рациона. Пациентам с подагрическим поражением почек показаны минимально калорийные диеты с низким содержанием белка, частое щелочное питье, умеренные физические нагрузки для снижения веса. При выборе препаратов для терапии мочекислой нефропатии учитывают форму и стадию заболевания.
Схема ведения больных с острой уратной нефропатией аналогична терапии ОПН. При проходимости мочеточников и отсутствии анурии показана непрерывная инфузионная терапия под контролем диуреза с введением моносахаридов, многоатомных спиртов, физиологического или полиионных кристаллоидных растворов, петлевых диуретиков. Одновременно назначается обезболивание алкалоидами трополонового ряда, применяются ингибиторы ксантиноксидазы. Неэффективность интенсивного консервативного лечения, проводимого в течение 60 часов, является показанием для перевода пациента на гемодиализ.
Больным с хронической подагрической почкой проводится терапия, позволяющая откорректировать концентрацию мочевой кислоты, предупредить развитие возможных осложнений. При подборе препарата обязательно учитывают стадию патологического процесса и сохранность фильтрующей функции. Наиболее часто для лечения мочекислой нефропатии используют:
- Урикодепрессивные препараты. Ингибиторы ксантиноксидазы, глютаминфософорибозилтрансферазы и в меньшей степени карбоновые конъюгаторы фосфорибозилпирофосфата влияют на обмен ксантинов, нарушают синтез мочевой кислоты. За счет эффективного снижения гиперурикемии уменьшают выраженность урикозурии, а значит – и риск камнеобразования. Обладают умеренным нефропротективным эффектом: снижают выраженность протеинурии, синтез ренина, продукцию свободных радикалов, замедляют гломерулосклероз и нефроангиосклероз. Не рекомендованы при наличии ХПН.
- Урикозурические средства. За счет угнетения реабсорбции уратов усиливают экскрецию мочевой кислоты, однако увеличивают нагрузку на почки. Показаны при сочетании гиперурикемии с нормальным содержанием мочекислых солей в моче, отсутствии камней и сохраненной фильтрующей функции. С учетом индивидуальной чувствительности и возможных противопоказаний больным с подагрической почкой назначают производные и аналоги сульфинпиразона, цинхофена, пробенецида, 5-хлоробензоксазола, кебузона. Часть этих препаратов обладает умеренным диуретическим эффектом.
При наличии уролитиаза для растворения уратных конкрементов применяют урикоразрушающие средства на основе солей лития, пиперазина, фермента уратоксидазы, цитратных смесей. Эффективно сочетание основных противоподагрических препаратов с фитоуроантисептиками, предотвращающими пиелонефрит, физиотерапевтическими методиками (фототерапией, магнитотерапией, электроимпульсной терапией), санаторно-курортным оздоровлением.
При нарастании ХПН проводится заместительная почечная терапия (гемодиализ, перитонеальный диализ, гемофильтрация, гемодиафильтрация). Пациентам с крупными конкрементами, нарушающими пассаж мочи и раздражающими паренхиму, показана нефролитотомия, пиелолитотомия, перкутанная или дистанционная нефролитотрипсия.
Прогноз и профилактика
Болезнь характеризуется рецидивирующим течением с периодами обострения и ремиссии. Прогноз серьезный, в большинстве случаев через 10-12 лет от начала заболевания развивается ХПН. Для профилактики подагрической нефропатии пациентам с наследственной предрасположенностью рекомендуется соблюдать диету с ограничением мясных продуктов, животных жиров, копченостей, бобовых, из которых могут образоваться ураты, проходить скрининговые обследования с целью выявления патологии на ранней (бессимптомной) стадии.
Больным с диагностированной подагрой необходимо адекватное лечение основного заболевания, строгое соблюдение рекомендаций ревматолога по коррекции образа жизни и веса, отказ от алкоголя, осторожный подход при приеме препаратов, провоцирующих гиперурикемию, исключение чрезмерных физических нагрузок.
Источник
