Как лечить остеопороз при камнях в почках
Актуальность. Существует множество факторов риска развития и рецидива мочекаменной болезни (МКБ), в частности остеопороз. Остеопороз чаще встречается у больных с камнями почек в анамнезе. Увеличение выделения кальция почками – один из важных факторов возникновения и рецидива МКБ. У пациентов с МКБ ниже минеральная плотность костной ткани (МПКТ) и выше риск остеопороза с возникновением переломов.
Цель исследования: уточнение факторов риска остеопороза и их связи с экскрецией кальция при МКБ.
Материал и методы. С осени 2016 г. 44 больных МКБ прошли анкетирование с целью выявления факторов риска остеопороза. 30 пациентам выполнена двухфотонная рентгеновская денситометрия для измерения плотности костной ткани. У всех пациентов определялась суточная экскреция кальция.
Результаты. По результатам анкетирования, факторы риска остеопороза МКБ имели 20 (45,5%) пациентов без значимых различий по частоте распределения у мужчин и женщин (р = 0,2). Более чем один фактор риска остеопороза достоверно чаще отмечался у мужчин (р = 0,0382). Сниженная МПКТ значимо чаще выявлялась у пациентов с МКБ в возрасте 45 лет и старше (р = 0,0091). С возрастом у пациентов с МКБ увеличивается суточная экскреция кальция. Это характерно как для пациентов, не имеющих факторов риска остеопороза (р = 0,004), так и для пациентов с факторами риска остеопороза (р = 0,0123).
Выводы. У больных МКБ вне зависимости от пола обнаруживаются факторы риска остеопороза, при этом у мужчин имеют место несколько факторов. Наличие факторов риска остеопороза, выявленных анкетированием, подтверждается данными денситометрии поясничного отдела позвоночника и бедренной кости. Возраст – главный фактор гиперкальциурии для популяции в целом и для больных МКБ и/или остеопорозом.
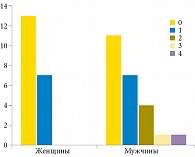
Рис. 1. Факторы риска остеопороза у мужчин и женщин с МКБ (n = 44)
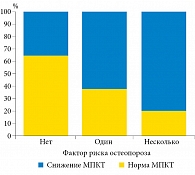
Рис. 2. Зависимость МПКТ от числа факторов риска остеопороза (n = 30)
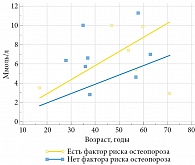
Рис. 3. Суточная экскреция кальция у больных МКБ разного возраста и факторы риска остеопороза (n = 14)
Актуальность
Метафилактика мочекаменной болезни (МКБ) основана на этиопатогенезе и факторах риска камнеобразования. Ее основная цель – снизить частоту рецидива и связанных с МКБ осложнений. В настоящее время разработаны методы комплексного обследования пациентов, а также обоснованные и эффективные методы поведенческой и лекарственной терапии рецидива камнеобразования [1, 2]. Многочисленные метаболические нарушения при МКБ требуют применения различных методов лечения [3].
К факторам риска образования камней относят наследственность, повышение уровня паратгормона, генетические причины, анатомические и уродинамические особенности. Ряд заболеваний, связанных с камнеобразованием (гиперпаратиреоидизм, заболевания желудочно-кишечного тракта), могут быть проявлением других патологических состояний, в частности остеопороза. Остеопороз широко распространен и признан социально значимой проблемой. Это прогрессирующее состояние, которое отражает нарушение обменных процессов в костной ткани и характеризуется снижением ее минеральной плотности (МПКТ) и архитектоники. Среди последствий остеопороза – увеличение частоты переломов и других патологий, связанных с состоянием скелета [4]. Прогрессирующее снижение МПКТ наблюдается преимущественно у лиц пожилого возраста, женщин в постменопаузе. Данное состояние сопровождается снижением уровня кальция в сыворотке крови и его повышенным выведением [5]. Изменение уровня паратгормона и эстрогенов влияет на выведение кальция из организма. Результатом этих процессов становится образование кальциевых камней в почках [6–10]. Сниженная МПКТ у мужчин с нефролитиазом встречается чаще, чем у мужчин без него. Это подтверждает взаимосвязь нарушений костно-кальциевого обмена и развития нефролитиаза [11, 12]. Тем не менее патогенез и факторы риска, связанные со снижением МПКТ и образованием кальциевых камней в почках, остаются предметом исследования [13–15].
В настоящее время установлено, что и при МКБ, и при остеопорозе изменяется динамика кальциевого обмена. Остеопороз характеризуется увеличивающейся с возрастом потерей кальция, в то же время повышенное выделение кальция – одна из главных причин возникновения и рецидива МКБ. Повышенное выделение кальция с мочой (гиперкальциурия) типично и для МКБ, и для остеопороза. Следствием снижения плотности костной ткани также является гиперкальциурия, которая ведет к камнеобразованию. Кроме того, камни в почках можно считать независимым фактором риска переломов. Пациенты с камнями почек нуждаются в дополнительном наблюдении относительно риска переломов позвоночника [16]. Частота остеопороза выше у больных с камнями почек в анамнезе [17]. Повышение выделения кальция почками – один из важных факторов возникновения и рецидива МКБ. У пациентов с МКБ снижена МПКТ и повышен риск остеопороза с возникновением переломов [18].
У остеопороза нет характерных клинических симптомов, поэтому особенно важно установить факторы риска этого заболевания [19]. Кроме того, на наш взгляд, уточнение факторов риска остеопороза при МКБ позволит прогнозировать вероятность камнеобразования в почках.
Материал и методы
С осени 2016 г. анкетирование для установления факторов риска остеопороза прошли 44 больных МКБ: 24 (54,5%) мужчины, 20 (45,5%) женщин. Средний возраст – 47,6 ± 14 лет. МКБ впервые диагностирована у 15 (34,1%), а повторно – у 29 (65,9%) пациентов.
30 пациентам выполнена двухфотонная рентгеновская денситометрия с целью определения МПКТ. Денситометрия аксиального скелета в настоящее время – стандартный метод диагностики остеопороза, с доказанной во многих исследованиях эффективностью при оценке риска переломов [19].
Все пациенты прошли комплексное обследование, в том числе обязательно определялась суточная экскреция кальция (референсные значения 2,5–7,5 ммоль/сут).
Полученные данные обработаны с помощью методов описательной статистики. Показатели представлены в виде среднего и стандартного отклонения, минимального и максимального значений. Сравнение данных выполнено с использованием критерия хи-квадрат и критерия Краскела – Уоллиса. Различия признавались значимыми при уровне р менее 0,05. Расчеты выполнены также с применением статистической программы MedCalc.
Результаты
По результатам анкетирования 24 (54,5%) пациента не имели факторов риска остеопороза. Факторы риска остеопороза выявлены у 20 (45,5%) больных МКБ: семи (15,9%) женщин и 13 (29,5%) мужчин, полученные результаты статистически не значимы (р = 0,2). Количество факторов риска остеопороза у мужчин и женщин с МКБ представлено на рис. 1. Более чем один фактор риска остеопороза достоверно чаще выявлялся у мужчин (р = 0,0382).
Была проанализирована зависимость факторов риска остеопороза от возраста. 19 (43,2%) пациентов были моложе 45 лет, 25 (56,8%) – в возрасте 45 лет и старше. Факторы риска остеопороза были выявлены у 14 пациентов в возрасте 45 лет и старше и только у шести пациентов в возрастной группе до 45 лет. Наличие и количество факторов риска в этих возрастных группах не имело статистически значимых различий (р = 0,1112 и р = 0,1577 соответственно).
30 пациентам выполнена рентгеновская двухфотонная денситометрия поясничного отдела и бедренной кости с целью уточнения плотности костной ткани (рис. 2). МПКТ последовательно снижалась с увеличением числа факторов риска остеопороза, результаты статистически не значимы (р = 0,1518). У мужчин соотношение количества факторов риска остеопороза и снижения МПКТ, по данным денситометрии, имело такую же тенденцию (р = 0,1096). У всех женщин с факторами риска остеопороза отмечалось снижение МПКТ.
По результатам денситометрии поясничного отдела и бедренной кости, снижение МПКТ чаще обнаруживалось у пациентов в возрасте 45 лет и старше по сравнению с больными в возрасте до 45 лет – 13 и двух человек соответственно (различие статистически значимо, р = 0,0091).
Один из наиболее значимых факторов возникновения и рецидива МКБ – избыточное выделение кальция почками. При остеопорозе наблюдается отрицательный баланс кальция. Суточная экскреция кальция у мужчин составила 6,6 (2,8–10), а у женщин – 5,7 (1,1–11,2) ммоль/л, разница статистически не значима (р = 0,81). Суточная экскреция кальция у пациентов до 45 лет составила 6,0 (2,8–10), а у пациентов в возрасте 45 лет и старше – 6,9 (1,14–11,2) ммоль/л, результаты статистически не значимы (р = 0,6373). У пациентов, имевших факторы риска остеопороза, суточная экскреция кальция составила 5,4 (1,14–9,9) ммоль/л, у пациентов без факторов риска остеопороза – 6,4 (2,8–11,2) ммоль/л, результаты статистически не значимы (р = 0,48), с одним фактором риска – 8,6 (3,5–9,9), а с несколькими – 2,9 (1,1–5,4) ммоль/л (р = 0,1169). У пациентов с нормальными значениями МПКТ суточная экскреция кальция составила 6,3 (2,8–11,2), а у пациентов со сниженной МПКТ – 6,9 (1,1–9,9) ммоль/л (р = 0,84). С возрастом у пациентов увеличивались показатели суточной экскреции кальция. Это характерно как для пациентов без факторов риска остеопороза (р = 0,004), так и для пациентов с установленными факторами риска (р = 0,0123) (рис. 3).
Обсуждение
Существуют обоснованные предположения, что физиологические и патологические изменения обмена кальция могут оказывать влияние на возникновение и рецидив МКБ. Поскольку типичных клинических признаков остеопороза, кроме состоявшегося перелома, не существует, то основной метод диагностики остеопороза – выявление факторов риска.
По результатам анкетирования, факторы риска остеопороза имели 20 (45,5%) пациентов без значимых различий по частоте распределения у мужчин и женщин, страдающих МКБ. Таким образом, независимо от пола у больных МКБ существуют условия, способствующие гиперкальциурии.
Факторы риска остеопороза определялись у пациентов с МКБ вне зависимости от возраста. При этом у мужчин количество факторов риска остеопороза было больше, чем у женщин. У мужчин чаще наблюдались факторы риска в разных комбинациях: переломы у родителей, у самих пациентов, прием кортикостероидов, злоупотребление алкоголем, диарея и эректильная дисфункция. Кроме того, сочетание факторов риска остеопороза обладает кумулятивным эффектом [19].
Результаты рентгеновской двухфотонной денситометрии поясничного отдела и бедренной кости подтвердили снижение МПКТ у пациентов с факторами риска остеопороза. Отсутствие значимых соотношений между данными анкетирования и результатами денситометрии могут объясняться длительным воздействием факторов риска и продолжительной реакцией костной ткани на данные воздействия. Таким образом, факторы риска остеопороза и сниженная МПКТ были характерны как для мужчин, так и для женщин.
Отмечено значимое преобладание частоты сниженной МПКТ с возрастом у пациентов (р = 0,0091). Так, снижение МПКТ выявлено только у двух пациентов в возрасте до 45 лет и у 13 пациентов в возрасте от 45 лет и старше.
Основной результат физиологических и патологических процессов в костной ткани, которые развиваются с возрастом, – изменение экскреции кальция почками. Это представляет не только теоретический, но и практический интерес с точки зрения диагностики предпосылок рецидива МКБ у больных, прошедших лечение.
Суточная экскреция кальция у пациентов с МКБ составила 6,3 (1,14–11,2) ммоль/сут. Статистически значимых различий показателя суточной экскреции кальция в зависимости от пола не выявлено (р = 0,81). При сопоставлении показателей суточной экскреции кальция с возрастом отмечена положительная значимая корреляция как в отсутствие факторов риска остеопороза (р = 0,004), так и при их наличии (р = 0,0123).
Выводы
У больных МКБ вне зависимости от пола обнаруживаются факторы риска остеопороза, при этом у мужчин они встречаются чаще. Выявленные факторы риска остеопороза подтверждаются данными денситометрии поясничного отдела позвоночника и бедренной кости.
Усиление экскреции кальция, характерное для остеопороза, обнаруживается и у пациентов с МКБ. Возраст – главный фактор гиперкальциурии и для популяции в целом, и для больных МКБ и/или остеопорозом.
По нашему мнению, выявление факторов риска остеопороза позволит своевременно диагностировать данное состояние, а лечение – замедлить развитие патологических изменений костной ткани, уменьшить потери кальция с мочой и потенциально предотвратить развитие и прогрессирование МКБ.
Источник
. |
| |||||||||||||
Источник
