Клинический случай реактивный артрит
Реактивный артрит (РеА) — иммуновоспалительное заболевание суставов, которое возникает одновременно с инфекционным процессом или вскоре после него и является системным клиническим проявлением этой инфекции.
Заболевание наиболее часто встречается у лиц молодого возраста (20-40 лет), при этом мужчины страдают реактивным артритом значительно чаще, чем женщины. Свыше 85 % больных являются носителями HLA-В27-антигена.
Термин «реактивный артрит» как нозологическая форма впервые был предложен в 1969 г. финскими исследователями P. Ahvonen, К. Sievers и К. Aho, описавшими артрит после перенесенной иерсиниозной инфекции. При этом подразумевалось, что реактивный артрит относится к «стерильным» воспалительным заболеваниям суставов, при которых в синовиальной жидкости и синовиальной оболочке больных не обнаруживаются ни патогенные микроорганизмы, ни их антигены. Однако в дальнейшем с помощью молекулярно-биологических методов исследования было показано, что у ряда больных реактивным артритом в синовиальной жидкости и синовиальной оболочке обнаруживаются не только бактериальные антигены (в частности, ДНК и РНК хламидий), но и микроорганизмы, способные к размножению. В связи с полученными фактами в последние годы наблюдается тенденция к сокращению группы собственно реактивных артритов и расширение группы инфекционных артритов.
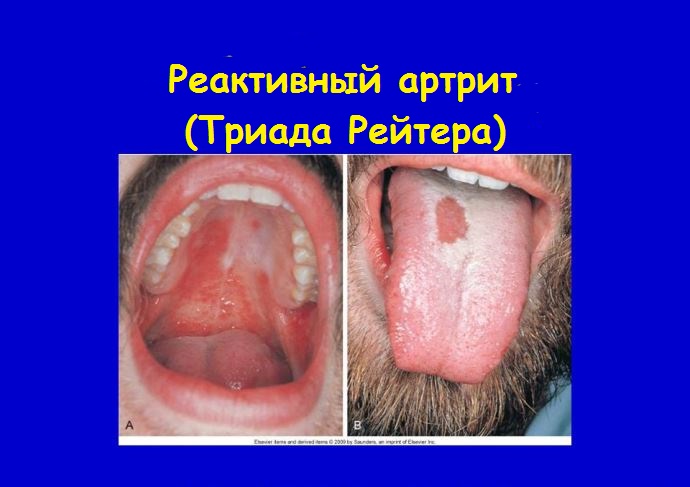
Клинически реактивный артрит проявляется воспалительным процессом в мелких суставах нижних конечностей, который сочетается в некоторых случаях с типичными для спондилоартропатии признаками — энтезопатиями и болями в нижних отделах спины. У некоторых больных наблюдается характерная триада — артрит, конъюнктивит и уретрит, что составляет симптомокомплекс болезни Рейтера. При реактивном артрите могут наблюдаться и системные проявления заболевания — в частности, ирит, изъязвления слизистой оболочки полости рта, кератодермия (keratodermia blenorragica), поражения сердца и нервной системы.
Этиология реактивного артрита.
В отличие от большинства других артритов, этиология которых не установлена, при реактивном артрите существует четкая хронологическая связь с экзогенным провоцирующим фактором, известны генетические маркеры и хорошо изучен клеточный и гуморальный иммунный ответ, развивающийся на причинный антиген.
По этиологическому фактору реактивные артриты подразделяются на две группы: постэнтероколитические и урогенитальные. Среди кишечных патогенов, способных вызвать заболевание, следует выделить иерсинии, сальмонеллы, кампилобактер и шигеллы. Ведущим возбудителем урогенитальных реактивных артритов является Chlamidia trachomatis, которая выявляется у 50-65 % больных. Роль данного микроорганизма при урогенитальных реактивных артритах подтверждается обнаружением его в соскобах эпителия уретры и цервикального канала, выявлением хламидийных антигенов в синовиальной жидкости больных, а также обнаружением ДНК и РНК хламидий в синовиальной оболочке пораженных суставов. При этом Chlamidia trachomatis практически единственный из триггеров реактивного артрита, который выявляется в пораженных суставах больных теми методами исследования, которые подтверждают жизнеспособность микроорганизма, — культуральными и молекулярно-биологическими.
Следует отметить, что за последние десятилетия произошли существенные изменения в составе провоцирующих микроорганизмов. Так, в спорадических случаях реактивного артрита частота инициации болезни хламидией осталась постоянной, в то время как частота возникновения артритов, связанных с перенесенной иерсиниозной инфекцией, снизилась в соответствии со снижением частоты возникновения кишечных инфекций в целом.
Понятие «реактивный артрит» иногда используют для определения артритов, развитие которых связано с уреаплазменной, микоплазменной, клостридиальной, боррелиозной, стрептококковой инвазией, а также вирусными инфекциями. Однако в этих случаях, как правило, нет ассоциации с HLA-B27. На IV Международном совещании по реактивным артритам, проходившем в Германии в 2000 г., было принято решение эти заболевания относить к группе «артритов, связанных с инфекцией».
Патогенез реактивного артрита.
В патогенезе реактивного артрита основная роль отводится нарушению иммунного ответа с преимущественной «заинтересованностью» клеточного звена иммунитета с развитием гипериммунного ответа организма на прямую инвазию микроорганизма в полость сустава или на инфекцию, имеющуюся вне сустава. При этом внутриклеточные микроорганизмы могут вызывать повреждение тканей либо путем прямого токсического воздействия на клетку-хозяина (цитопатический эффект), либо инициацией антибактериального иммунного ответа, который при своей неэффективности в отношении причинного микроорганизма сам индуцирует повреждение тканей (нецитопатический эффект). В частности, при реактивных артритах, вызванных С. trachomatis, в синовиальных выстилках нередко определяются живые бактерии. Более того, в реакции полимеразной идентификации в суставных тканях, по данным ряда исследователей, определяется не только хламидийная ДНК, но и первичные хламидийные м-РНК транскриптанты. С учетом того, что период полужизни их очень короткий, наличие проявленией транскрипции доказывает присутствие жизнеспособных и метаболически активных хламидий.
На сегодняшний день имеется много доказательств, что хламидии и иерсинии способны инициировать цитотоксический Т-клеточный ответ, при этом активация и пролиферация CD8+ Т-лимфоцитов, ответственных за элиминацию причинных микроорганизмов, осуществляемую при участии антигена HLA-B27 и цитокинов, приводит к повреждению синовиальной оболочки. Образующиеся в большом количестве иммунные комплексы фиксируются в суставных тканях, вызывая гиперпродукцию провоспалительных цитокинов (простагландина Е2, интерлейкина-1β, фактора некроза опухолей-α и др.), что приводит к индукции и поддержанию воспалительного процесса в суставах.
О значении генетических факторов в патогенезе реактивного артрита свидетельствует тесная ассоциация с антигеном HLA-B27 (на сегодняшний день известно уже 25 субтипов антигенов — от HLA-B2701 до В2725), который выявляется при урогенитальных РеА в 80-90 % случаев и в 70 % — при постэнтероколитических артритах. Согласно гипотезе антигенной мимикрии, рецепторное сходство между антигеном HLA-B27 и бактериальными пептидами способствует их длительной персистенции в организме пациента и стимуляции выработки антител, направленных против собственных тканей организма, в частности синовиальной оболочки и хрящевой ткани суставов. У пациентов-носителей HLA-B27 антигена определяется низкий уровень элиминации S. typhymurium, при этом он еще более низкий у HLA-B27+ больных реактивным артритом. Некоторые исследователи объясняют этот феномен способностью липополисахаридных компонентов клеточной стенки микроорганизма стимулировать гиперпродукцию ИЛ-10 Т-лимфоцитами, что может способствовать персистенции иммуновоспалительных изменений.
Более предпочтительной является теория «артритогенного пептида», согласно которой HLA-B27 является единственной из молекул главного комплекса гистосовместимости I класса, способной представлять артрит-индуцирующий пептид или пептиды цитотоксическим Т-лимфоцитам CD8+ (схема 2). Известно, что артритогенный пептид является компонентом клеточной стенки этиотропных бактерий, а для аутоиммунных процессов характерно образование антител, реагирующих как с антигенами микроорганизмов, так и перекрестно с поврежденными собственными тканями. На сегодняшний день известно около 60 хламидийных пептидов, которые в соответствии со своей аминокислотной последовательностью могут связываться с HLA-B27. Более того, один из таких пептидов (хит-шоковый протеин 70) оказался способным активировать цитотоксические Т-лимфоциты больных реактивным артритом.
С практической точки зрения патогенез реактивного артрита можно условно подразделить на три фазы: инициации, острого реактивного артрита и хронического реактивного артрита. В фазе инициации пациент подвергается воздействию патогенных микроорганизмов, что клинически проявляется инфекционным процессом (энтероколит или уретрит) с характерной клинической симптоматикой. У большинства больных происходит полное излечение без каких-либо последствий, однако у некоторых развивается реактивный артрит. Для фазы острого реактивного артрита характерно развитие синовита, а признаки спондилоартропатии развиваются в основном у носителей HLA-В27-антигена. В случае хронического реактивного артрита также возможны клинические различия между пациентами с HLA-B27+ и HLA-B27-, при этом у больных с HLA-B27+ большая вероятность развития рецидивирующих форм заболевания.
Болезни суставов
В.И. Мазуров
Источник
Реактивный артрит — воспаление суставов на фоне половой или кишечной инфекции. Чаще всего оно встречается у мужчин 20-40 лет, реже — у женщин такого же возраста, еще реже — у людей старшего возраста и подростков.
Историческая справка
В 1969 году финские ревматологи доказали связь артрита с колитом, вызванным бактериями рода иерсиний. От острых инфекционных артритов он отличался тем, что микробы не обнаруживались в синовиальной оболочке. Финны предложили выделить его в отдельную нозологическую форму и дали ему название — реактивный артрит.
Наука не стоит на месте и через десяток лет был изобретен новый микробиологический метод исследования — иммуноцитохимический. С его помощью обнаружили, что при реактивном артрите в клетках синовиальной оболочки содержатся частицы бактерий. В 90-х годах прошлого века в лабораториях стал использоваться анализ ПЦР. Он позволяет выявить ДНК микробов в синовиальной жидкости.
Причины возникновения
Ученым пока не известно, почему у одних людей суставы реагируют на инфекцию, а у других — нет. Предполагают, что реактивный артрит возникает у носителей HLA-B27 антигена.
Этот антиген является рецептором для бактерий. Он связывается с ними и способствует их транспортировке в разные ткани организма, включая синовиальную оболочку. Чаще это возбудители кишечных инфекций:
- шигеллы;
- иерсинии;
- сальмонеллы;
- бластоцисты;
- кампилобактер;
- клостридии.
В два раза реже — возбудители половых инфекций (хламидиоза, гонореи и др.).
Энтероколитический реактивный артрит чаще всего развивается после дизентерии, урогенитальный — на фоне хламидиоза.
Присутствие патогенных микроорганизмов или их частей является мощным раздражителем для иммунной системы. Причем иммунные клетки атакуют не только чужеродные агенты, но и клетки своих же суставов и других органов, которые контактировали с возбудителем инфекции. Из-за этого в них развивается аутоиммунное воспаление.
Клиника реактивного артрита

Чаще всего болезнь поражает суставы ног — большого пальца, голеностопные, коленные, пяточные сухожилия. Если воспаление касается рук, то страдают лучезапястные, локтевые суставы.
В целом для реактивного артрита характерны:
- поражение немногих суставов (от одного до трех);
- асимметричность;
- ночные боли;
- вовлечение в процесс сухожилий и связок;
- сопутствующий уретрит или конъюнктивит;
- сосискообразный вид пальцев;
- поражение подошвенной поверхности стоп и ногтей.
Как и при всех артритах, суставы опухают, кожа над ними краснеет, становится горячей.
Конъюнктивит клинически проявляется покраснением склер, ощущением песка в глазах, уретрит — частым болезненным мочеиспусканием.
Существует особая форма реактивного артрита, при которой воспаление суставов сочетается с конъюнктивитом и уретритом одновременно. Она называется синдромом (триадой) Рейтера.

И при обычном реактивном артрите, и при синдроме Рейтера изменяются подошвенные поверхности стоп. Сначала они покрываются красными пятнами. В центре пятен образуются зоны повышенного ороговения — гиперкератоза, проще говоря, затвердения кожи. Постепенно они распространяются на всю подошву. Утолщенная кожа отслаивается.
Ногти на ногах тоже реагируют на воспаление. Они утолщаются, желтеют и разрушаются. Поражение подошв и ногтей не вызывает болевых ощущений, поэтому человек не придает им значения.
В редких случаях наблюдаются другие системные проявления:
- увеличение лимфузлов (особенно паховых);
- баланит (воспаление кожи головки пениса);
- ирит (воспаление радужки глаза);
- образование язв на слизистой рта;
- гломерулонефрит;
- поражение сердца (миокардит, недостаточность аортального клапана, перикардит);
- полиневрит;
- плеврит.
Как протекает реактивный артрит?
Болезнь возникает остро через 2 недели-месяц после перенесенной инфекции. Симптомы сохраняются, в среднем, от 3 до 6 месяцев, редко — до года и дольше. Затем, в большинстве случаев, наступает стойкая ремиссия или полное выздоровление.
У 15-20% больных процесс хронизируется. Так бывает при урогенитальном реактивном артрите, особенно часто — при синдроме Рейтера. Причиной частых рецидивов могут быть невылеченная хламидийная инфекция и повторное заражение.
Рецидивы, как правило, протекают более тяжело — воспаляется все большее число суставов, поражаются глаза, слизистые оболочки, кожа, мочеиспускательный канал.
При длительном течении реактивный артрит может трансформироваться в ревматоидный, лечение которого требует гораздо больших усилий.
Принципы диагностики
Отличить реактивный артрит от другой патологии суставов непросто. Обычно врач предполагает его наличие, если пациент молод, воспаление суставов несимметрично, сопровождается ночными болями. Когда артрит сочетается с поражением глаз, стоп, мочеполовых органов, кишечника, постановка диагноза не вызывает затруднений.
Нередко клиническая картина болезни бывает стертой, нетипичной или слишком похожей на другие заболевания (так, сосискообразная деформация пальцев характерна и для псориатического артрита). Тогда на помощь приходят дополнительные методы исследования.
Всех пациентов с подозрением на реактивный артрит обязательно направляют на анализы крови. В них чаще всего находят:
- повышение СОЭ;
- повышенный уровень СРБ, серомукоида, сиаловых кислот;
- лейкоцитоз;
- нормохромную анемию;
- антиген HLA-B27.
Антинуклеарный и ревматоидный фактор в крови отсутствуют, что косвенно подтверждает диагноз.
В общем анализе мочи при урогенитальном реактивном артрите обнаруживают большое количество лейкоцитов, небольшое — эритроцитов (микрогематурия), белок. Посев мочи позволяет выявить возбудителя инфекции. Для диагностики хламидиоза также делают соскобы из уретры и канала шейки матки.
Для выявления кишечной инфекции применяют серологические методы — определение в крови антител к иерсиниям, сальмонеллам, кампилобактеру. Сальмонеллы и шигеллы можно обнаружить при бактериологическом анализе фекалий.
Существует правило: каждый больной реактивным артритом должен быть обследован на гонорею и ВИЧ-инфекцию.
Если возникает необходимость дифференцировать реактивный артрит от септического, исследуют синовиальную жидкость. Она имеет признаки воспаления: плохое образование муцинового сгустка, низкую вязкость, повышенное содержание лейкоцитов (5-10 тысяч на мкл, при септическом — 20-100 тысяч), среди которых преобладают сегментоядерные нейтрофилы.
Чтобы исключить другие ревматические болезни, делают рентгенографию крестцово-подвздошных сочленений. На снимке при длительном течении артрита можно увидеть сакроилеит справа или слева. Асимметричность поражения говорит в пользу инфекционной природы заболевания.
Лечение
Современные лабораторные методы позволяют не только выявить возбудителя болезни, но и определить, какие антибиотики могут с ним справиться. При воспалении, вызванном хламидиями, обычно назначаются азитромицин, кларитромицин, доксициклин, фторхинолоны. Курс лечения длится от 10 до 30 дней, иногда — до 3 месяцев.
Необходимость лечения антибиотиками реактивного артрита, возникшего после кишечной инфекции, не доказана.
Чтобы подавить воспаление в суставах и избавить пациента от боли, применяются НПВС, при высокой активности процесса — глюкокортикоидные гормоны.
Казалось бы, лечение не должно представлять трудностей: назначили антибиотик — победили болезнь. Но на деле все оказывается сложнее. Даже если бактерий уже нет в организме, остаются нарушения деятельности иммунной системы. Поэтому при длительно текущем обострении больным назначают иммуномодуляторы (метотрексат, азатиоприн, сульфасалазин). В последнее время они используются все реже, так как их эффективность при серонегативных спондилоартритах вызывает большие сомнения.
Реактивные артриты протекают относительно доброкачественно, не приводя к тяжелым нарушениям функций суставов. Поэтому необходимости в оперативном лечении, как правило, не возникает.
Меры профилактики

Болезнь несложно предотвратить, если соблюдать простые правила:
- часто мыть руки;
- правильно хранить и готовить пищу;
- пить только очищенную воду;
- избегать случайных половых контактов.
Если один половой партнер заболел, второй должен быть обследован на наличие половой инфекции и пролечен.
Источник
Реактивный артрит (синдром Рейтера), его трудно диагностировать, но найти его причины еще сложнее. Однако было замечено, что реактивный артрит обычно развивается после инфекций, в том числе мочеполовой системы (например, хламидии). Каковы причины и симптомы реактивного артрита? Каково лечение?
Реактивный артрит также известный как синдром Рейтера, синдром Физингера и Лерои или постинфекционный артрит, является заболеванием, которое относится как к системным заболеваниям, так и к серонегативному спондилоартриту — группе ревматических заболеваний, которые приводят к артриту с сопутствующим воспалением позвоночника.
Суть реактивного артрита — нездоровое воспаление суставов, связанное с предыдущей инфекцией пищеварительной системы, урогенитальным трактом или, реже, с дыхательной системой. Кроме того, есть признаки других систем и органов.
Частота реактивного артрита в мире оценивается в 30-200 / 100 000.
Реактивный артрит — причины и факторы риска
Точные причины реактивного артрита неизвестны, однако два фактора — инфекционные (бактериальные) и генетические (HLA B27) играют важную роль в его развитии.
Согласно наблюдениям врачей, заболевание обычно является осложнением после бактериальной инфекции пищеварительной системы, мочеполовой системы или, реже, респираторной системы, которая чаще всего вызывается бактериями.
Важную роль играет также присутствие антигена HLA B27 (происходит у 65-80% пациентов). Это белок, который помогает иммунной системе распознавать собственные клетки и различать самость и чужеродные антигены. Его присутствие связано с риском развития нескольких аутоимунных заболеваний (в которых организм нападает сам). Считается, что риск развития реактивного артрита в 50 раз выше у людей с нынешним антигеном HLA B27, чем у людей, которые этого не делают. Однако его роль в развитии болезни четко не объясняется.
В свою очередь, факторы риска — пол (симптомы реактивного артрита чаще встречаются у мужчин, чем у женщин) и возраста (заболевание чаще всего появляется у людей в возрасте 20-40 лет).
Реактивный артрит — симптомы
- артрит — односоединение или асимметричное воспаление нескольких стадий (в основном, колено и лодыжка, запястье и межфаланговые руки) — характерна боль колена, голеностопного сустава или стопы, боль и отек пальцев (так называемые колбасные колпачки);
- воспаление сухожильных приступов — симптомы — это боль в пятке, симптомы воспаления ахиллова сухожилия, симптомы так называемого «локоть теннисиста» или «локоть игрока в гольф»;
- воспаление позвоночника — боль в пояснице (боль в спине), скованность позвоночника, боль в ягодицах.
Около 15-30 процентов. у пациентов развивается хронический артрит или рецидивирующий артрит сакроусилика и / или позвоночника.
Реактивный артрит — диагностика
Проводится анализ крови, мочи, фекалий, осмотра синовиальной жидкости и синовиальной мембраны, визуализации (рентгеновских суставов) и определения антигена HLA-B27.
Реактивный артрит — лечение
Пациенты должны ограничивать свою физическую активность (это относится, в частности, к занятым суставам). Рекомендуется реабилитация. Также полезны физиотерапия и кинезотерапия.
Пациентка лечится нестероидными противовоспалительными препаратами (чтобы свести к минимуму боль). В более тяжелых случаях врач может заказать глюкокортикостероиды (но только на короткое время). Если симптомы сохраняются более 3 месяцев или неэффективны нестероидные противовоспалительные препараты, рекомендуется добавлять противоревматические препараты, модифицирующие болезнь (DMARDs), например сульфасалазин, метотрексат, азатиоприн. Антибиотикотерапия показана только в случае активной инфекции и в основном затрагивает инфекцию хламидий.
Поражения кожи можно лечить локально глюкокортикостероидами и кератолитическими средствами (они смягчают утолщенный роговой слой). Изменения в слизистой оболочке полости рта спонтанно исчезают и не требуют лечения.
В случае воспалительных изменений глаза лечение должно проводиться офтальмологом.
Источник
