Остеопороз от рака кожи
Риск заболевания раком груди увеличивается с возрастом; то же самое касается и остеопороза. Лечение, которое применяется при раке груди, может стать причиной развития остеопороза. Узнайте больше о том, как те, что вылечились от рака груди, могут бороться с остеопорозом.
Воздействие рака груди
Национальный Институт Рака утверждает, что каждая восьмая женщина в Соединённых Штатах (около 13 %) болеет раком груди на протяжении жизни. На самом деле, после рака кожи, рак груди является наиболее распространённым видом рака среди американок.
Так как точная причина возникновения рака груди неизвестна, риск заболевания увеличивается с возрастом. Особенно подвержены высокому риску женщины после 60 лет. Вследствие их возраста, эти женщины уже подвержены риску заболевания остеопорозом. Вследствие увеличения частоты заболевания раком груди и улучшения длительности выживаемости, здоровье костей и предотвращение переломов становится важным аспектом для тех, кто выжил после рака груди.
Что такое остеопороз?
При остеопорозе кости теряют плотность и более подвержены переломам. Переломы, вследствие заболевания остеопорозом, могут привести к сильным болям и инвалидности. Остеопороз угрожает здоровью, как показали исследования, 44 миллионам американцев, 68 % которых являются женщинами:
Факторы риска развития остеопороза включают:
худощавость или небольшие размеры
наличие болезни в семейном анамнезе
постклимактерический период или наступление преждевременной менопаузы у женщин или отсутствие месячных (аменорея)
приём определённых медикаментов, например, глюкокортикоидов
дефицит кальция
недостаточность физической активности
курение и
злоупотребление алкоголем.
Остеопороз является бессимптомным заболеванием, которое часто можно предотвратить. Но если его не выявить, он может прогрессировать на протяжении многих лет без проявления симптомов, до того момента, пока не случится перелом. Его называют «детской болезнью, которая имеет последствия в старости» из-за того, что процесс костеобразования в молодости является важным для предотвращения остеопороза и переломов позже.
Связь между раком груди и остеопорозом
Женщины, прошедшие курс лечения от рака груди, могут быть подвержены повышенному риску заболевания остеопорозом и предрасположенности к переломам вследствие нескольких причин. Во-первых, эстроген оказывает защитное воздействие на кость, и снижение уровня содержания гормона способствует потере косной массы. Вследствие химиотерапии или операции, многие выжившие после рака груди теряют функцию яичников, и, соответственно, уровень эстрогена снижается. Женщины, у которых предклимактерический период начался до прохождения курса лечения от рака, склонны к наступлению менопаузы ранее, чем те, которые не заболели раком.
Исследования также предполагают, что химиотерапия может непосредственно негативно воздействовать на кости. Кроме того, сам по себе рак груди может стимулировать выработку остеокластов, клеток, которые разрушают кость.
Стратегии управления
Придерживание некоторых стратегий может снизить риск подверженности остеопорозу или снизить воздействие болезни, уже диагностированной у женщины.
Питание: Некоторые исследования обнаружили связь между раком груди и придерживанием диеты. Однако ещё не совсем понятно, какие продукты питания или пищевые добавки играют роль в сокращении заболеваемости раком груди. Относительно здоровья костей, необходимо придерживаться хорошо сбалансированной и обогащенной кальцием и витамином D диеты. Источники кальция включают молочные продукты с низким содержанием жира; тёмно-зелёные листовые овощи; обогащенные кальцием продукты питания и напитки. Также, для восполнения требуемой ежедневной нормы кальция можно принимать пищевые добавки Институт Медицины рекомендует ежедневно употреблять 1000 миллиграмм кальция мужчинам и женщинам в возрасте от 19 до 59 лет, и увеличить дозу до 1200 мг после 50 лет.
Витамин D играет важную роль в усвоении кальция и для здоровья костей. Он синтезируется кожей под воздействием солнечного света. Некоторым людям необходимы пищевые добавки с содержанием витамина D, для восполнения рекомендуемой ежедневной дозы, которая состоит из 400 — 800 МЕ (Международных единиц).
Физическая активность: Как и мышцы, кости состоят их живой ткани, которая реагирует на физические нагрузки, укрепляясь. Весовые нагрузки, при которых вы преодолеваете силу притяжения, являются наилучшим способом тренировки костной ткани. Некоторые примеры: ходьба, подъём по лестнице, танцы и подъём тяжестей. Регулярные физические нагрузки, например ходьба, помогут предотвратить потерю костной массы и обеспечат многими другими преимуществами здоровья. Недавние исследования показали, что физические упражнения могут сократить риск заболевания раком груди у молодых женщин.
Здоровый образ жизни: Курение плохо влияет на кости, также как и на сердце и лёгкие. Кроме того, курящие люди абсорбируют меньше кальция. Некоторые исследования показывают немного повышенный риск заболевания раком груди среди женщин, употребляющих алкоголь, и существуют доказательства, что алкоголь может негативно отразиться на состоянии здоровья костей. Люди, которые злоупотребляют алкоголем, более предрасположены потере костной массы и переломам из-за недостаточного питания, а также из-за повышенного риска падения.
Источник
Под словосочетанием «рак костей» понимают злокачественные опухоли костной ткани. На самом деле это не совсем правильный термин. Строго говоря, слово «рак» применимо лишь к опухолям, которые происходят из эпителиальных тканей — кожи и слизистых оболочек. Костная ткань — это одна из разновидностей соединительной ткани. Развивающиеся из нее злокачественные опухоли называются саркомами.
Выбор тактики лечения и прогноз определяются типом рака кости, который диагностирован у пациента, и некоторыми другими факторами.
Разновидности рака костей
Метастатический рак — наиболее распространенные злокачественные опухоли костей. Костные метастазы встречаются при разных онкологических заболеваниях, в частности, при раке молочной железы, простаты, легких, желудка. Такие опухоли обозначают по названию органа, в котором находится первичный очаг, например, «рак молочной железы с метастазами». Под микроскопом опухолевые клетки имеют внешний вид, характерный для первичного очага. Лечение костных метастазов проводится препаратами, на которые реагирует первичная опухоль.
Остеосаркома — наиболее распространенная разновидность первичного рака костей. Чаще всего встречается в возрасте 10-30 лет, как правило, возникает в костях рук и ног, таза. Мужчины болеют чаще по сравнению с женщинами. Менее 10% случаев остеосаркомы приходится на людей старше 60 лет.
Хондросаркомы происходят из хрящевой ткани, это второй по распространенности тип первичного рака костей. Молодые люди до 20 лет болеют очень редко. С 20 до 75 лет риск возникновения хондросаркомы постепенно нарастает, мужчины и женщины болеют примерно одинаково часто. Хондросаркомы могут возникать в костях рук и ног, таза, черепа, в лопатке. Они могут начать расти и во внутренних органах, в которых присутствует хрящевая ткань, например, в гортани, трахее.
Саркома Юинга — третий по распространенности тип рака костей. Поражает детей, подростков, молодых людей. После 30 лет заболевание встречается крайне редко. Чаще всего опухоль локализуется в костях таза, нижних и верхних конечностях, лопатках, ребрах.
Злокачественная фиброзная гистиоцитома обычно локализуется в мягких тканях, в редких случаях — в костях. Заболевание преимущественно встречается в среднем и пожилом возрасте. При костной локализации чаще всего поражаются кости ног в области колена. Злокачественная фиброзная гистиоцитома склонна к локальному росту, но иногда может давать метастазы, например, в легких.
Фибросаркома также чаще встречается в мягких тканях. У людей среднего и пожилого возраста может поражать кости рук, ног.
Хордома — опухоль, которая чаще всего находится в основании черепа или позвоночном столбе. Обычно диагностируется после 30 лет, у мужчин примерно вдвое чаще, чем у женщин. Хондромы склонны к медленному локальному росту, в редких случаях дают метастазы в лимфатические узлы, печень.
Лечение рака костей
Лечением пациента со злокачественной опухолью костной ткани занимается команда врачей, в которую могут входить: онколог, хирург, специализирующийся в сфере ортопедии, химиотерапевт, врач лучевой терапии, ортопед, реабилитолог, психоонколог.
Хирургическое лечение рака костной ткани
Хирургия — основной радикальный метод лечения рака костей. В прошлом у большинства пациентов прибегали к ампутации — удалению всей конечности или ее части, пораженной опухолью. В настоящее время хирурги стараются отдавать предпочтение органосохраняющим вмешательствам. Удаленную часть кости заменяют костным трансплантатом или эндопротезом из металла, других материалов. Если приходится удалять фрагмент бедренной или плечевой кости, нижележащую часть конечности можно сохранить. При этом рука или нога станет короче, но сможет ограниченно выполнять свои функции.
Иногда в качестве альтернативы хирургическому вмешательству применяют криодеструкцию (разрушение опухолевой ткани низкой температурой), кюретаж (выскабливание специальным инструментом), введение в отверстие в кости цемента из полиметилметакрилата (при затвердевании он нагревается и разрушает опухолевые клетки).
Лучевая терапия при раке костей
Для того чтобы уничтожить опухолевые клетки в кости, требуются высокие дозы излучения, которые приводят к серьезным побочным эффектам. Поэтому лучевая терапия при раке костей находит ограниченное применение:
- Если опухоль невозможно полностью удалить хирургически.
- При положительном крае резекции по данным биопсии после операции.
- В качестве паллиативного метода лечения при рецидиве, чтобы уменьшить боль и отек.
Наиболее широкое применение лучевая терапия находит при саркомах Юинга.
Химиотерапия при раке костей
Химиотерапию чаще всего применяют для лечения остеосарком и сарком Юинга. Другие виды рака костей реагируют на нее плохо. Применяют различные химиопрепараты: цисплатин, доксорубицин, ифосфамид, этопозид, метотрексат, циклофосфамид, винкристин.
Иногда применяют таргетные препараты — лекарственные вещества, которые блокируют молекулы, необходимые для роста и выживания злокачественных опухолей.
Лечение при метастазах рака в костях
При лечении метастазов в костной ткани используют химиопрепараты, которые эффективны против первичной опухоли. Применяют лучевую терапию. Если метастатические очаги приводят к значительному разрушению костной ткани, назначают бисфосфонаты. Эти препараты вводят внутривенно каждые 3-4 недели, они помогают предотвратить патологические переломы, уменьшить боль, снизить уровень кальция в крови.

Хирургическое лечение носит паллиативный характер. При патологических переломах кости укрепляют с помощью винтов, стержней и других металлических конструкций. Иногда прибегают к радиочастотной аблации: в опухоль вводят иглу и подают на нее ток высокой частоты, который разрушает опухолевые клетки.
Реабилитация после лечения рака костей
После ампутации конечности показано протезирование. При правильно спланированных реабилитационных мероприятиях пациенты, перенесшие ампутацию нижней конечности, обычно могут снова ходить спустя 3-6 месяцев.
После органосохраняющих операций реабилитационный период продолжается дольше. Способность ходить восстанавливается примерно через год. Если не проводить реабилитационное лечение, возникает стойкая утрата функции конечности. При инфицировании, смещении или разрушении эндопротеза требуется повторное хирургическое вмешательство. Некоторым пациентам в последующем приходится выполнять ампутацию.
После наступления ремиссии и завершения лечения пациент должен находиться под наблюдением врача. При возникновении любых симптомов нужно посетить клинику и пройти обследование. Это помогает вовремя диагностировать рецидив рака в кости, метастазов в других органах.
Прогноз выживаемости
На прогноз влияют такие факторы, как тип и стадия рака кости, локализация и размер опухоли, возраст пациента. В среднем пятилетняя выживаемость (процент пациентов, которые остаются живы в течение 5 лет с момента диагностики заболевания) при всех типах злокачественных опухолей костей составляет 70%.
Стадии рака костей
Выделяют 4 стадии развития опухолей кости:
- 1 стадия: опухоль ограничена костью, не прорастает в соседние ткани, не распространяется в лимфатические узлы, отдаленные метастазы отсутствуют. Опухоль является высокодифференцированной и отличается низкой степенью агрессивности.
- 2 стадия: опухоль также ограничена костью, не прорастает в соседние ткани, но является низкодифференцированной (опухолевая ткань практически утратила черты нормальной ткани) и более агрессивной.
- 3 стадия: в кости имеется 2-3 очага, они могут быть высоко- или низкодифференцированными.
- 4 стадия: опухоль, которая распространилась за пределы кости в другие органы и ткани.
Причины и факторы риска рака костей
Точные причины возникновения злокачественных опухолей костей неизвестны. Некоторые факторы риска повышают вероятность развития заболевания:
- Остеосаркомы чаще диагностируют у людей, которые перенесли курс лучевой терапии и/или химиотерапии по поводу других типов рака.
- Риски остеосаркомы повышает применение металлических фиксирующих устройств (скоб, спиц, пластин, винтов) при переломах костей.
- Играют роль некоторые наследственные заболевания: наследственная ретинобластома (редкая злокачественная опухоль глаза), синдром Ли-Фраумени.
- У пожилых людей возникновению рака костей может предшествовать Болезнь Педжета — заболевание, при котором нарушается процесс естественного обновления костной ткани, и кости становятся хрупкими.
Симптомы злокачественных опухолей костей
Зачастую первым проявлением рака костей становится боль. Поначалу она возникает лишь во время сна и физических нагрузок, затем становится постоянной, мучительной. Если пораженный участок кости не прикрыт массивными мышцами и находится близко к коже, опухоль можно увидеть при визуальном осмотре, прощупать. Возникает отек.
Рак разрушает нормальную костную ткань, ослабляет кости, в итоге происходят патологические переломы от небольшого усилия. Во время перелома в кости возникает сильная острая боль. Если опухоль сдавливает нерв, в пораженной части тела появляется онемение, покалывание, слабость мышц (парезы, вплоть до паралича).
Похожие симптомы могут возникать и при других заболеваниях, например, при артритах, остеомиелите, после перенесенных травм. Рак костей встречается редко, но при возникновении болей в костях без видимой причины лучше сразу посетить врача и провериться.
Методы диагностики
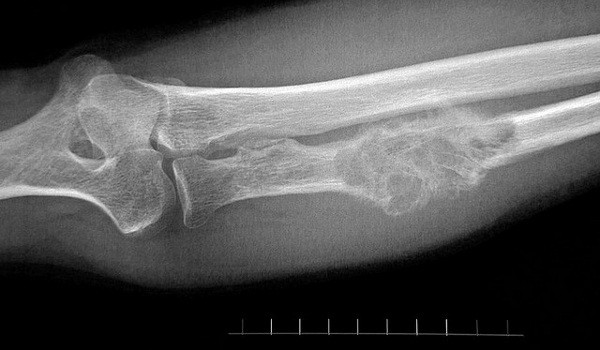
Обычно пациенту, который обратился в клинику с жалобой на боли в костях, в первую очередь назначают рентгенографию. Это самый быстрый и доступный метод диагностики, он позволяет быстро оценить состояние костной ткани и обнаружить патологическое образование. Пораженная кость выглядит на снимках «изъеденной», либо в ней обнаруживается дефект, «дыра». Можно увидеть, как опухоль распространяется в соседние ткани. По некоторым признакам на рентгенограммах можно с высокой степенью вероятности предположить наличие злокачественной опухоли, но установить точный диагноз позволяет только биопсия.
Компьютерная томография помогает уточнить размеры, расположение, количество опухолевых очагов, степень прорастания в окружающие ткани, обнаружить метастазы в лимфатических узлах и внутренних органах. По показаниям назначают МРТ: она помогает лучше визуализировать опухоль, оценить состояние мягких тканей, головного и спинного мозга.

В поиске мелких метастазов помогает позитронно-эмиссионная томография. Во время исследования в организм вводят молекулы сахара с радиоактивной меткой. Опухолевые клетки поглощают радиофармпрепарат и становятся видимыми на снимках, выполненных специальным аппаратом.
Наиболее точный метод диагностики онкологических заболеваний — биопсия. Во время исследования получают фрагмент предположительно опухолевой ткани и отправляют в лабораторию для изучения внешнего вида клеток, строения ткани, молекулярно-генетических характеристик. Биопсию можно провести разными способами:
- При тонкоигольной биопсии используют шприц с иглой. Если кость находится глубоко, скрыта мышцами, процедуру проводят под контролем компьютерной томографии.
- При трепан-биопсии используют толстую иглу диаметром примерно полтора миллиметра. Считается, что этот метод лучше, чем тонкоигольная биопсия, он позволяет установить более точный диагноз.
- Иногда для исследования нужен большой фрагмент кости. В таких случаях проводят эксцизионную или инцизионную биопсию: выполняют хирургическое вмешательство, удаляют всю опухоль или ее часть.
Источник
Рак молочной железы (РМЖ) — самая частая злокачественная опухоль у женщин в экономически развитых странах. Число новых случаев заболевания в мире превышает 1 млн в год. На протяжении жизни одна из 7 женщин в США, а в России одна из 12 женщин заболевает РМЖ [1]. РМЖ занимает 1-е место в структуре заболеваемости злокачественными новообразованиями среди женщин в России и составляет 20,9% [2]. В Ханты-Мансийском автономном округе (ХМАО), расположенном на севере Тюменской области, заболеваемость РМЖ выше, чем в среднем по России, и составляет 26,5% [3].
Основными методами лечения РМЖ являются хирургический, лучевой, лекарственный и их комбинации. В процессе лечения у больных РМЖ появляется болевой синдром в костях, в позвоночнике, крупных и мелких суставах, который беспокоит на протяжении длительного времени [4, 5].
Современные методы диагностики и лечения позволили существенно улучшить выживаемость больных РМЖ. В отдельных прогностически благоприятных группах больных ранним РМЖ 5-летняя безрецидивная выживаемость достигает 98%. Увеличились также сроки жизни больных с диссеминированным процессом, наиболее ощутимо при гормонозависимых опухолях. Все это делает актуальным поддержание здоровья костной системы, ведь нормальное функционирование опорно-двигательного аппарата является неотъемлемой составной частью хорошего качества жизни [1].
Патогенез развития болевого синдрома у больных РМЖ чаще всего обусловлен явлениями остеопороза. Причиной развития метаболических нарушений костной структуры при остеопорозе является как влияние самой болезни, так и результат воздействия большого количества факторов, в том числе химиотерапии, гормонотерапии и хирургической кастрации, которые являются основными методами лечения РМЖ [6, 7].
На сегодняшний день потеря костной ткани в результате противоопухолевого лечения РМЖ является актуальной проблемой. Противоопухолевая терапия (эндокринная терапия, химиотерапевтическое лечение и хирургическая кастрация) приводит к снижению уровня половых гормонов — эстрогенов [8]. Несмотря на то, что адекватная терапия остеопороза способна снизить частоту последующих осложнений на 40-60%, диагностика проводится менее чем у 25% женщин, а соответствующую терапию получает еще меньшее количество пациенток [5]. Остеопороз является серьезным нежелательным явлением, отрицательно влияющим на качество жизни онкологических больных в первую очередь за счет болевого синдрома, который носит постоянный характер [9, 10].
Цель исследования — установить взаимосвязь остеопороза и развития болевого синдрома у больных РМЖ на фоне проведенного лечения и повысить эффективность диагностики и профилактики остеопороза.
В исследование включили 77 женщин, из них 47 больных РМЖ в возрасте от 30 до 50 лет и 30 здоровых женщин аналогичного возраста — группа сравнения. В соответствии со ст. 30-34, 61 «Основ законодательства РФ об охране здоровья граждан» от 22.07.1993 № 5487−1, ст. 18, 20-22, 28, 41 Конституции Р.Ф. все обследуемые лица давали информированное добровольное согласие на выполнение диагностических исследований и в соответствии с требованиями ст. 9 закона РФ от 27.07.2006 «О персональных данных» № 152-ФЗ — на обработку персональных данных. Критериями включения в обследование были больные РМЖ с гистологически верифицированным диагнозом в фертильном возрасте и наличием менструации. Всем пациенткам была проведена остеосцинтиграфия для исключения метастазов в костях. Критериями исключения из обследования явились: первично-множественные опухоли, наличие переломов в анамнезе и метастазов в костях, длительный прием глюкокортикоидов (более 3 мес).
В нашем исследовании в 70,2% случаев выявлен РМЖ I-II стадии (табл. 1). В РФ за 2013 г. — 66,7%, в ХМАО — 69,3% за 2014 г. [3].
Таблица 1. Распределение больных РМЖ в зависимости от стадии
Лечение больных РМЖ зависело как от стадии, так и от гистологической и иммуногистохимической характеристики и степени злокачественности опухоли. Всем 47 пациенткам проведено оперативное лечение, из них 7 (14,9%) — радикальная резекция молочной железы. У 18 (38,3%) пациенток провели неоадъювантную полихимиотерапию (НАПХТ) в связи с распространенностью процесса и с целью проведения органосохраняющей операции, 38 (80,8%) больных получили адъювантную ПХТ, 12 (25,5%) — лучевую терапию. Гормонотерапия назначена в 36 (76,6%) случаях РМЖ.
Всем больным РМЖ и группы сравнения была проведена остеоденситометрия методом DXA на денситометре EXPLORER (производство «Hologic», США, 2007 г.) и определены биохимические маркеры остеопороза. Обследование проводили до назначения лечения и через 6 мес после лечения. Оценку болевого синдрома проводили с помощью Мак-Гилловского болевого опросника [11] и по данным классификации болевого синдрома. Болевой синдром при остеопорозе характеризуется снижением работоспособности, повышенной утомляемостью, болью в спине или после физической нагрузки, ощущением тяжести между лопатками, необходимостью отдыха в положении лежа. Появляется летучая боль в костях и суставах, непостоянная, усиливающаяся при смене погоды, минимальная утренняя скованность не более 30 мин, уменьшение объема движений. По данным симптомам и результатам Мак-Гилловского болевого опросника нами разработана классификация степени выраженности болевого синдрома.
Достоверность различий изучаемых параметров анализировали с применением критерия χ2 Пирсона с коррекцией на непрерывность по Йетсу, для непараметрических величин, в динамике наблюдения — по критерию Вилкоксона: за достоверные принимали различия при значениях р < 0,05. Полученный цифровой материал обрабатывали с использованием программы MS Exсel и istica 8.0. Средние величины представлены в виде М±m.
В контрольной группе женщин фертильного возраста (от 30 до 50 лет) остеопению (начальные изменения костной ткани) наблюдали в 3 (10%) случаях. Остеопороза в группе сравнения не было. Клинические проявления в виде болевого синдрома 1-й степени у здоровых женщин наблюдали в 6 (20%) случаях.
Среди 47 больных РМЖ фертильного возраста болевой синдром до лечения основного заболевания выявили в 6 (12,7%) случаях. Через 6 мес после лечения РМЖ болевой синдром был выявлен в 36 (76,6%) случаях: в 18 — 1-я степень, в 16 — 2-я степень и в 2 случаях — 3-я степень (рис. 1).
Рис. 1. Проявление болевого синдрома на фоне лечения РМЖ (абсолютное число и %).
Получена статистическая достоверная разница появления и усиления болевого синдрома до лечения по поводу РМЖ и через 6 мес после проведенного лечения (р<0,01).
Больным РМЖ была проведена остеоденситометрия: 1-я группа — нормальные значения Т-критерия, 2-я группа — остеопения (отклонение Т-критерия по остеоденситометрии от -1,1 до -2,5 ББ) и 3-я группа — остеопороз (показатели остеоденситометрии менее -2,5 ББ Т-критерия).
У больных РМЖ до лечения признаки остеопении и остеопороза наблюдали в 11 (23,4%) случаях, из них у 1 — остеопороз, а через 6 мес после проведенного лечения — в 30 (63,8%) случаях, из них у 2 — остеопороз (рис. 2).
Рис. 2. Проявление остеопении и остеопороза на фоне специального лечения РМЖ (абсолютное число и %).
Среднее значение абсолютных показателей минеральной плотности кости (МПК) до лечения составило -0,01±1,23 г/см2, а через 6 мес после проведенного лечения средний показатель МПК составил -0,85±1,24 г/см2. Получены статистически значимые результаты появления остеопороза и остеопении после проведенного лечения по поводу РМЖ (р<0,001).
На фоне проведенного специального лечения уже через 6 мес у больных РМЖ фертильного возраста достоверно увеличивается количество случаев развития остеопороза и остеопении на фоне проявления и (или) усиления болевого синдрома (рис. 3). Прямая корреляционная зависимость болевого синдрома от степени остеопороза и остеопении до и после проведения специального лечения подтверждена статистически (р<0,01).
Рис. 3. Соотношение остеопороза и остеопении с болевым синдромом у больных РМЖ на фоне проведенного специального лечения (в %).
Помимо оценки факторов остеопороза и МПК в диагностике остеопороза нашло применение определение биохимических маркеров костного метаболизма, которые делятся на показатели костеобразования и резорбции костной ткани, а также предикторов нарушений костного гомеостаза [12]. Из маркеров формирования костной ткани у больных РМЖ определяли остеокальцин, щелочную фосфатазу, кальцитонин; из маркеров резорбции костной ткани — С-концевые телопептиды; а из маркеров состояния обмена — паратиреоидный гормон (ПТГ), тиреотропный гормон (ТТГ), кальций и фосфор. Использование данных биохимических тестов у больных РМЖ позволяет проводить более полную диагностику остеопороза (табл. 2).
Таблица 2. Лабораторные показатели на фоне лечения РМЖ
Нами не было выявлено достоверных различий в лабораторных показателях крови у больных с остеопорозом и остеопенией до и после специального лечения по поводу РМЖ (p>0,05). Однако маркеры остеопороза помогают исключить заболевания, сходные с остеопорозом, сопровождающиеся диффузным разрежением костной структуры: остеомаляцию, гиперпаратиреоз, почечную остеопатию, плазмоцитому, метастазы в скелете (диагностика исключения) и т. д. Таким образом, с помощью маркеров костного обмена можно установить причину вторичного остеопороза. Согласно данным литературы, лабораторные показатели костной ткани в большинстве случаев используются для оценки эффективности лечения [13].
Согласно современным рекомендациям, у всех больных, начинающих или уже получающих терапию ингибиторами ароматазы, необходимо исходно измерять МПК и оценить другие факторы риска переломов. Пациентки с исходным значением МПК по Т-шкале ниже -2,0 или наличием, по крайней мере, двух факторов повышенного риска переломов, независимо от показателя МПК нуждаются в немедленном начале терапии бисфосфонатами (в сочетании с витамином D и препаратами кальция). При исходном значении МПК по Т-шкале -2,0 и выше и отсутствии факторов риска следует рекомендовать прием витамина D и препаратов кальция. При этом каждый год нужно оценивать состояние костной системы и появление каких-либо факторов риска. При ежегодном снижении МПК на 5% и более необходимо исключить дополнительные причины развития остеопороза и начать терапию бисфосфонатами [14].
1. Остеопороз и остеопения у больных РМЖ фертильного возраста после комплексного лечения выявляется в 63,8% случаев, а болевой синдром — в 76,6% случаев, что подтверждено статистически (р<0,01). Имеется прямая корреляционная зависимость появления и усиления болевого синдрома от степени остеопороза и остеопении до и после проведения специального лечения (р<0,01).
2. Остеопороз чаще наблюдается у пациенток, которым проведено комплексное лечение с блокировкой функции яичников, т. е. наступлением искусственной менопаузы (р<0,01). Этим пациенткам рекомендовано проведение остеоденситометрии для своевременной диагностики остеопороза и назначения соответствующего лечения.
3. Лабораторные маркеры остеопороза не могут быть использованы в качестве диагностических критериев для оценки остеопороза. Они используются для оценки эффективности лечения.
Участие авторов
Концепция и дизайн исследования: Н.Ю.Т., Е.В.К.
Сбор и обработка материала: Н.Ю.Т.
Статистическая обработка данных: Н.Ю.Т.
Написание текста: Н.Ю.Т., Е.В.К.
Редактирование: Е.В.К.
Конфликт интересов отсутствует.
Источник
