Патогенез и принципы лечения подагры

Подагра – ревматическая патология, вызванная отложением кристаллов солей мочевой кислоты – уратов в суставах, затем в почках. Клиника подагры характеризуется рецидивирующими и прогрессирующими приступами артрита с интенсивными болями и формированием тофусов – подагрических узелков, приводящих к деформации суставов. В дальнейшем поражаются почки, может развиться мочекаменная болезнь и почечная недостаточность. Для диагностики подагры производят исследование синовиальной жидкости на наличие уратов, рентгенисследование пораженных суставов. Лечение подагры направлено на купирование воспаления (НПВС, глюкокортикоиды), снижение уровня мочевой кислоты в крови, нормализацию питания.
Общие сведения
В основе патогенеза подагры лежат метаболические расстройства, вызванные нарушением регуляции обмена пуринов в организме и ведущие к накоплению мочевой кислоты и ее производных — кислых уратных солей. Увеличенная концентрация мочевой кислоты (гиперурикемия) в плазме крови и отложение уратов является следствием их повышенного синтеза и уменьшения выделения с мочой. Уратные микрокристаллы накапливаются в суставных полостях с развитием подагрического воспаления, а также в почках, вызывая подагрическую нефропатию. Подагра обычно поражает пациентов после 40 лет, при этом у мужчин она выявляется в 20 раз чаще, чем у женщин.
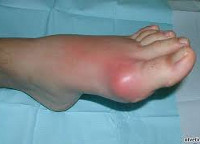
Подагра
Классификация подагры
В клинике подагры различаются почечная, метаболическая и смешанная формы. Почечная форма подагры характеризуется снижением экскреции мочевой кислоты, метаболическая – излишками ее образования; смешанная форма сочетает умеренные нарушения синтеза и удаления из организма мочевой кислоты.
В зависимости от причин, ведущих к развитию заболевания, подагра может быть первичной либо вторичной. Первичная подагра нередко бывает обусловлена генетическими дефектами и гипофункцией ферментов, участвующих в обмене пуринов и выведении мочевых солей. К факторам развития подагры относится избыточный и однообразный характер питания, повышенное потребление мясной пищи и алкоголя, малоактивный образ жизни. Вторичная подагра является следствием других заболеваний — патологии почек с нарушением их функций, заболеваний крови (лейкозов, лимфомы, полицитемии), псориаза, лекарственной терапии цитостатиками, салуретиками и др. препаратами.
Клиническая классификация выделяет семь форм течения подагры: типичный (классический) приступ острого подагрического артрита, полиартрит по инфекционно-аллергическому типу, подострый, ревматоидоподобный, псевдофлегмонозный, периартритический и малосимптомный варианты.
Симптомы подагры
В клинике подагры различают 3 фазы: преморбидную, интермиттирующую и хроническую.
Преморбидная фаза характеризуется бессимптомной урикемией и еще не является подагрой. На лабораторном уровне гиперурикемия выявляется у 8-14% взрослых. Интермиттирующая фаза подагры характеризуется эпизодами приступов острого артрита, чередующимися с бессимптомными периодами. К проявлениям хронической формы подагры относится образование подагрических узелков (тофусов), хроническое течение подагрического артрита, внесуставные проявления в виде поражения почек (в 50-70% клинических случаев).
Классический приступ острого подагрического артрита развивается у 50-80% пациентов. Типично внезапное начало, чаще в ночные часы. Первичный приступ подагры нередко бывает спровоцирован алкоголем, жирной пищей, травмой, переохлаждением. Приступ подагры характеризуется резчайшими болями в области плюснефалангового сустава 1-го пальца стопы, фебрильным синдромом, опуханием сустава, блеском и гиперемией кожи над ним, нарушением функции сустава. Через 3-10 суток приступ подагры стихает с исчезновением всех признаков и нормализацией функций. Повторная подагрическая атака может развиться спустя несколько месяцев и даже лет, однако с каждым разом промежутки между приступами укорачиваются. У мужчин первичный приступ подагры чаще протекает по типу моноартрита с поражением суставов стопы, у женщин – олиго- и полиартрита с вовлечением суставов кисти.
Полиартрит по инфекционно-аллергическому типу при подагре развивается у 5% пациентов. Такая форма течения подагры характеризуется мигрирующими болями во множественных суставах, быстрым регрессом признаков воспаления, как и в случае клиники инфекционно-аллергического полиартрита. Для подострого варианта течения подагры характерны типичная локализация боли в первом плюснефаланговом суставе и умеренно выраженные признаки поражения. При подострой подагре у молодых пациентов возможно развитие моно- или олигоартрита средних и крупных суставов.
Ревматоидноподобная форма подагры отличается первичной заинтересованностью суставов рук в виде моно- или олигоартрита. При псевдофлегмонозном типе подагры наблюдаются моноартриты различной локализации с воспалением сустава и парасуставных тканей, лихорадка. По клинике данный вариант напоминает течение флегмоны либо острого артрита. Малосимптомный вариант течения подагры характеризуется слабо выраженной, стертой симптоматикой – небольшой болью, слабой гиперемией кожи в зоне поражения.
Для периартритической формы подагры свойственно поражение бурс и сухожилий (чаще пяточных) при сохранных суставах. В дальнейшем присоединяются явления хронического подагрического полиартрита с поражением суставов ног, их дефигурацией и скованностью; деформации суставных тканей, костные разрастания; контрактуры, хруст в коленных и голеностопных суставах, неполные вывихи пальцев. На этом фоне продолжаются атаки подагры с возможным развитием подагрического статуса – не стихающего обострения артрита с хроническим воспалением парасуставных тканей за счет их инфильтрации солями. В результате тяжелых приступов подагры пациенты теряют трудоспособность и двигательную активность.
При длительном анамнезе подагры (дольше 5-6 лет) и гиперурикемии высокой степени появляются специфические признаки — тофусы или подагрические узелки, представляющие собой скопление кристаллов уратов в мягких тканей. Излюбленными участками локализации тофусов служат ушные раковины, подкожная клетчатка предплечий, локтей, пальцев рук, стоп, голеней, бедер. Во время приступов подагры тофусы могут вскрываться с выходом наружу беловатого отделяемого.
Осложнения подагры
Диагностика подагры
Пациентам с подозрением на подагру рекомендована консультация ревматолога и уролога. Общий анализ крови вне подагрической атаки не изменен; в период приступа отмечается нейтрофильный сдвиг лейкоцитарной формулы влево, нарастание СОЭ. Биохимическое исследование крови при обострении подагры выявляет увеличение мочевой кислоты, фибрина, серомукоида, сиаловых кислот, гаптоглобина, γ- и α2- глобулинов.
По рентгенографии суставов характерные изменения выявляются при хроническом подагрическом полиартрите. Рентгенологическая картина обнаруживает наличие остеопороза, на фоне которого определяются очаги просветления в области эпифизов и суставов размером до 2-3 см; при глубокой запущенности процесса — разрушение костных эпифизов с их замещением скоплением уратных масс. Специфические признаки подагры на рентгенограммах определяются по истечении 5 лет от манифестации заболевания.
Для взятия суставной жидкости проводят пункцию сустава. Микроскопический анализ синовиальной жидкости при подагре показывает наличие в ней микрокристаллов урата натрия. При исследовании материала, полученного при биопсии тофусов, обнаруживаются кристаллы мочевой кислоты. Во время УЗИ почек определяются уратные конкременты.
Диагностическими маркерами подагры являются:
- микрокристаллические ураты в синовиальной жидкости;
- лабораторно подтвержденные тофусы с отложением кристаллических уратов;
- наличие не менее шести из перечисленных далее признаков: присутствие в анамнезе более одной острой атаки артрита; максимальные признаки воспаления сустава в острой фазе; покраснение кожи над воспаленным суставом; моноартикулярный тип поражения; боль и припухлость I плюсне-фалангового сустава с одной стороны; односторонний характер поражения свода стопы; тофусоподобные узелки; асимметричная припухлость сустава; гиперурикемия; рентгенологически определяемые субкортикальные кисты без эрозии; отсутствие роста микрофлоры при бакпосеве суставной жидкости.
Лечение подагры
Основным принципом терапии подагры является контроль содержания мочевой кислоты путем подавления ее продукции и ускорения выведения из организма. Назначается диета, исключающая потребление рыбных и мясных бульонов, мяса животных, почек, печени, легких, алкоголя. В рационе питания вводится ограничение на бобовые и овощные культуры (фасоль, горох, бобы, шпинат, щавель, редис, баклажаны, спаржу, цветную капусту), грибы, икру, некоторые виды рыбы (сардины, балтийскую сельдь и др.). При подагре потребность в калориях удовлетворяется за счет углеводистой пищи, поэтому пациентам следует контролировать свой вес. В умеренных количествах разрешается употреблять в пищу яйца, крупы, нежирную рыбу, баранину, говядину. При подагре требуется ограничение солевой нагрузки и прием достаточного объема жидкости (до 3-х литров в сутки).
Медикаментозный подход к терапии подагры направлен на купирование острых подагрических атак, их предотвращение в дальнейшем, предупреждение отложения уратов в суставах и почках. Для купирования приступов подагры используются НПВП (индометацин), растительные алкалоиды (колхицин), местные мази и гели. В качестве антирецидивной терапии при подагре назначается колхицин в малых дозах или антигиперурикемические препараты. Целью лечения подагры является понижение концентрации мочевой кислоты в крови в 2 раза ниже нормы, требуемое для растворения уратных кристаллов. Для активизации выведения мочевой кислоты производится назначение урикозурических препаратов — пробенецида, сульфинпиразона, азапропазона, бензбромарона. К средствам, ингибирующим продукцию мочевой кислоты, относятся аллопуринол.
При атипичной форме подагры, протекающей со скоплением внутрисуставного выпота, производится его пункционная эвакуация. Проведение сеансов экстракорпоральной гемокоррекции направлено на снижение концентрации мочевой кислоты и уратных солей, подавление воспаления и снижение дозировки принимаемых препаратов. Физиотерапевтическое и курортное лечение при подагре проводится в ремиссионной стадии. Проведение УФО области заинтересованного сустава в острую фазу в ряде случаев помогает прекратить начавшийся приступ подагры.
Прогноз и профилактика подагры
Своевременное распознавание и начало рационального лечения дает прогностически благоприятные результаты. Факторами, усугубляющими прогноз подагры, являются молодой (до 30 лет) возраст, сочетание мочекаменной болезни и инфекций мочевыделительного тракта, отягощенный соматический анамнез (сахарный диабет, артериальная гипертензия), прогрессирование нефропатии.
Необходимость профилактики подагры следует учитывать при проведении химиотерапии, а также у пациентов с угрозой распада и некроза опухоли. С первого дня курса химиотерапевтического лечения необходимо назначение гипоурикемических препаратов (аллопуринола). Профилактика новых обострений подагры зависит от соблюдения водно-солевого режима, диеты, контроля массы тела. При наличии родственников, страдающих подагрой, другим членам семьи рекомендуется следить за уровнем мочевой кислоты.
Источник
Подагра (болезнь королей, пиратская болезнь, болезнь воскресного вечера и утром в понедельник) – хроническое метаболическое заболевание, связанное с нарушением пуринового обмена и накоплением в организме мочевой кислоты, клинически проявляющееся рецидивирующим артритом, образованием подагрических узлов (тофусов) и поражением внутренних органов.
Классификация подагры (по МКБ-10):
А) идиопатическая подагра
Б) свинцовая подагра
В) лекарственная подагра
Г) подагра, обусловленная нарушением почечной функции
Выделяют Первичную подагру (самостоятельное заболевание) И вторичную подагру (проявление других болезней – миелолейкоза, псориаза, ХПН, приема цитостатиков и др.
Этиология подагры:
1) причины, обуславливающие снижение экскреции мочевой кислоты (90%):
– генетически обусловленная гипофункция ферментных систем почек, регулирующих экскрецию мочевой кислоты
– дегидратация, склонность к кетоацидозу
– хроническая почечная недостаточность
– некоторые ЛС (салуретики, цитостатики)
– гипотиреоидизм и др.
2) причины, обуславливающие гиперпродукцию мочевой кислоты (10%):
– генетически обусловленное снижение активности гипоксантин-гуанинфосфорибозилтрансферазы и аденинфосфорибозил-пирофосфат-синтетазы, повышение активности 5-фосфорибозил-1-синтетазы
– миелопролиферативные заболевания (полицитемия, лейкозы)
– псориаз
– избыточное питание с преобладанием однообразной мясной пищи
– употребление определенных алкогольных напитков (особенно пива, сухих вин)
Патогенез подагры:
Дефекты энзимов обмена мочевой кислоты и др. этиологические факторы ® гиперпродукция мочевой кислоты и/или снижение ее экскреции ® гиперурикемия ® отложение уратов в тканях ®
А) активация уратовыми кристаллами в суставной полости фактора Хагемана, комплемента, кининов ® повышение сосудистой проницаемости, приток нейтрофилов, высвобождающих лизосомальные ферменты, цитокины ® острое подагрическое воспаление
Б) накопление уратовых кристаллов в интерстиции почек и канальцев ® подагрическая нефропатия и др.
Клиника подагры:
1. клиника типичного острого приступа подагры:
– начинается внезапно в любое время суток, но чаще ночью или рано утром (когда снижается скорость диффузии уратов в плазму)
– появляются резчайшие боли чаще всего в I плюснефаланговом суставе (болезненно даже прикосновение простыни)
– быстро нарастают местные симптомы воспаления, достигающие максимума через несколько часов: припухлость, отек, локальная гипертермия; кожа над суставов вначале гиперемирована, затем становится синевато-багровой, блестит, напряжена; характерно значительное ограничение подвижности сустава
– через 7-10 дней происходит полное спонтанное обратное развитие симптомов
2. проявления гиперурикемии (подагрического статуса):
– подкожные тофусы (подагрические узлы) – образуются при высокой гиперурикемии и длительности заболевания свыше 5-6 лет; представляют собой узелки желтоватого цвета, содержащие ураты, окруженные соединительной тканью; локализуются чаще всего на ушных раковинах, локтях, в бурсах локтевых суставов, стопах, на пальцах кистей, разгибательной поверхности предплечья; содержимое тофусов белого цвета, при приступах может разжижаться и выделяться через свищи (нагноения не характерны, т. к. ураты обладают бактерицидным эффектом)
– уролитиаз и нефролитиаз – мочекаменная болезнь (клиника почечной колики или присоединившегося пиелонефрита, подагрическая нефропатия (подагрический интерстициальный нефрит) с исходом в ХПН
– поражение клапанного аппарата сердца
Стадии естественного прогрессирующего течения подагры:
А) острый подагрический артрит – клиника острого приступа
Б) межприступная подагра – период между атаками падагры, когда больной не предъявляет жалоб; без адекватной терапии постепенно укорачивается
В) хроническая тофусная подагра – клиника подагрического статуса.
Диагностические критерии подагры:
А. Наличие характерных мононатриевых уратных кристаллов в синовиальной жидкости и/или
Б. Тофус, подтвержденный химическим анализом или поляризационной микроскопией и/или
С. Наличие 6 из 12 клинических, лабораторных, рентгенологических признаков:
1) максимум интенсивности воспаления в первый день
2) наличие более чем одной атаки артрита
3) моноартрит
4) покраснение сустава
5) боль и воспаление плюснефалангового сустава первого пальца
6) симметричное воспаление плюснефалангового сустава
7) одностороннее поражение суставов тыла стопы
8) подозрение на тофусы
9) гиперурикемия
10) асимметричное воспаление суставов
11) субкортикальные кисты без эрозий при рентгенологическом обследовании
12) отсутствие микроорганизмов в культуре синовиальной жидкости
Диагностика подагры:
1. Лабораторные данные:
А) ОАК: во время приступа – нейтрофильный лейкоцитоз со сдвигов влево, повышение СОЭ
Б) БАК: в периоде обострения – повышение серомукоида, фибрина, гаптоглобина, сиаловых кислот, a2- и γ-глобулинов, мочевой кислоты (повышается не во время острого приступа, а в межприступный период; в норме 0,12-0,24 ммоль/л)
В) ОАМ: при подагрической нефропатии: изостенурия, микрогематурия, протеинурия, цилиндрурия
2. Инструментальные исследования:
А) рентгенография суставов – выявляет изменения при хроническом подагрическом артрите; изменения суставов и эпифизов в виде круглых «штампованных» очагов просветления различного диаметра (из-за костных тофусов); симптом «вздутия костного края» – разрушение коркового вещества кости увеличенными узлами; возможно полное разрушение эпифизов и замещение их уратными массами (в далеко зашедших случаях заболевания)
Б) исследование синовиальной жидкости: прозрачная, вязкость не изменена или снижена, лейкоцитов 1-15*109/л, гранулоцитов 25-75%, кристаллы урата натрия
В) пункционная биопсия тофусов – обнаружение кристаллов мочевины
Лечение подагры:
1. Диета № 6: ограничение пуринов (сардин, анчоусов, печени, жирного мяса), жиров, исключение алкогольных напитков, увеличение объема выпиваемой жидкости до 2-3 л/сут.
2. Купирование острого подагрического приступа:
а) покой пораженного сустава, прохладные компрессы
б) колхицин по 0,5 мг каждый час до купирования приступа, но не более 6-8 мг/сут (не более 1 дня)
в) НПВС (индометацин, диклофенак) в высоких дозах 3-5 дней, при уменьшении боли доза снижается
г) УФО суставов, УВЧ, калий-литиевый электрофорез на сустав, аппликации димексида
NB! Нельзя применять урикостатики и уриколитики, т. к. колебания концентрации мочевой кислоты способны пролонгировать приступ подагры.
3. Лечение в межприступном периоде:
а) урикостатики – блокируют образование мочевой кислоты: аллопуринол, начальная доза 100 мг/сут с постепенным увеличением ее до 300 мг/сут за 3-4 недели
б) уриколитики – усиливают выведения мочевой кислоты: пробенецид по 250 мг 2 раза/сут 1 неделю, затем по 500 мг 2 раза/сут (противопоказнаы при МКБ, подагрическом нефрите)
в) препараты комбинированного действия (урикостатик+уриколитик): алломарон по 1 таб 1 раз/сут
г) фонофорез с гидрокортизоном, теплолечение, бальнеолечение
4. Санаторно-курортное лечение показано только в фазе ремиссии при сохраненной функции суставов (грязелечение, лечебное питание, щелочные минеральные воды, бальнеотерапия – радоновые, сероводородные ванны).
Источник
Этиология подагры.
Детерминирующим фактором риска развития подагры является содержание уратов в плазме. Под гиперурикемией понимают концентрацию уратов в сыворотке выше 7,0 мг/дл (или 0,42 ммоль/л) у мужчин и выше 6,0 мг/дл (или 0,36 ммоль/л) у женщин.
Значительная агрегация подагры и гиперурикемии у родственников свидетельствует о значении генетических факторов в предрасположенности к этому заболеванию. Так, например, в Японии описано шесть поколений японской семьи с подагрическим артритом и прогрессирующей нефропатией (Yokota N. [et al.], 1991). Имеются сведения о существовании слабой ассоциации подагры с HLA-B14 (В. Casstum [et al.], 1994).
Используя молекулярно-генетические методы исследования, было выявлено
ингибирование репаративного синтеза ДНК при воздействии мутагенов УФ-типа у больных подагрой. Выявленные изменения сохранялись в перевиваемых клеточных линиях фибробластов у пациентов с нарушением пуринового обмена. В подтверждение роли генетических факторов при подагре можно привести и данные Nicklas J., который показал, что ген, ответственный за гипоксантин-гуанин-фосфорибозилтрансферазу, находится на длинном рукаве Х-хромосомы (Xq 26).
Запасы мочевой кислоты в организме в норме составляют 1000 мг при скорости их обновления в пределах 650 мг/сут. Нарушение обмена пуринов может приводить к повышению уровня мочевой кислоты в крови. Источником образования мочевой кислоты в организме являются пуриновые соединения, поступающие с пищей, а также образующиеся в организме в процессе обмена нуклеотидов.

Метаболизм пуриновых нуклеотидов. ГГФТ — гипоксантингуанинфосфорибозил-трансфераза; АФТ — аденинфосфорибозилтрансфераза; АТФ — аденозинтрифосфат; ФРПФ — фосфорибозилпирофосфат
Метаболизм пуриновых оснований регулируется несколькими ферментами. В настоящее время доказано наличие двух ферментативных дефектов, сопровождающихся усилением синтеза мочевой кислоты и развитием подагры в детском или подростковом возрасте. Речь идет о дефиците гипоксантингуанинфос-форибозилтрансферазы (ГГФТ) и повышенной активности фосфорибозилпиро-фосфатсинтетазы (ФРПФ-синтетаза). Данные ферменты контролируются генами, связанными с Х-хромосомой. Повышенное внутриклеточное разрушение АТФ (с образованием большого количества аденина), наблюдаемое при врожденных (гликогенозы, непереносимость фруктозы) и приобретенных заболеваниях и состояниях (гипоксемия, физическая нагрузка, злоупотребление алкоголем), также может приводить к гиперурикемии. Полный дефицит ГГФТ наряду с развитием подагрического артрита приводит к выраженным психоневрологическим нарушениям: умственной отсталости, аутоагрессивности, хореоатетозу. Данный симптомокомплекс получил название синдрома Леша — Найхана.
В норме процессы синтеза мочевой кислоты и ее выделения сбалансированы. Но при каком-либо нарушении этого процесса повышается содержание мочевой кислоты в сыворотке крови: развивается гиперурикемия.
Подробный перечень факторов, способствующих гиперурикемии, приводит в своей работе Дж. Скотт (1990):
1) факторы, обусловливающие повышенное образование мочевой кислоты:
- специфические ферментные дефекты;
- снижение активности гипоксантингуанинфосфорибозилтрансферазы;
- повышение активности фосфорибозилпирофосфатсинтетазы;
- усиление обмена нуклеотидов;
- характер питания и др.;
2) факторы, обусловливающие замедление выведения мочевой кислоты:
- нарушение функции почек;
- лекарственные препараты;
- накопление кетоновых соединений;
- артериальная гипертензия;
3) другие факторы:
- раса;
- пол;
- возраст;
- нарушение липидного обмена;
- алкоголь.
Патогенез подагры.
Процессы отложения солей мочевой кислоты в тканях определяют клинические проявления подагры. Механизм отложения уратов до конца не выяснен. Определенное значение имеет недостаточная васкуляризация тканей, что подтверждается преимущественным отложением уратов в сухожилиях и хрящах. К факторам, определяющим образование кристаллов, относят концентрацию уратов, локальную температуру и наличие субстанций, удерживающих ураты в жидкости, — протеогликанов. Повышение диффузии воды из сустава ведет к увеличению концентрации уратов, что способствует их кристаллизации.
Большое значение для кристаллизации мочевой кислоты имеет и рН сыворотки крови. Доказано, что полное растворение солей мочевой кислоты происходит при рН = 12,0-13,0, что невозможно in vivo. Растворимость уратов зависит от температуры окружающей среды: переохлаждение периферических суставов способствует кристаллизации уратов и образованию микротофусов.
Образование кристаллов уратов натрия рассматривается как основной патологический процесс при подагрическом артрите. К факторам, определяющим образование кристаллов, относят концентрацию уратов, локальную температуру и присутствие или отсутствие субстанций, удерживающих ураты в жидкости, главным образом протеогликанов. Концентрация уратов в синовиальной жидкости, как правило, близка к их плазменному и тканевому содержанию, но может нарастать, если в силу каких-то причин содержание воды, например в суставе, уменьшается. Повышение диффузии воды из сустава ведет к увеличению концентрации уратов, что, в свою очередь, способствует их кристаллизации. Предполагается, что на последний процесс влияет и концентрация других катионов, таких как кальций и натрий.
Одновременно в результате метаболической активности нейтрофилов в синовиальной жидкости происходит снижение рН, что ведет к дальнейшему осаждению кристаллов уратов. Наиболее ярким проявлением этого процесса является острый подагрический артрит.
Еще в 1961 г. D. McCarty и J. Hollander установили, что острый приступ артрита развивается вследствие выпадения микрокристаллов урата натрия в полость сустава. М. Cohen и В. Emmerson (1994) полагают, что острая атака подагры ассоциируется с образованием кристаллов, а не с выходом последних из ранее образованных депозитов в субсиновии. Кристаллы уратов способны инициировать интенсивную атаку острого воспаления, так как обладают способностью стимулировать высвобождение различных медиаторов воспаления, таких как С5а, брадикинин, а также ИЛ-1, ИЛ-6 и ИЛ-8, ФНО и кислородные радикалы.

Патогенез подагрического артрита
Именно эти цитокины провоцируют приток нейтрофилов в полость сустава. Описывая воспалительную реакцию при подагре, авторы подчеркивают, что кристаллы, покрытые протеином (IgG), через реакцию с Fc-рецепторами на поверхности клеток обеспечивают фагоцитоз с образованием фаголизосом. Фаголизосо-мальные энзимы удаляют IgG с поверхности кристаллов, а водородные соединения индуцируют лизис мембран. В результате высвобождаются протеолитические ферменты лизосом, происходит секреция радикалов кислорода, простагландинов, лейкотриенов и других медиаторов воспаления. Кристаллы уратов являются активаторами комплемента, они активируют фактор Хагемана и каскад кининов.
Таким образом, активация калликреиновой и кининовой систем, увеличение проницаемости сосудистой стенки, активация системы комплемента, усиливая хемотаксис лейкоцитов к кристаллам уратов, поддерживают воспалительный процесс. В очаге воспаления снижается рН среды, что способствует еще большей кристаллизации уратов. Создается патогенетический порочный круг.
Причины, самоограничивающие течение острого подагрического артрита, до конца не ясны, но, вероятно, связаны с синтезом «антивоспалительных» медиаторов (рецепторный антагонист ИЛ-1, ТФР-β).
Патоморфология подагры.
Отложения уратов выявляются преимущественно в тканях суставов (синовиальной мембране, хряще, эпифизах костей, капсуле), околосуставных тканях (сухожилиях, связках). Гистопатологические изменения, наблюдаемые в синовиальной оболочке, включают отложения фибрина, пролиферацию синовиальных клеток и выраженную инфильтрацию нейтрофильными лейкоцитами.
Острый подагрический артрит характеризуется наличием кристаллов уратов в поверхностном слое синовиальной мембраны. Уратные кристаллы при остром артрите, как правило, находятся внутри фагоцитирующих клеток синовиальной жидкости; в составе клеточных инфильтратов преобладают нейтрофилы.
При хронической подагре поражение суставов характеризуется значительной деструкцией хряща, изменениями сухожилий, связок и синовиальных сумок, нередко выявляется и субхондральное нарушение целостности кости. При этой форме подагры происходит образование тофусов и поражение внутренних органов.
В тофусах отмечается большое скопление кристаллов уратов, окруженное гранулематозной тканью, в составе которой обнаруживаются гигантские гранулематозные многоядерные клетки. С течением времени тофусы могут кальцифицироваться, оссифицироваться.
Среди внутренних органов наиболее выраженные изменения наблюдаются в почках. Отложения уратов обнаруживают в интерстициальной ткани, в клубочках, в просвете канальцев и их стенках, в чашечках и лоханках. В интерстиции выявляется гигантоклеточная и лейкоцитарная воспалительная реакция. Изменения в клубочках (утолщение петель капилляров, умеренные клеточные инфильтраты преимущественно на периферии петель) непосредственно не связаны с отложением уратов, а являются вторичными. Возможно увеличение мезангиального матрикса, реже наблюдается мезангиальная пролиферация. В сосудах встречаются изменения типа артерио- и артериолосклероза, которые коррелируют с выраженностью тубулярной атрофии.
Несмотря на то что увеличение уровня мочевой кислоты является фактором риска, у многих больных с выраженной гиперурикемией подагра не развивается. Следовательно, в развитии подагры наряду с гиперурикемией имеют значение и другие факторы, требующие дальнейшего изучения.
Болезни суставов
В.И. Мазуров
Источник
