Подагра и ее характеристика
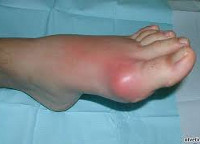
Подагра – ревматическая патология, вызванная отложением кристаллов солей мочевой кислоты – уратов в суставах, затем в почках. Клиника подагры характеризуется рецидивирующими и прогрессирующими приступами артрита с интенсивными болями и формированием тофусов – подагрических узелков, приводящих к деформации суставов. В дальнейшем поражаются почки, может развиться мочекаменная болезнь и почечная недостаточность. Для диагностики подагры производят исследование синовиальной жидкости на наличие уратов, рентгенисследование пораженных суставов. Лечение подагры направлено на купирование воспаления (НПВС, глюкокортикоиды), снижение уровня мочевой кислоты в крови, нормализацию питания.
Общие сведения
В основе патогенеза подагры лежат метаболические расстройства, вызванные нарушением регуляции обмена пуринов в организме и ведущие к накоплению мочевой кислоты и ее производных — кислых уратных солей. Увеличенная концентрация мочевой кислоты (гиперурикемия) в плазме крови и отложение уратов является следствием их повышенного синтеза и уменьшения выделения с мочой. Уратные микрокристаллы накапливаются в суставных полостях с развитием подагрического воспаления, а также в почках, вызывая подагрическую нефропатию. Подагра обычно поражает пациентов после 40 лет, при этом у мужчин она выявляется в 20 раз чаще, чем у женщин.

Подагра
Классификация подагры
В клинике подагры различаются почечная, метаболическая и смешанная формы. Почечная форма подагры характеризуется снижением экскреции мочевой кислоты, метаболическая – излишками ее образования; смешанная форма сочетает умеренные нарушения синтеза и удаления из организма мочевой кислоты.
В зависимости от причин, ведущих к развитию заболевания, подагра может быть первичной либо вторичной. Первичная подагра нередко бывает обусловлена генетическими дефектами и гипофункцией ферментов, участвующих в обмене пуринов и выведении мочевых солей. К факторам развития подагры относится избыточный и однообразный характер питания, повышенное потребление мясной пищи и алкоголя, малоактивный образ жизни. Вторичная подагра является следствием других заболеваний — патологии почек с нарушением их функций, заболеваний крови (лейкозов, лимфомы, полицитемии), псориаза, лекарственной терапии цитостатиками, салуретиками и др. препаратами.
Клиническая классификация выделяет семь форм течения подагры: типичный (классический) приступ острого подагрического артрита, полиартрит по инфекционно-аллергическому типу, подострый, ревматоидоподобный, псевдофлегмонозный, периартритический и малосимптомный варианты.
Симптомы подагры
В клинике подагры различают 3 фазы: преморбидную, интермиттирующую и хроническую.
Преморбидная фаза характеризуется бессимптомной урикемией и еще не является подагрой. На лабораторном уровне гиперурикемия выявляется у 8-14% взрослых. Интермиттирующая фаза подагры характеризуется эпизодами приступов острого артрита, чередующимися с бессимптомными периодами. К проявлениям хронической формы подагры относится образование подагрических узелков (тофусов), хроническое течение подагрического артрита, внесуставные проявления в виде поражения почек (в 50-70% клинических случаев).
Классический приступ острого подагрического артрита развивается у 50-80% пациентов. Типично внезапное начало, чаще в ночные часы. Первичный приступ подагры нередко бывает спровоцирован алкоголем, жирной пищей, травмой, переохлаждением. Приступ подагры характеризуется резчайшими болями в области плюснефалангового сустава 1-го пальца стопы, фебрильным синдромом, опуханием сустава, блеском и гиперемией кожи над ним, нарушением функции сустава. Через 3-10 суток приступ подагры стихает с исчезновением всех признаков и нормализацией функций. Повторная подагрическая атака может развиться спустя несколько месяцев и даже лет, однако с каждым разом промежутки между приступами укорачиваются. У мужчин первичный приступ подагры чаще протекает по типу моноартрита с поражением суставов стопы, у женщин – олиго- и полиартрита с вовлечением суставов кисти.
Полиартрит по инфекционно-аллергическому типу при подагре развивается у 5% пациентов. Такая форма течения подагры характеризуется мигрирующими болями во множественных суставах, быстрым регрессом признаков воспаления, как и в случае клиники инфекционно-аллергического полиартрита. Для подострого варианта течения подагры характерны типичная локализация боли в первом плюснефаланговом суставе и умеренно выраженные признаки поражения. При подострой подагре у молодых пациентов возможно развитие моно- или олигоартрита средних и крупных суставов.
Ревматоидноподобная форма подагры отличается первичной заинтересованностью суставов рук в виде моно- или олигоартрита. При псевдофлегмонозном типе подагры наблюдаются моноартриты различной локализации с воспалением сустава и парасуставных тканей, лихорадка. По клинике данный вариант напоминает течение флегмоны либо острого артрита. Малосимптомный вариант течения подагры характеризуется слабо выраженной, стертой симптоматикой – небольшой болью, слабой гиперемией кожи в зоне поражения.
Для периартритической формы подагры свойственно поражение бурс и сухожилий (чаще пяточных) при сохранных суставах. В дальнейшем присоединяются явления хронического подагрического полиартрита с поражением суставов ног, их дефигурацией и скованностью; деформации суставных тканей, костные разрастания; контрактуры, хруст в коленных и голеностопных суставах, неполные вывихи пальцев. На этом фоне продолжаются атаки подагры с возможным развитием подагрического статуса – не стихающего обострения артрита с хроническим воспалением парасуставных тканей за счет их инфильтрации солями. В результате тяжелых приступов подагры пациенты теряют трудоспособность и двигательную активность.
При длительном анамнезе подагры (дольше 5-6 лет) и гиперурикемии высокой степени появляются специфические признаки — тофусы или подагрические узелки, представляющие собой скопление кристаллов уратов в мягких тканей. Излюбленными участками локализации тофусов служат ушные раковины, подкожная клетчатка предплечий, локтей, пальцев рук, стоп, голеней, бедер. Во время приступов подагры тофусы могут вскрываться с выходом наружу беловатого отделяемого.
Осложнения подагры
Диагностика подагры
Пациентам с подозрением на подагру рекомендована консультация ревматолога и уролога. Общий анализ крови вне подагрической атаки не изменен; в период приступа отмечается нейтрофильный сдвиг лейкоцитарной формулы влево, нарастание СОЭ. Биохимическое исследование крови при обострении подагры выявляет увеличение мочевой кислоты, фибрина, серомукоида, сиаловых кислот, гаптоглобина, γ- и α2- глобулинов.
По рентгенографии суставов характерные изменения выявляются при хроническом подагрическом полиартрите. Рентгенологическая картина обнаруживает наличие остеопороза, на фоне которого определяются очаги просветления в области эпифизов и суставов размером до 2-3 см; при глубокой запущенности процесса — разрушение костных эпифизов с их замещением скоплением уратных масс. Специфические признаки подагры на рентгенограммах определяются по истечении 5 лет от манифестации заболевания.
Для взятия суставной жидкости проводят пункцию сустава. Микроскопический анализ синовиальной жидкости при подагре показывает наличие в ней микрокристаллов урата натрия. При исследовании материала, полученного при биопсии тофусов, обнаруживаются кристаллы мочевой кислоты. Во время УЗИ почек определяются уратные конкременты.
Диагностическими маркерами подагры являются:
- микрокристаллические ураты в синовиальной жидкости;
- лабораторно подтвержденные тофусы с отложением кристаллических уратов;
- наличие не менее шести из перечисленных далее признаков: присутствие в анамнезе более одной острой атаки артрита; максимальные признаки воспаления сустава в острой фазе; покраснение кожи над воспаленным суставом; моноартикулярный тип поражения; боль и припухлость I плюсне-фалангового сустава с одной стороны; односторонний характер поражения свода стопы; тофусоподобные узелки; асимметричная припухлость сустава; гиперурикемия; рентгенологически определяемые субкортикальные кисты без эрозии; отсутствие роста микрофлоры при бакпосеве суставной жидкости.
Лечение подагры
Основным принципом терапии подагры является контроль содержания мочевой кислоты путем подавления ее продукции и ускорения выведения из организма. Назначается диета, исключающая потребление рыбных и мясных бульонов, мяса животных, почек, печени, легких, алкоголя. В рационе питания вводится ограничение на бобовые и овощные культуры (фасоль, горох, бобы, шпинат, щавель, редис, баклажаны, спаржу, цветную капусту), грибы, икру, некоторые виды рыбы (сардины, балтийскую сельдь и др.). При подагре потребность в калориях удовлетворяется за счет углеводистой пищи, поэтому пациентам следует контролировать свой вес. В умеренных количествах разрешается употреблять в пищу яйца, крупы, нежирную рыбу, баранину, говядину. При подагре требуется ограничение солевой нагрузки и прием достаточного объема жидкости (до 3-х литров в сутки).
Медикаментозный подход к терапии подагры направлен на купирование острых подагрических атак, их предотвращение в дальнейшем, предупреждение отложения уратов в суставах и почках. Для купирования приступов подагры используются НПВП (индометацин), растительные алкалоиды (колхицин), местные мази и гели. В качестве антирецидивной терапии при подагре назначается колхицин в малых дозах или антигиперурикемические препараты. Целью лечения подагры является понижение концентрации мочевой кислоты в крови в 2 раза ниже нормы, требуемое для растворения уратных кристаллов. Для активизации выведения мочевой кислоты производится назначение урикозурических препаратов — пробенецида, сульфинпиразона, азапропазона, бензбромарона. К средствам, ингибирующим продукцию мочевой кислоты, относятся аллопуринол.
При атипичной форме подагры, протекающей со скоплением внутрисуставного выпота, производится его пункционная эвакуация. Проведение сеансов экстракорпоральной гемокоррекции направлено на снижение концентрации мочевой кислоты и уратных солей, подавление воспаления и снижение дозировки принимаемых препаратов. Физиотерапевтическое и курортное лечение при подагре проводится в ремиссионной стадии. Проведение УФО области заинтересованного сустава в острую фазу в ряде случаев помогает прекратить начавшийся приступ подагры.
Прогноз и профилактика подагры
Своевременное распознавание и начало рационального лечения дает прогностически благоприятные результаты. Факторами, усугубляющими прогноз подагры, являются молодой (до 30 лет) возраст, сочетание мочекаменной болезни и инфекций мочевыделительного тракта, отягощенный соматический анамнез (сахарный диабет, артериальная гипертензия), прогрессирование нефропатии.
Необходимость профилактики подагры следует учитывать при проведении химиотерапии, а также у пациентов с угрозой распада и некроза опухоли. С первого дня курса химиотерапевтического лечения необходимо назначение гипоурикемических препаратов (аллопуринола). Профилактика новых обострений подагры зависит от соблюдения водно-солевого режима, диеты, контроля массы тела. При наличии родственников, страдающих подагрой, другим членам семьи рекомендуется следить за уровнем мочевой кислоты.
Источник
Пода́гра (др.-греч. ποδάγρα, буквально — капкан для ног; от πούς, ποδός — нога и ἄγρα — ловля, охота)[3] — метаболическое заболевание, которое характеризуется отложением в различных тканях организма кристаллов уратов в форме моноурата натрия или мочевой кислоты. В основе возникновения лежит накопление мочевой кислоты и уменьшение её выведения почками, что приводит к повышению концентрации последней в крови (гиперурикемия). Клинически подагра проявляется рецидивирующим острым артритом и образованием подагрических узлов — тофусов. Поражение почек также является одним из основных клинических проявлений подагры наряду с артритом.
Чаще заболевание встречается у мужчин, однако в последнее время возрастает распространённость заболевания среди женщин, с возрастом распространённость подагры увеличивается. Для лечения используются препараты, воздействующие на патогенетический механизм заболевания, а также препараты для симптоматического лечения.
История[править | править код]
«Подагра». Иллюстрация Джеймса Гилрея, 1799. Мастер карикатуры изобразил болевой синдром при подагре как демона или дракона
Подагра известна с глубокой древности. Первые документальные свидетельства заболевания известны из Древнего Египта и датируются 2600 годом до н. э.[4] Они основываются на описании подагрического артрита большого пальца[4]. Древнегреческий целитель и врач Гиппократ в V веке до н. э. описывал клинические симптомы подагрического артрита в своих «Афоризмах», где он отметил, что заболевание не встречается у евнухов и женщин до наступления менопаузы[5][6]. Римский философ и врач Авл Корнелий Цельс описывал взаимосвязь развития подагры с употреблением алкоголя и связанными с ней нарушениями работы почек[7]. В 150 году Гален указывал, что подагра обусловлена «распущенностью, несдержанностью и наследственностью»[8].
В конце XVII века английский врач-клиницист Томас Сиденгам, более 30 лет страдавший подагрой, классифицировал её как отдельную болезнь и весьма точно описал клиническую картину острого приступа подагрического артрита в работе «Трактат о подагре» (лат. «Tractatus de podagra et hydrope»). В нём он сравнивал болевой синдром при подагре с болями «от зажима конечности прессом» и описывал ощущения больного, сравнимые с тем, как «в палец впилась клыками огромная собака»[9]. В 1679 году голландский учёный Антони ван Левенгук впервые описал микроскопическое строение кристаллов мочевой кислоты[5].
В 1848 году английский физиолог Альфред Баринг Гаррод (Alfred Baring Garrod, 1819—1906) при помощи нитки, опущенной в кровь пациента, страдающего подагрой, открыл и описал факт повышения содержания мочевой кислоты в крови при этом заболевании[10][11][12].
Первые научные работы французского врача Жана Мартена Шарко относятся к области подагры: «Повреждения хряща при подагре» (фр. Les altérations des cartilages dans la gouite, 1858), «Подагрические отложения (тофусы) в наружном ухе у подагриков» (Les concrétions tophacées de l’oreille externe chez les goutteux, 1860), «Изменения в почках при подагре» (Les altérations du rein chez les goutteux, 1864), «О подагре и свинцовых отравлениях» (Les rapports de la goutte et de l’intoxication saturnine, 1864).
В 1899 году было обнаружено наличие кристаллов уратов в суставной жидкости во время приступа подагрического артрита. В 1961 году MacCarty и Hollander выявили роль кристаллов уратов в возникновении и развитии подагрического воспаления[13].
Исторически сложилось так, что со Средних веков и до XX века подагрой страдали преимущественно богатые и знатные люди, в связи с чем она носила название «болезнь королей»[4][14], «болезнь богачей» и «болезнь аристократов»[4]. Считалось, что она была связана с избыточным весом, перееданием (особенно злоупотреблением мясной пищей) и чрезмерным употреблением алкогольных напитков. К примеру, в 1739 году француз Эжен Мушрон (фр. Eugène Moucheron) издал брошюру под названием «О благородной подагре и сопровождающих её добродетелях», в которой воспевал подагру и отмечал, что это болезнь королей, принцев, выдающихся полководцев, умных и одарённых людей, а также приводил примеры коронованных особ, политических деятелей, людей искусства, страдавших подагрой[15]. Новая вспышка интереса к подагре возникла в начале XX века, когда Хавелок Эллис (англ. Henry Havelock Ellis, 1859—1939) опубликовал в 1927 году книгу под названием «История английского гения». В ней автор касался темы подагры и приводил в пример 55 известных выдающихся англичан, болеющих ею[16]. В 1955 году вышла работа Эгона Орована «The origin of man», опубликованная в журнале «Nature», в которой он описывал повышенную частоту болеющих подагрой среди гениев и объяснял её тем, что мочевая кислота структурно является весьма сходной с метилированными пуринами: кофеином, теофиллином и теобромином, являющимися стимуляторами умственной активности, оказывающими стимулирующее воздействие на высшие мозговые функции, в частности, концентрацию внимания и способность к концентрации. Орован указал, что мочевая кислота у всех развитых млекопитающих, за исключением человекообразных обезьян и человека, расщепляется под действием вырабатываемого в печени фермента уриказы до аллантоина, у приматов же, из-за отсутствия уриказы, она сохраняется в крови[16]
Эпидемиология[править | править код]
Гиперурикемия выявляется у 4—12 % населения, подагрой страдает 0,1 % населения России[17].
В США и Европе подагрой болеют 2 % жителей, среди мужчин в возрасте 55—65 лет подагрой болеют 4—6 %.
Соотношение мужчин к женщинам составляет от 7:1 до 19:1. Пик заболеваемости приходится на 40-50 лет у мужчин, 60 лет и старше у женщин. До менопаузы женщины заболевают редко, вероятно за счёт воздействия эстрогенов на экскрецию мочевой кислоты[17].
Частота подагрического артрита в различных популяциях колеблется и составляет от 5 до 50 на 1000 мужчин и 1-9 на 1000 женщин, а число новых случаев в год — соответственно 1−3 на 1000 у мужчин и 0,2 на 1000 у женщин[17]. За последнее десятилетие[когда?] частота случаев заболевания подагрой возросла[18].
Острый приступ подагры у подростков и молодых людей наблюдают редко, обычно он опосредован первичным или вторичным дефектом синтеза мочевой кислоты[17].
Этиология[править | править код]
Факторы развития заболевания[править | править код]
Существует целый ряд факторов риска, способствующих возникновению и развитию подагры у определённых лиц.
К факторам риска развития подагры относят артериальную гипертонию, гиперлипидемию, а также:
- повышенное поступление в организм пуриновых оснований, например, при употреблении большого количества красного мяса (особенно субпродуктов), некоторых сортов рыбы, какао, чая, шоколада, гороха, чечевицы, фруктозы, алкоголя (особенно пива, содержащего много гуанозина и ксантина — предшественников мочевой кислоты);
- увеличение количества пуриновых нуклеотидов при общем катаболизме (например при противоопухолевой терапии; массивном апоптозе у людей с аутоиммунными болезнями);
- торможение выведения мочевой кислоты с мочой (например при почечной недостаточности);
- повышенный синтез мочевой кислоты при одновременном снижении выведения её из организма (например, при злоупотреблении алкоголем, шоковых состояниях, гликогенозе с недостаточностью глюкозо-6-фосфатазы);
- наследственная предрасположенность (характер наследования всё ещё окончательно не выяснен).
Патогенез[править | править код]
В основе патогенеза заболевания находится повышение уровня мочевой кислоты в крови. Но данный симптом не является синонимом заболевания, так как гиперурикемия также наблюдается при других заболеваниях (болезни крови, опухоли, заболевания почек и т. д.), чрезвычайно высоких физических перегрузках и питании жирной пищей.
Выделяют минимум три основных элемента возникновения подагры:
- накопление мочекислых соединений в организме;
- отложение данных соединений в органах и тканях;
- развитие острых приступов воспаления в данных местах поражения, образования подагрических гранулем и подагрических «шишек» — тофусов, обычно вокруг суставов.
Симптомы и течение заболевания[править | править код]
Полная естественная эволюция подагры проходит четыре стадии:
- бессимптомная гиперурикемия;
- острый подагрический артрит;
- межкритический период;
- хронические подагрические отложения в суставах.
Нефролитиаз может развиться в любой стадии, кроме первой.
Наблюдается постоянно повышенная концентрация мочевой кислоты в плазме крови и в моче; воспаление суставов по типу моноартритов, что сопровождается сильной болью и лихорадкой; уролитиаз и рецидивирующие пиелонефриты, завершающиеся нефросклерозом и почечной недостаточностью.
Диагностика[править | править код]
Диагноз подагрического артрита может быть установлен на основании эпидемиологических критериев диагностики, принятых на третьем международном симпозиуме по исследованиям ревматических болезней, Нью-Йорк, 1966.
1. При химическом или микроскопическом выявлении кристаллов мочевой кислоты в синовиальной жидкости или отложении уратов в тканях.
2. При наличии двух или более таких критериев:
- чёткий анамнез и/или наблюдение хотя бы двух атак болевого припухания суставов конечностей (атаки, по меньшей мере, на ранних стадиях, должны начинаться внезапно с сильным болевым синдромом; на протяжении 1-2 недель должна наступать полная клиническая ремиссия);
- чёткий анамнез и/или наблюдение подагрической атаки (см. выше) с поражением большого пальца ноги;
- клинически доказанные тофусы; чёткий анамнез и/или наблюдение быстрой реакции на колхицин, то есть уменьшение объективных признаков воспаления на протяжении 48 часов после начала терапии.
Рентгеновское исследование не включено в список обязательных диагностических исследований, однако оно может показать тофусные отложения кристаллов и повреждение костной ткани в результате повторных воспалений. Рентгеновское исследование также может быть полезно для мониторирования влияния хронической подагры на суставы.
Выявления гиперурикемии недостаточно для установления диагноза, так как лишь 10 % лиц с гиперурикемией страдают подагрой[17].
Диагностические критерии подагры (ВОЗ 2000г)[править | править код]
I. Наличие характерных кристаллических уратов в суставной жидкости.
II. Наличие тофусов (доказанных), содержащих кристаллические ураты, подтверждённые химически или поляризационной микроскопией.
III. Наличие как минимум 6 из 12 ниже представленных признаков:
- более чем одна острая атака артрита в анамнезе;
- максимум воспаления сустава уже в первые сутки;
- моноартикулярный характер артрита;
- гиперемия кожи над поражённым суставом;
- припухание или боль, локализованные в I плюснефаланговом суставе;
- одностороннее поражение суставов свода стопы;
- узелковые образования, напоминающие тофусы;
- гиперурикемия;
- одностороннее поражение I плюснефалангового сустава;
- асимметричное припухание поражённого сустава;
- обнаружение на рентгенограммах субкортикальных кист без эрозий;
- отсутствие флоры в суставной жидкости.
Наиболее достоверны такие признаки, как острый или, реже, подострый артрит, обнаружение кристаллических уратов в синовиальной жидкости и наличие доказанных тофусов. Кристаллы уратов имеют вид палочек или тонких игл с обломанными или закруглёнными концами длиной около 10 мкм. Микрокристаллы уратов в синовиальной жидкости обнаруживаются как свободно лежащими, так и в нейтрофилах.
Дифференциальная диагностика[править | править код]
Подагру дифференцируют с сепсисом, который может протекать параллельно с ней, а также с другими микрокристаллическими артритами (кристаллассоциированными синовиитами прежде всего с хондрокальцинозом (в первую очередь с депозицией пирофосфата кальция — особенно у лиц пожилого возраста); реактивными, псориатическим и ревматоидным артритами.
Лечение[править | править код]
Больные подагрой, впервые выявленной или в периоде обострения заболевания, подлежат стационарному лечению в специализированных ревматологических отделениях областных или городских больниц. Больные подагрой в период ремиссии заболевания при условии назначения адекватной терапии могут находиться под надзором ревматолога, нефролога по месту жительства в районных поликлиниках. Ориентировочная продолжительность лечения в стационарных условиях (специализированные ревматологические отделения) — 7-14 суток при условии подбора адекватной эффективной терапии, улучшение клинических и лабораторных признаков заболевания.
На сегодняшний день, современная фармакология так и не смогла представить ни одного препарата, который одновременно был бы универсальным, и мог бы действительно решать вопрос лечения подагры.
Лечение при подагре предусматривает:
- по возможности быстрое и осторожное купирование острого приступа;
- профилактику рецидива острого подагрического артрита;
- профилактику или регресс осложнений болезни, вызванной отложением кристаллов однозамещенного урата натрия в суставах, почках и других тканях;
- профилактику или регресс сопутствующих симптомов, таких как ожирение, гипертриглицеридемия или гипертензия;
- профилактику образования мочекислых почечных камней.
Лечение при остром приступе подагры[править | править код]
При остром подагрическом артрите проводят противовоспалительное лечение. Чаще всего используют колхицин. Его назначают для приёма внутрь обычно в дозе 0,5 мг каждый час или 1 мг каждые 2 ч, и лечение продолжают до тех пор, пока: 1) не наступит облегчение состояния больного; 2) не появятся побочные реакции со стороны желудочно-кишечного тракта или 3) общая доза препарата не достигнет 6 мг на фоне отсутствия эффекта. Колхицин наиболее эффективен, если лечение начинают вскоре после появления симптомов. В первые 12 ч лечения состояние существенно улучшается более чем у 75 % больных. Однако у 80 % больных препарат вызывает побочные реакции со стороны желудочно-кишечного тракта, которые могут проявляться раньше клинического улучшения состояния или одновременно с ним. При приёме внутрь максимальный уровень колхицина в плазме достигается примерно через 2 ч. Следовательно, можно предположить, что его приём по 1,0 мг каждые 2 ч с меньшей вероятностью обусловит накопление токсичной дозы до проявления терапевтического эффекта. Поскольку, однако, терапевтическое действие связано с уровнем колхицина в лейкоцитах, а не в плазме, эффективность режима лечения требует дальнейшей оценки.
При внутривенном введении колхицина побочные эффекты со стороны желудочно-кишечного тракта не наступают, а состояние больного улучшается быстрее. После однократного введения уровень препарата в лейкоцитах повышается, оставаясь постоянным в течение 24 ч, и поддаётся определению даже спустя 10 сут. В качестве начальной дозы внутривенно следует вводить 2 мг, а затем, если необходимо, двукратно повторить введение по 1 мг с интервалом в 6 ч. При внутривенном введении колхицина следует соблюдать специальные предосторожности. Он оказывает раздражающее действие и при попадании в окружающие сосуд ткани может вызвать резкую боль и некроз. Важно помнить, что внутривенный путь введения требует аккуратности и что препарат следует разводить в 5—10 объёмах обычного солевого раствора, а вливание продолжать не менее 5 мин. Как при пероральном, так и при парентеральном введении колхицин может угнетать функцию костного мозга и вызывать алопецию, недостаточность печёночных клеток, психическую депрессию, судороги, восходящий паралич, угнетение дыхания и смерть. Токсические эффекты более вероятны у больных с патологией печени, костного мозга или почек, а также у получающих поддерживающие дозы колхицина. Во всех случаях дозу препарата необходимо уменьшить. Его не следует назначать больным с нейтропенией.
При остром подагрическом артрите эффективны и другие противовоспалительные средства, в том числе индометацин, фенилбутазон, напроксен, эторикоксиб и др.
Индометацин можно назначать для приёма внутрь в дозе 75 мг, после которой через каждые 6 ч больной должен получать по 50 мг; лечение этими дозами продолжается и на следующие сутки после исчезновения симптомов, затем дозу уменьшают до 50 мг каждые 8 ч (трижды) и до 25 мг каждые 8 ч (тоже трижды). К побочным эффектам индометацина относятся желудочно-кишечные расстройства, задержка натрия в организме и симптомы со стороны центральной нервной системы. Несмотря на то, что указанные дозы могут вызывать побочные эффекты почти у 60 % больных, индометацин переносится обычно легче, чем колхицин, и служит, вероятно, средством выбора при остром подагрическом артрите.
Препараты, стимулирующие экскрецию мочевой кислоты, и аллопуринол при остром приступе подагры неэффективны.
При острой подагре, особенно при противопоказаниях или неэффективности колхицина и нестероидных противовоспалительных средств, пользу приносит системное или местное (то есть внутрисуставное) введение глюкокортикоидов. Для системного введения, будь то пероральное или внутривенное, следует назначать умеренные дозы в течение нескольких дней, так как концентрация глюкокортикоидов быстро уменьшается и их действие прекращается. Внутрисуставное введение длительно действующего стероидного препарата (например гексацетонид триамцинолона в дозе 15—30 мг) может купировать приступ моноартрита или бурсита в течение 24—36 ч. Это лечение особенно целесообразно при невозможности использовать стандартную лекарственную схему.
Диета[править | править код]
Традиционные рекомендации по диете заключаются в ограничении потребления пуринов и алкоголя. К продуктам с высоким содержанием пуринов относятся мясные и рыбные продукты, а также чай, какао и кофе. Недавно также было показано, что снижение веса, достигаемое умеренным ограничением углеводов и калорийной пищи в сочетании с пропорциональным повышением белка и ненасыщенных жирных кислот, приводило у больных подагрой к значительному уменьшению уровня мочевой кислоты и дислипидемии[19].
См. также[править | править код]
- Артрит микрокристаллический
- Хондрокальциноз
- Ураты
- Мочевая кислота
- Тофус
Примечания[править | править код]
- ↑ 1 2 3 4 Monarch Disease Ontology release 2018-06-29sonu — 2018-06-29 — 2018.
- ↑ 1 2 3 4 база данных Disease ontology (англ.) — 2016.
- ↑ Подагра / В. Г. Барскова // Перу — Полуприцеп. — М. : Большая российская энциклопедия, 2014. — С. 524. — (Большая российская энциклопедия : [в 35 т.] / гл. ред. Ю. С. Осипов ; 2004—2017, т. 26). — ISBN 978-5-85270-363-7.
- ↑ 1 2 3 4 Richette P., Bardin T. Gout // Lancet. — January 2010. — Vol. 375, № 9711. — P. 318—328. — doi:10.1016/S0140-6736(09)60883-7. — PMID 19692116.
- ↑ 1 2 Pillinger M. H., Rosenthal P., Abeles A.M. Hyperuricemia and gout: new insights into pathogenesis and treatment // Bulletin of the NYU Hospital for Joint Diseases. — 2007. — Vol. 65, № 3. — P. 215–221. — PMID 17922673. Архивировано 16 декабря 2008 года.
- ↑ The Internet Classics Archive Aphorisms by Hippocrates. MIT.
- ↑ A. Cornelius Celsus. On Medicine. University of Chicago.
- ↑ Зилва Дж. Ф., Пэннелл П. Р. Клиническая химия в диагностике и лечении. — М.: Медицина, 1988. — 528 с. — ISBN 5-225-00220-X.
- ↑ Насонова В., Барскова В. Болезнь изобилия // Наука и жизнь. — 2004. — № 7.
- ↑ Garrod A. B. The nature and treatment of gout and rheumatic gout. — London: Walton and Maberly, 1859.
- ↑ Keitel W. The High Priest of gout – Sir Alfred Baring Garrod (1819–1907) // Z Rheumatol. — 2009. — Vol. 68, № 10. — P. 851—856. — doi:10.1007/s00393-009-0541-4. — PMID 19937040.
- ↑ Storey G. D. Alfred Baring Garrod (1819–1907) // Rheumatology (Oxford). — 2001. — Vol. 40, № 10. — P. 1189—1190. — doi:10.1093/rheumatology/40.10.1189. — PMID 11600751.
- ↑ McCarthy D. J., Hollander J. L. Identification of urate crystals in gouty synovial fluid. // Annals of Internal Medicine. — 1961. — Vol. 54. — P. 452.
- ↑ The Disease Of Kings — Forbes.com. Forbes.
- ↑ Засельский В., Лалаянц И. Природа гениальности // Огонёк. — 1996. — № 27. — С. 4.
- ↑ 1 2 Лалаянц И. Мочевая кислота бьёт в голову. Шишки гениальности следовало бы искать не на голове, а на ногах // Вокруг света. — 2008.
- ↑ 1 2 3 4 5 Под ред. С.Л. Насонова. Клинические рекомендации. Ревматология. — ГЭОТАР-Медиа, 2008. — С. 112—119. — 288 с. — ISBN 978-5-9704-0698-4.
- ↑ Lisa K. Stamp, Tony R. Merriman, Nicola Dalbeth. Gout (англ.) // The Lancet. — 2016-10-22. — Т. 388, вып. 10055. — С. 2039–2052. — ISSN 1474-547X 0140-6736, 1474-547X. — doi:10.1016/S0140-6736(16)00346-9.
- ↑ Барскова, В.Г. & Насонова, В.А. (2002), Подагра и синдром инсулинорезистентности, <https://medinfa.ru/article/31/117288/> Архивная копия от 1 февраля 2009 на Wayback Machine
Ссылки[править | править код]
- Мочевая кислота бьет в голову // Вокруг света
Источник
