Порочный круг при подагре

Этиология подагры.
Детерминирующим фактором риска развития подагры является содержание уратов в плазме. Под гиперурикемией понимают концентрацию уратов в сыворотке выше 7,0 мг/дл (или 0,42 ммоль/л) у мужчин и выше 6,0 мг/дл (или 0,36 ммоль/л) у женщин.
Значительная агрегация подагры и гиперурикемии у родственников свидетельствует о значении генетических факторов в предрасположенности к этому заболеванию. Так, например, в Японии описано шесть поколений японской семьи с подагрическим артритом и прогрессирующей нефропатией (Yokota N. [et al.], 1991). Имеются сведения о существовании слабой ассоциации подагры с HLA-B14 (В. Casstum [et al.], 1994).
Используя молекулярно-генетические методы исследования, было выявлено
ингибирование репаративного синтеза ДНК при воздействии мутагенов УФ-типа у больных подагрой. Выявленные изменения сохранялись в перевиваемых клеточных линиях фибробластов у пациентов с нарушением пуринового обмена. В подтверждение роли генетических факторов при подагре можно привести и данные Nicklas J., который показал, что ген, ответственный за гипоксантин-гуанин-фосфорибозилтрансферазу, находится на длинном рукаве Х-хромосомы (Xq 26).
Запасы мочевой кислоты в организме в норме составляют 1000 мг при скорости их обновления в пределах 650 мг/сут. Нарушение обмена пуринов может приводить к повышению уровня мочевой кислоты в крови. Источником образования мочевой кислоты в организме являются пуриновые соединения, поступающие с пищей, а также образующиеся в организме в процессе обмена нуклеотидов.

Метаболизм пуриновых нуклеотидов. ГГФТ — гипоксантингуанинфосфорибозил-трансфераза; АФТ — аденинфосфорибозилтрансфераза; АТФ — аденозинтрифосфат; ФРПФ — фосфорибозилпирофосфат
Метаболизм пуриновых оснований регулируется несколькими ферментами. В настоящее время доказано наличие двух ферментативных дефектов, сопровождающихся усилением синтеза мочевой кислоты и развитием подагры в детском или подростковом возрасте. Речь идет о дефиците гипоксантингуанинфос-форибозилтрансферазы (ГГФТ) и повышенной активности фосфорибозилпиро-фосфатсинтетазы (ФРПФ-синтетаза). Данные ферменты контролируются генами, связанными с Х-хромосомой. Повышенное внутриклеточное разрушение АТФ (с образованием большого количества аденина), наблюдаемое при врожденных (гликогенозы, непереносимость фруктозы) и приобретенных заболеваниях и состояниях (гипоксемия, физическая нагрузка, злоупотребление алкоголем), также может приводить к гиперурикемии. Полный дефицит ГГФТ наряду с развитием подагрического артрита приводит к выраженным психоневрологическим нарушениям: умственной отсталости, аутоагрессивности, хореоатетозу. Данный симптомокомплекс получил название синдрома Леша — Найхана.
В норме процессы синтеза мочевой кислоты и ее выделения сбалансированы. Но при каком-либо нарушении этого процесса повышается содержание мочевой кислоты в сыворотке крови: развивается гиперурикемия.
Подробный перечень факторов, способствующих гиперурикемии, приводит в своей работе Дж. Скотт (1990):
1) факторы, обусловливающие повышенное образование мочевой кислоты:
- специфические ферментные дефекты;
- снижение активности гипоксантингуанинфосфорибозилтрансферазы;
- повышение активности фосфорибозилпирофосфатсинтетазы;
- усиление обмена нуклеотидов;
- характер питания и др.;
2) факторы, обусловливающие замедление выведения мочевой кислоты:
- нарушение функции почек;
- лекарственные препараты;
- накопление кетоновых соединений;
- артериальная гипертензия;
3) другие факторы:
- раса;
- пол;
- возраст;
- нарушение липидного обмена;
- алкоголь.
Патогенез подагры.
Процессы отложения солей мочевой кислоты в тканях определяют клинические проявления подагры. Механизм отложения уратов до конца не выяснен. Определенное значение имеет недостаточная васкуляризация тканей, что подтверждается преимущественным отложением уратов в сухожилиях и хрящах. К факторам, определяющим образование кристаллов, относят концентрацию уратов, локальную температуру и наличие субстанций, удерживающих ураты в жидкости, — протеогликанов. Повышение диффузии воды из сустава ведет к увеличению концентрации уратов, что способствует их кристаллизации.
Большое значение для кристаллизации мочевой кислоты имеет и рН сыворотки крови. Доказано, что полное растворение солей мочевой кислоты происходит при рН = 12,0-13,0, что невозможно in vivo. Растворимость уратов зависит от температуры окружающей среды: переохлаждение периферических суставов способствует кристаллизации уратов и образованию микротофусов.
Образование кристаллов уратов натрия рассматривается как основной патологический процесс при подагрическом артрите. К факторам, определяющим образование кристаллов, относят концентрацию уратов, локальную температуру и присутствие или отсутствие субстанций, удерживающих ураты в жидкости, главным образом протеогликанов. Концентрация уратов в синовиальной жидкости, как правило, близка к их плазменному и тканевому содержанию, но может нарастать, если в силу каких-то причин содержание воды, например в суставе, уменьшается. Повышение диффузии воды из сустава ведет к увеличению концентрации уратов, что, в свою очередь, способствует их кристаллизации. Предполагается, что на последний процесс влияет и концентрация других катионов, таких как кальций и натрий.
Одновременно в результате метаболической активности нейтрофилов в синовиальной жидкости происходит снижение рН, что ведет к дальнейшему осаждению кристаллов уратов. Наиболее ярким проявлением этого процесса является острый подагрический артрит.
Еще в 1961 г. D. McCarty и J. Hollander установили, что острый приступ артрита развивается вследствие выпадения микрокристаллов урата натрия в полость сустава. М. Cohen и В. Emmerson (1994) полагают, что острая атака подагры ассоциируется с образованием кристаллов, а не с выходом последних из ранее образованных депозитов в субсиновии. Кристаллы уратов способны инициировать интенсивную атаку острого воспаления, так как обладают способностью стимулировать высвобождение различных медиаторов воспаления, таких как С5а, брадикинин, а также ИЛ-1, ИЛ-6 и ИЛ-8, ФНО и кислородные радикалы.

Патогенез подагрического артрита
Именно эти цитокины провоцируют приток нейтрофилов в полость сустава. Описывая воспалительную реакцию при подагре, авторы подчеркивают, что кристаллы, покрытые протеином (IgG), через реакцию с Fc-рецепторами на поверхности клеток обеспечивают фагоцитоз с образованием фаголизосом. Фаголизосо-мальные энзимы удаляют IgG с поверхности кристаллов, а водородные соединения индуцируют лизис мембран. В результате высвобождаются протеолитические ферменты лизосом, происходит секреция радикалов кислорода, простагландинов, лейкотриенов и других медиаторов воспаления. Кристаллы уратов являются активаторами комплемента, они активируют фактор Хагемана и каскад кининов.
Таким образом, активация калликреиновой и кининовой систем, увеличение проницаемости сосудистой стенки, активация системы комплемента, усиливая хемотаксис лейкоцитов к кристаллам уратов, поддерживают воспалительный процесс. В очаге воспаления снижается рН среды, что способствует еще большей кристаллизации уратов. Создается патогенетический порочный круг.
Причины, самоограничивающие течение острого подагрического артрита, до конца не ясны, но, вероятно, связаны с синтезом «антивоспалительных» медиаторов (рецепторный антагонист ИЛ-1, ТФР-β).
Патоморфология подагры.
Отложения уратов выявляются преимущественно в тканях суставов (синовиальной мембране, хряще, эпифизах костей, капсуле), околосуставных тканях (сухожилиях, связках). Гистопатологические изменения, наблюдаемые в синовиальной оболочке, включают отложения фибрина, пролиферацию синовиальных клеток и выраженную инфильтрацию нейтрофильными лейкоцитами.
Острый подагрический артрит характеризуется наличием кристаллов уратов в поверхностном слое синовиальной мембраны. Уратные кристаллы при остром артрите, как правило, находятся внутри фагоцитирующих клеток синовиальной жидкости; в составе клеточных инфильтратов преобладают нейтрофилы.
При хронической подагре поражение суставов характеризуется значительной деструкцией хряща, изменениями сухожилий, связок и синовиальных сумок, нередко выявляется и субхондральное нарушение целостности кости. При этой форме подагры происходит образование тофусов и поражение внутренних органов.
В тофусах отмечается большое скопление кристаллов уратов, окруженное гранулематозной тканью, в составе которой обнаруживаются гигантские гранулематозные многоядерные клетки. С течением времени тофусы могут кальцифицироваться, оссифицироваться.
Среди внутренних органов наиболее выраженные изменения наблюдаются в почках. Отложения уратов обнаруживают в интерстициальной ткани, в клубочках, в просвете канальцев и их стенках, в чашечках и лоханках. В интерстиции выявляется гигантоклеточная и лейкоцитарная воспалительная реакция. Изменения в клубочках (утолщение петель капилляров, умеренные клеточные инфильтраты преимущественно на периферии петель) непосредственно не связаны с отложением уратов, а являются вторичными. Возможно увеличение мезангиального матрикса, реже наблюдается мезангиальная пролиферация. В сосудах встречаются изменения типа артерио- и артериолосклероза, которые коррелируют с выраженностью тубулярной атрофии.
Несмотря на то что увеличение уровня мочевой кислоты является фактором риска, у многих больных с выраженной гиперурикемией подагра не развивается. Следовательно, в развитии подагры наряду с гиперурикемией имеют значение и другие факторы, требующие дальнейшего изучения.
Болезни суставов
В.И. Мазуров
Источник
Над статьей доктора
Шестернина А. С.
работали
литературный редактор
Елена Бережная,
научный редактор
Сергей Федосов
Дата публикации 6 декабря 2017Обновлено 22 июля 2019
Определение болезни. Причины заболевания
Подагра — системное заболевание, которое развивается в связи с воспалительным процессом, возникшим в месте отложения кристаллов моноурата натрия у людей с повышенным уровнем мочевой кислоты в сыворотке крови (более 360 мкмоль/л). Гиперурикемия возникает под воздействием как внешнесредовых, так и генетических факторов.
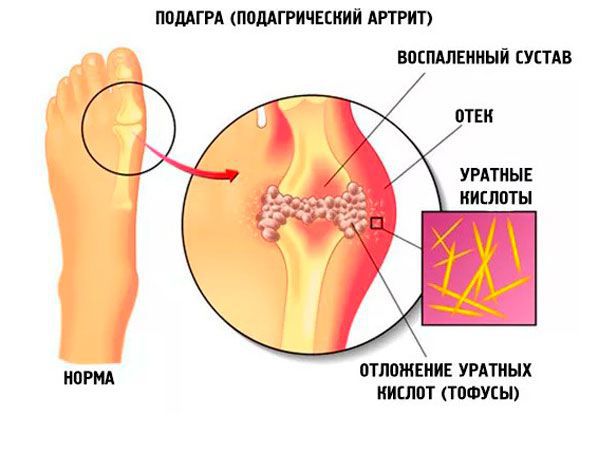
Заболеванию, как правило, подвержены мужчины, однако в последнее время оно выявляется и у слабого пола. Распространенность подагры растет, и это можно связать с ростом уровня жизни населения. Бессимптомная гиперурикемия встречается часто, однако далеко не всегда при этом развивается подагра.
На развитие подагры влияет:
- наследственность (предрасположенность к нарушению обмена пуринов);
- избыток в пище пуринов;
- нарушение функции почек, когда теряется их способность выводить мочевую кислоту (хроническая почечная недостаточность, поликистоз почек, гидронефроз, нефропатия в связи со злоупотреблением нестероидными противовоспалительными препаратами, при голодании);
- увеличение распада пуриновых нуклеотидов (цитостатическая терапия, лучевая и химиотерапия, хирургические вмешательства, гемолиз).[1][19]
Особенности современного течения подагры:
- значительный рост заболеваемости;
- увеличение частоты встречаемости у женщин;
- увеличение коморбидных состояний;
- начало заболевания в молодом возрасте.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением — это опасно для вашего здоровья!
Симптомы подагры
Подагра поражает опорно-двигательный аппарат и мочевыделительную систему. Возникает острый моноартрит, сопровождающийся нестерпимой, быстронарастающей и быстропроходящей за несколько часов или суток суставной болью, кожа над суставом краснеет, сам он увеличивается в объеме.
Из других симптомов — повышенная температура тела, слабость, потливость. При переходе в хроническую форму заболевания вокруг пораженных суставов образуются тофусы, суставы деформируются.
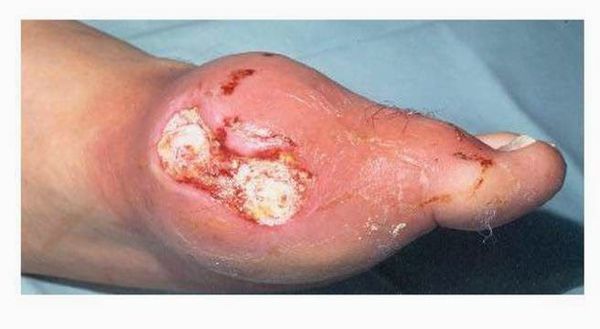
В почках образуются уратные камни, провоцируя тянущие боли в пояснице и периодическое появление крови в моче, никтурию (больше мочи выделяется ночью).[2][3]
Патогенез подагры
Поскольку образование уратов растет и нарушается выведение их почками, образуется избыток мочевой кислоты в крови, и происходит накопление уратов в тканях организма. Когда происходит отложение кристаллов моноурата в полости сустава, возникает воспалительный процесс из-за активации различных провоспалительных цитокинов. Кроме того, эти кристаллы откладываются в почечной ткани, приводя к развитию нефропатии и уратного нефролитиаза.[7]
Классификация и стадии развития подагры
3 стадии развития подагры:
- острый приступ подагрического артрита;
- межприступные периоды;
- хроническая тофусная подагра.[8]
Впервые подагрический приступ настигает пациента без предвестников, как правило, в возрасте от 40 до 50 лет, хотя известны случаи заболевания и в гораздо более молодом возрасте. Острая суставная боль, чаще в плюснефаланговом суставе большого пальца стопы (классический вариант начала), застает человека во второй половине ночи или в ранние утренние часы. Любое движение в суставе или прикосновение вызывает сильнейшую боль. Нарушение диеты, застолья с алкогольными напитками (алкоголь блокирует почку к выделению мочевой кислоты), хирургические вмешательства, инфекционные заболевания, повышенные нагрузки и травматизация сустава предшествуют возникновению приступа. Пациенты жалуются на покраснение пораженной области, ее припухание, сильную боль, общую слабость и недомогание, повышение температуры тела, потливость, разбитость, подавленность. Также характерными являются острые бурситы (препателлярный или локтевой сумки).[6]
В течение нескольких дней (около недели) приступ самостоятельно проходит. Именно из-за этого подагра часто создаёт видимость доброкачественности: всё проходит (особенно в начале) самостоятельно, и проблема забывается до следующего обострения. На самом деле подагра при таком подходе может привести к разрушению и деформации суставов, хронической болезни почек. Далее при отсутствии адекватного контроля над заболеванием приступы учащаются, перестают проходить самостоятельно, проходят за больший промежуток времени. Позже человек вообще перестает чувствовать себя здоровым, а находится в состоянии затянувшегося приступа. В результате этого над областью пораженных суставов образуются безболезненные подкожные узелки с крошковидным, творожистым содержимым – тофусы (соли мочевой кислоты беловатого или желтоватого цвета). Излюбленное место расположения тофусов – область суставов кистей и стоп, ахиллово сухожилие, ушные раковины, голеностопные и локтевые суставы. При хронической тофусной подагре происходит разрушение хряща, что грозит деформацией, полным разрушением сустава и его анкилозом (полное заращение и отсутствие движений). Иногда тофусы могут самостоятельно вскрываться, а из них выделяется густое содержимое.[9][17]
Осложнения подагры
- образование тофусов;
- формирование деформаций и анкилозов суставов;
- нефролитиаз (камни в почках);
- депрессия как следствие постоянного болевого синдрома;
- повышение артериального давления, ишемическая болезнь сердца. Гиперурикемия связана с повышенным риском смерти от болезней сердечно-сосудистой системы;
- статистически значимо при подагре гораздо более часто встречаются сопутствующие заболевания (артериальная гипертензия, сахарный диабет, атеросклероз, гипертриглицеридемия — метаболический синдром).[10]
Диагностика подагры
Диагностические критерии подагры Wallace (предложены ААР в 1975 году, одобрены ВОЗ в 2002 году):
- наличие кристаллов мочевой кислоты в суставной жидкости;
- наличие тофусов, содержание кристаллов мочевой кислоты в которых подтверждено химически или поляризационной микроскопией;
- наличие 6 из 12 следующих признаков:
- типичная картина острой суставной атаки (один и более раз) в анамнезе;
- признаки воспаления наиболее выражены в первые сутки;
- воспаление одного сустава (моноартрит);
- покраснение кожи над пораженным суставом;
- припухание и боль в первом плюснефаланговом суставе;
- поражение первого плюснефалангового сустава с одной стороны;
- поражение суставов стопы с одной стороны;
- тофусы и образования, напоминающие их;
- лабораторные изменения (повышение уровня мочевой кислоты в крови);
- несимметричный отек суставов;
- кисты под кортикальным слоем кости без эрозий на рентгенографии;
- стерильная синовиальная жидкость.[13]
При пункции врач получает синовиальную жидкость, в которой под микроскопом обнаруживаются кристаллы моноурата натрия. Они могут обнаруживаться и в тофусе. Диагноз при этом можно установить со стопроцентной вероятностью. Ураты выглядят как иглообразные кристаллы с одним утонченным концом. В отсутствие поляризационного микроскопа диагноз основывается в основном на типичных клинических проявлениях подагры. Острый артрит, болевые ощущения при котором нарастают лавинообразно, появляется отек и покраснение пораженного сустава, является веским поводом подумать о подагре. Рентгенологическое исследование суставов на ранней стадии болезни малоинформативно. Изменения выявляются на поздней стадии. В частности, симптом «пробойника» (субкортикальные кисты) — типичный рентгенологический признак подагры — полезен для диагностики ее тофусных форм. Также при рентгенографии при подагре отсутствует околосуставной остеопороз, редко видим сужение суставной щели, часто выявляется остеолиз.[11]
Дифференциальная диагностика:
- гнойный артрит;
- болезнь отложения кристаллов пирофосфата кальция дигидрата;
- ревматоидный артрит;
- реактивный артрит;
- псориатический артрит;
- остеоартроз.
Стоит обратить внимание на то, что во время приступа уровень содержания мочевой кислоты в крови может быть нормальным, так как она в этот момент усиленно выводится почками. На ее уровень в крови не следует ориентироваться при постановке диагноза.
Лечение подагры
Нелекарственные методы:
- соблюдение диеты;
- ограничение употребления алкоголя;
- уменьшение избыточного веса.
Диета при подагре является довольно строгой, но выполнение диетических рекомендаций является залогом успешного лечения. Продукты, которые богаты пуринами, подлежат исключению или минимизации. Обильное щелочное питье помогает почкам избавиться от избытка мочевой кислоты в крови (почки — единственный орган, выводящий мочевую кислоту).
Начнем с главного источника пуринов — птицы и мяса. Курица — один из самых вредных видов птицы. Курице немного уступают (содержат меньше пуринов) утка и гусь. Индейка замыкает список, обладая самым низким содержанием пуринов среди птицы. Говядина — лидер среди мясных продуктов по содержанию пуринов, далее идут телятина и свинина, баранина.
Что касается рыбы, то самые вредные — лососевые виды, далее шпроты, килька, сардины, треска. Морские обитатели, живущие в раковинах (устрицы), являются самыми богатыми на пурины. Субпродукты также очень вредны (мозги, печень, легкие, почки), так же, как и холодец, мясные бульоны и соусы. Колбасу (любую) стоит полностью исключить из рациона. Не рекомендуются также: грибы и грибные бульоны, бобовые, щавель, яйца, шоколад, дрожжи, рис полированный, инжир, геркулес, капуста цветная, дрожжи. Алкогольные напитки запрещены (особое внимание пиву, вину, шампанскому).
Объем употребляемой за сутки жидкости — 2-2,5 литра. Рекомендовано щелочное питье: щелочная минеральная вода, вода с добавлением лимона, соки.
Теперь о бедных пуринами продуктах — как раз о тех, которые необходимо есть. Ими являются: молоко и молочные, молочнокислые продукты, многие овощи (капуста белокочанная, картофель, огурцы, помидоры, морковь, лук), орехи, фрукты, мучные изделия, крупы, мед, масло сливочное. Отварное мясо и рыбу рекомендуется есть 2-3 раза в неделю. Можно есть сало, так как жир почти не содержит пуринов. Некоторые исследования свидетельствуют, что 1,5 литра кофе в день приравнивается к 100 мг аллопуринола, а таккже известно, что вишня и черешня обладают гипоурикемическим действием.[4][15]
Лекарственные методы
Лечение приступа подагры:
- колхицин и нестероидные противовоспалительные препараты — это первое, чем стоит лечить приступ подагры. Колхицин является растительным препаратом (производное безвременника). При приеме колхицина довольно часто возникают побочные эффекты (рвота, жидкий стул, сильный дискомфорт в животе, синдром мальабсорбции, геморрагический энтероколит, редко возникает миелосупрессия и гиперкоагуляция), поэтому стоит строго придерживаться рекомендуемых дозировок. Нестероидные противовоспалительные препараты (ацеклофенак, нимесулид, диклофенак, эторикоксиб) стоит принимать в максимальных терапевтических дозировках — меньшие могут быть неэффективны. Анальгетики при подагре неэффективны;
- глюкокортикоиды внутрисуставно, внутрь или парентерально, когда противопоказан колхицин, нестероидные противовоспалительные препараты или же лечение ими неэффективно. Эти препараты дают выраженный эффект, но должны быть назначены только врачом, злоупотребление глюкокортикоидами имеет необратимые последствия (развитие сахарного диабета, неконтролируемая артериальная гипертензия и т. д.);
- канакинумаб (Иларис) — моноклональные антитела к интерлейкину-1, используются у пациентов с частыми приступами (более трех приступов за последний год), которые не могут принимать колхицин и НПВП.[12][20]
Лечение хроничекого подагрического артрита
Чтобы успешно лечить хроническую подагру, нужно предупредить образование и растворить уже имеющиеся кристаллы моноурата натрия, а для этого необходимо поддерживать уровень мочевой кислоты ниже 360 мкмоль/л.
- аллопуринол — урикодепрессор, доза подбирается индивидуально с врачом. При почечной недостаточности доза подбирается под особым контролем. Аллопуринол подлежит отмене во время приступа;[18]
- фебуксостат (аденурик) — используется при неэффективности аллопуринола, выводится печенью, является альтернативой для лечения пациентов с патологией почек;
- бензбромарон — блокирует обратное всасывание мочевой кислоты в канальцах почек и способствует ее выведению через почки и кишечник;
- пеглотиказа — раствор ферментов, который расщепляет подагрические соли, в РФ не зарегистрирован, применятся только при тяжелом течении подагры;
- первое время, для исключения повторных приступов, можно использовать колхицин (0,5-1,0 грамм в сутки).[5][16]
Пациенты подлежат диспансерному наблюдению у врача-ревматолога. Врач определяет периодичность контроля анализов, меняет (увеличивает или уменьшает) дозы получаемых препаратов, занимается лечением приступа. Противоподагрические средства принимаются длительное время. Также к лечению сопутствующей патологии могут быть подключены смежные специалисты (кардиолог, эндокринолог, уролог, нефролог). Пациент может быть госпитализирован в ревматологическое отделение при длительном по времени приступе, неэффективном лечении на амбулаторном этапе, а также для подбора постоянной терапии.
Прогноз. Профилактика
Прогноз зависит от своевременности и успешности начатого лечения, приверженности пациента к лечению, соблюдения диетических рекомендаций. По большей части прогноз благоприятный, но он ухудшается при развитии поражения почек, которое может стать даже причиной смерти пациента.
Строгое соблюдение диеты является основным моментом в профилактике приступов подагры. Необходимо ограничить употребление алкоголя, не принимать некоторые лекарства (мочегонные препараты из группы тиазидов и петлевые мочегонные, неселективные бета-блокаторы, аспирин, никотиновую кислоту, леводопу). Если пациент худеет, то следует опасаться быстрой потери веса. Нужно стараться избегать обезвоживания и тяжелых физических нагрузок, воздействия низких температур. В профилактических целях аллопуринол может быть назначен только пациентам, страдающим онкологическими заболеваниями и получающим химиотерапию.[14]
Источник
