Ревматоидный артрит и артериальная гипертония
 Ревматоидный артрит (РА) – заболевание с доказанно высоким кардиоваскулярным риском. Основными причинами высокой смертности от сердечно-сосудистых осложнений (ССО) у таких больных являются ускоренное прогрессирование атеросклероза, развитие хронической сердечной недостаточности и внезапной сердечной смерти. Риск ишемической болезни сердца (ИБС) и инфаркта миокарда при РА выше в 2 раза, мозгового инсульта – в 1,9 раза, сердечной недостаточности – в 1,8 раза, чем в общей популяции, причем его резкое увеличение отмечается уже в дебюте заболевания. Повышение кардиоваскулярной летальности при РА обусловлено накоплением традиционных факторов риска (ТФР) сердечно-сосудистых заболеваний (ССЗ): артериальной гипертензии (АГ), дислипидемии, курения и т. д.; хроническим воспалением, аутоиммунными нарушениями, составляющими основу патогенеза этого заболевания; побочными эффектами противоревматической терапии и недостаточным вниманием к профилактике ССО со стороны врачей и пациентов. Поэтому разработка эффективных мер по снижению кардиоваскулярного риска у больных РА – актуальная задача современной медицины.
Ревматоидный артрит (РА) – заболевание с доказанно высоким кардиоваскулярным риском. Основными причинами высокой смертности от сердечно-сосудистых осложнений (ССО) у таких больных являются ускоренное прогрессирование атеросклероза, развитие хронической сердечной недостаточности и внезапной сердечной смерти. Риск ишемической болезни сердца (ИБС) и инфаркта миокарда при РА выше в 2 раза, мозгового инсульта – в 1,9 раза, сердечной недостаточности – в 1,8 раза, чем в общей популяции, причем его резкое увеличение отмечается уже в дебюте заболевания. Повышение кардиоваскулярной летальности при РА обусловлено накоплением традиционных факторов риска (ТФР) сердечно-сосудистых заболеваний (ССЗ): артериальной гипертензии (АГ), дислипидемии, курения и т. д.; хроническим воспалением, аутоиммунными нарушениями, составляющими основу патогенеза этого заболевания; побочными эффектами противоревматической терапии и недостаточным вниманием к профилактике ССО со стороны врачей и пациентов. Поэтому разработка эффективных мер по снижению кардиоваскулярного риска у больных РА – актуальная задача современной медицины.
Доказано, что АГ является важнейшим модифицируемым фактором риска не только в общей популяции, но и у больных РА. Наличие АГ в 3–6 раз увеличивает риск развития ССО при РА. Частота АГ при РА в среднем на 50% выше, чем в общей популяции. Отмечено раннее формирование изолированной систолической АГ, наиболее неблагоприятной в плане развития ССО. К возможным причинам повышения АД при РА относят наличие хронического воспаления и аутоиммунных нарушений, составляющих основу патогенеза заболевания, метаболические нарушения, гиподинамию, генетические факторы и использование противоревматических препаратов с потенциально гипертензивными эффектами. Диагностика АГ должна соответствовать рекомендациям Российского кардиологического общества (РКО). Важно учитывать, что проведение суточного мониторирования АД (СМАД) значительно улучшает диагностику АГ у больных РА. Так, по нашим данным, диагноз АГ на основании опроса, медицинской документации и измерения АД на двух руках был установлен у 20% больных ранним РА, тогда как с учетом результатов СМАД – у 64%. При этом у подавляющего большинства больных уже была АГ II стадии (с поражением органов-мишеней) или III стадии (с наличием ассоциированных клинических состояний: ИБС, инфаркт миокарда/мозговой инсульт в анамнезе). Такая катастрофическая разница между обычным осмотром больного и результатами СМАД может быть связана с особенностями суточного профиля АД при РА. К ним относят увеличение пульсового АД, рост вариабельности АД и повышение частоты таких прогностически неблагоприятных типов суточного профиля АД, как «нон-диппер» (АД не снижается в ночные часы) и «найт-пикер» (АД в ночные часы выше, чем днем), особенно на фоне высокой активности заболевания и лечения глюкокортикоидами (ГК), нестероидными противовоспалительными препаратами (НПВП).
АГ в качестве единственного фактора риска встречается лишь у 7% больных РА. У подавляющего же большинства пациентов она выявляется в сочетании с другими факторами риска (дислипидемией, висцеральным ожирением, курением и др.), что повышает вероятность поражения органов-мишеней (атеросклероз, гипертрофия и ремоделирование миокарда левого желудочка), поэтому необходимо проводить одновременный скрининг всех ТФР ССЗ.
С одной стороны, эффективная противовоспалительная терапия занимает важное место в профилактике ССО и АГ, с другой – большинство препаратов, рутинно используемых для лечения РА, могут вызывать АГ или препятствовать ее эффективному контролю (НПВП, ГК, некоторые базисные противовоспалительные препараты). Использование лефлуномида при РА ассоциируется со снижением вероятности ССО, но риск их развития в 2 раза выше, чем при лечении метотрексатом. АГ, ассоциированная с лефлуномидом, выявляется у 2–10% больных РА. К механизмам повышения АД на фоне приема лефлуномида относят усугубление гиперсимпатикотонии и повышение влияния НПВП на почечный кровоток. Необходимо учитывать, что длительное (более 2 лет) применение даже низких доз ГК (4–6 мг) увеличивает риск развития АГ на 30%, более 5 лет – на 37%, а инфаркта миокарда – на 16%. Доказано 5-кратное возрастание риска ССО у больных, получающих ГК в дозе >7,5 мг/сут. Нужно сказать о генноинженерных биологических препаратах: все препараты этой группы могут вызывать инфузионные реакции в виде гипо- и гипертонии. Наши клинические наблюдения свидетельствуют о том, что в некоторых случаях повышение АД на фоне инфузий инфликсимаба, ритуксимаба и тоцилизумаба бывает очень выраженным, сопровождается ангинозными приступами и требует проведения интенсивной терапии.
Как обстоят дела с лечением АГ у больных РА? Процент больных РА, информированных о наличии у них АГ, получающих гипотензивную терапию и эффективно контролирующих АД, в 1,5 раза ниже, чем в общей популяции. Отсутствие эффективного контроля АГ при РА вдвойне печально, так как пациентов регулярно госпитализируют, они часто посещают ревматолога, т. е. имеют возможность следить за АД. Крайне важно, что АГ чаще не диагностируется у молодых больных РА, у которых как раз можно ожидать наибольшую пользу от ранней идентификации АГ и ее лечения. А эффективный контроль АД, как правило, отсутствует у пожилых больных, вероятно, в связи с наличием коморбидных состояний и низкой приверженностью лечению вследствие полипрагмазии.
 Согласно рекомендациям EULAR, лечение АГ при РА должно проводиться ревматологом, и только в сложных ситуациях (наличие хронической сердечной недостаточности, инфаркта миокарда и/или инсульта в анамнезе, сахарного диабета, хронической почечной недостаточности) показана консультация кардиолога. При ССЗ тактика ведения аналогична таковой у пациентов без ревматического заболевания. Если у больного РА нет доказанных ССЗ, то необходимо оценить суммарный кардиоваскулярный риск по шкале SCORE. По рекомендациям EULAR, при использовании шкалы SCORE у больных РА определяют соотношение уровня холестерина (ХС) и ХС липопротеинов высокой плотности. Модели подсчета должны быть адаптированы для больных РА: риск увеличивается в 1,5 раза при наличии 2 из 3 перечисленных факторов: длительность заболевания более 10 лет; ревматоидный фактор/антитела к антицитруллинированному пептиду – позитивность; наличие внесуставных проявлений (www.scardio.org). К сожалению, шкалы, основанные на учете ТФР, даже при введении поправочного коэффициента, не всегда позволяют объективно оценить кардиоваскулярный риск у больных РА. Поэтому систему стратификации риска ССО по шкале SCORE целесообразно использовать как предварительную с последующим уточнением величины риска после проведения дополнительного обследования (оценка поражения органов-мишеней).
Согласно рекомендациям EULAR, лечение АГ при РА должно проводиться ревматологом, и только в сложных ситуациях (наличие хронической сердечной недостаточности, инфаркта миокарда и/или инсульта в анамнезе, сахарного диабета, хронической почечной недостаточности) показана консультация кардиолога. При ССЗ тактика ведения аналогична таковой у пациентов без ревматического заболевания. Если у больного РА нет доказанных ССЗ, то необходимо оценить суммарный кардиоваскулярный риск по шкале SCORE. По рекомендациям EULAR, при использовании шкалы SCORE у больных РА определяют соотношение уровня холестерина (ХС) и ХС липопротеинов высокой плотности. Модели подсчета должны быть адаптированы для больных РА: риск увеличивается в 1,5 раза при наличии 2 из 3 перечисленных факторов: длительность заболевания более 10 лет; ревматоидный фактор/антитела к антицитруллинированному пептиду – позитивность; наличие внесуставных проявлений (www.scardio.org). К сожалению, шкалы, основанные на учете ТФР, даже при введении поправочного коэффициента, не всегда позволяют объективно оценить кардиоваскулярный риск у больных РА. Поэтому систему стратификации риска ССО по шкале SCORE целесообразно использовать как предварительную с последующим уточнением величины риска после проведения дополнительного обследования (оценка поражения органов-мишеней).
Основная цель лечения больных АГ – максимальное снижение риска развития ССО и смерти от них. Для этого требуется снижение АД до целевого уровня, коррекция всех модифицируемых факторов риска (курение, дислипидемия, гипергликемия, ожирение), предупреждение, замедление темпа прогрессирования и/или уменьшение поражения органов-мишеней, лечение ассоциированных и сопутствующих заболеваний (ИБС, сахарный диабет).
При необходимости коррекции АД у больного РА на первом месте, как и в общей популяции, стоят немедикаментозные меры профилактики, которые включают отказ от курения; нормализацию массы тела (поддержание индекса массы тела на уровне 20–23 кг/м2, объема талии <80 см для женщин и <94 см для мужчин); увеличение физической активности; изменение режима питания. Немедикаментозная профилактика способствует также более эффективному контролю воспалительной активности при РА.
 Коррекция АГ с достижением целевого уровня АД должна проводиться согласно рекомендациям РКО. Но, учитывая высокий риск развития ССО при РА, целесообразно раннее назначение гипотензивной терапии. Как известно, основная польза гипотензивной терапии – снижение АД, независимо от класса используемых препаратов. Согласно рекомендациям EULAR, ингибиторы ангиотензинпревращающего фермента (иАПФ) и антагонисты рецепторов ангиотензина II (АРА) являются препаратами первой линии для лечения АГ при РА. Помимо эффективности при лечении АГ, хронической сердечной недостаточности и почечной патологии, иАПФ и АРА способны замедлять прогрессирование атеросклероза, оказывать противовоспалительное действие, уменьшать гиперсимпатикотонию. АРА повышают чувствительность периферических тканей к инсулину. Но в настоящее время получены данные о наличии плеотропных эффектов и у других классов гипотензивных препаратов. Так, β-адреноблокаторы (БАБ) 3-го поколения не только уменьшают гиперсимпатикотонию, но и улучшают эндотелиальную функцию, снижают перекисное окисление липидов, уровень общего ХС, триглицеридов и глюкозы. Но следует помнить о снижении гипотензивного эффекта БАБ, иАПФ и АРА на фоне одновременного приема с НПВП. Антагонисты кальция также занимают важное место в лечении АГ у больных РА. Они метаболически нейтральны, что позволяет назначать их при метаболическом синдроме и/или сахарном диабете, способствуют уменьшению симптомов при болезни/синдроме Рейно и не взаимодействуют с НПВП.
Коррекция АГ с достижением целевого уровня АД должна проводиться согласно рекомендациям РКО. Но, учитывая высокий риск развития ССО при РА, целесообразно раннее назначение гипотензивной терапии. Как известно, основная польза гипотензивной терапии – снижение АД, независимо от класса используемых препаратов. Согласно рекомендациям EULAR, ингибиторы ангиотензинпревращающего фермента (иАПФ) и антагонисты рецепторов ангиотензина II (АРА) являются препаратами первой линии для лечения АГ при РА. Помимо эффективности при лечении АГ, хронической сердечной недостаточности и почечной патологии, иАПФ и АРА способны замедлять прогрессирование атеросклероза, оказывать противовоспалительное действие, уменьшать гиперсимпатикотонию. АРА повышают чувствительность периферических тканей к инсулину. Но в настоящее время получены данные о наличии плеотропных эффектов и у других классов гипотензивных препаратов. Так, β-адреноблокаторы (БАБ) 3-го поколения не только уменьшают гиперсимпатикотонию, но и улучшают эндотелиальную функцию, снижают перекисное окисление липидов, уровень общего ХС, триглицеридов и глюкозы. Но следует помнить о снижении гипотензивного эффекта БАБ, иАПФ и АРА на фоне одновременного приема с НПВП. Антагонисты кальция также занимают важное место в лечении АГ у больных РА. Они метаболически нейтральны, что позволяет назначать их при метаболическом синдроме и/или сахарном диабете, способствуют уменьшению симптомов при болезни/синдроме Рейно и не взаимодействуют с НПВП.
Таким образом, диагностика АГ должна осуществляться согласно рекомендациям РКО. У пациентов с РА, имеющих ≥2 ТФР ССЗ, высокую активность заболевания, длительность РА более 5 лет, принимающих НПВП, ГК, лефлуномид, необходимо более углубленное обследование, направленное на выявление субклинических признаков поражения сердечно-сосудистой системы. Ведение пациента с РА и АГ должно включать устранение возможных причин повышения АД (НПВП, ГК, лефлуномид), рекомендации по изменению образа жизни, решение вопроса о необходимости назначения гипотензивной терапии, статинов и антиагрегантов согласно стратификации риска ССО. Если необходим одновременный прием аспирина и НПВП, следует минимизировать их дозу, использовать ингибиторы протонной помпы. Необходимо динамическое наблюдение за пациентами с РА и АГ. Рекомендуется систематический контроль АД при каждом обращении к ревматологу (не реже 1 раза в 6 мес). При развитии АГ проводят ежемесячный контроль АД до достижения целевых значений. При назначении терапии НПВП или ГК важен ежемесячный контроль АД в течение первых 6 мес, по возможности нужно минимизировать дозу и длительность приема как ГК, так и НПВП. При каждом визите к ревматологу, независимо от наличия у пациента АГ, необходим пересмотр антиревматических препаратов, обладающих потенциальными гипертензивными эффектами.
РА, как и сахарный диабет, относят к заболеваниям с доказанно высоким кардиоваскулярным риском. Если при сахарном диабете стратегия агрессивного скрининга и лечения ССЗ привела к значительному снижению ССО, то при РА решению данной проблемы не уделяется должного внимания. Высокая частота АГ при РА требует проведения агрессивного скрининга и тщательного контроля АД с более низким порогом назначения гипотензивной терапии.
Д.м.н. Д.С. Новикова, старший научный сотрудник лаборатории функциональной и ультразвуковой диагностики,
д.м.н. Т.В. Попкова, руководитель лаборатории системных ревматических заболеваний с группой гемореологических нарушений
ФГБУ «НИИР им. В.А. Насоновой» РАМН
Источник
- Авторы
- Резюме
- Файлы
- Ключевые слова
- Литература
Громова М.А.
1
Мясоедова С.Е.
1
1 ГБОУ ВПО «Ивановская государственная медицинская академия» Минздрава России
Обследован 101 пациент с достоверным диагнозом ревматоидный артрит (РА), средний возраст 61 год, 92 % женщин. Средняя продолжительность РА – 7 лет. Серопозитивный вариант был у 67 %, системные проявления – у 18 %. Всем больным регистрировали артериальное давление (АД), скорость распространения пульсовой волны (СРПВ), вариабельность ритма сердца (ВРС); оценивали выраженность болевого синдрома по визуальной аналоговой шкале, анкете Ван – Корфа, Мак-Гилловскому болевому опроснику, опроснику нейропатической боли DN4. Артериальная гипертензия 1–3 степени выявляется более чем у половины больных РА, у большинства из них она возникает на фоне РА, у пациентов более старшего возраста и с абдоминальным ожирением. Подъемы систолического и пульсового АД, изменения ВРС и СРПВ коррелировали с характеристиками хронического болевого синдрома.
хронический болевой синдром
артериальная гипертензия
ревматоидный артрит
скорость распространения пульсовой волны
вариабельность ритма сердца
1. Мясоедова Е.Е. Распространенность и факторы риска артериальной гипертензии при ревматоидном артрите // Научно-практическая ревматология. – 2012. – № 2. – С. 31–34.
2. Новикова Д.С., Попкова Т.В., Насонов Е.Л. Современные представления о патогенезе и особенности лечения артериальной гипертензии при ревматоидном артрите (обзор) // Тер. арх. – 2011. – № 5. – С. 24–33.
3. Попкова Т.В. Кардиоваскулярные факторы риска при ревматических заболеваниях: связь с воспалением // Consilium medicum. – 2010. – № 12. – С. 112–8.
4. Ревматология: клинические рекомендации; под ред. акад. РАМН Е.Л. Насонова. – 2-е изд., испр. и доп. – М.: ГЭОТАР-Медиа, 2010. – 752 с.
5. Gonzalez A., Maradit Kremers H., et al. The widening mortality gap between rheumatoid arthritis patients and the general population // Rheumatoid arthritis. – 2007. – № 56(11). – Р. 3583–7.
6. Maradit-Kremers H., Nicola P.J., Crowson C.S., Gabriel S.E. Cardiovascular death in rheumatoid arthritis: a population-based study // Rheumatoid arthritis. – 2005. – № 52(3). – Р. 722–32.
Ревматоидный артрит (РА) – аутоиммунное ревматическое заболевание неизвестной этиологии, характеризующееся хроническим эрозивным артритом (синовитом) и системным воспалительным поражением внутренних органов [4]. Доказано, что кардиоваскулярный риск при ревматоидном артрите (РА) значительно увеличен по сравнению с общей популяцией [5, 6]. Однако механизмы кардиоваскулярных заболеваний у больных РА до конца не изучены. Артериальная гипертензия является одним из наиболее распространенных факторов риска, имеет мультифакторный генез при РА, обусловленный вкладом традиционных факторов риска АГ и характеристик основного заболевания, и ассоциирована с неблагоприятным прогнозом в отношении кардиоваскулярных заболеваний и смерти от кардиоваскулярных причин [1, 2, 3]. Также остается неизученным вопрос о роли хронического болевого синдрома (ХБС) в изменениях уровней артериального давления и в развитии функциональных изменений сердечно-сосудистой системы у больных РА.
Цель работы: оценить влияние ХБС на уровень артериального давления (АД) и функциональные нарушения сердечно-сосудистой системы у больных РА.
Материал и методы исследования
Обследован 101 пациент с достоверным диагнозом РА, в возрасте от 32 до 75 лет (средний возраст 60,6 лет), большинство из них – женщины (92 %). Средний возраст начала РА составил 54 года. Средняя продолжительность РА – 6,7 лет. Серопозитивный вариант был у 67 %, системные проявления – у 18 %. У большинства наблюдалась 2–3 степень активности, II–III функциональный класс (ФК). У 96 % больных выявлен эрозивный артрит. В лечении РА использовали метотрексат в сочетании с селективными нестероидными противовоспалительными препаратами, 37,6 % больных получали глюкокортикоиды. Антигипертензивная терапия включала комбинации ингибиторов ангиотензинпревращающего фермента или блокаторов рецепторов ангиотензина II с диуретиками, антагонистами кальция и бета-блокаторами. Диагностика АГ осуществлялась с учетом Национальных рекомендаций по диагностике и лечению АГ (2010 г.), степень и динамика АГ оценивалась по данным амбулаторной карты и при офисном измерении АД на момент обследования. Рассчитывали SCORE для стран высокого риска с поправкой Европейской антиревматической лиги от 2008 г., учитывающей длительность РА более 10 лет, положительный результат теста на ревматоидный фактор или антитела к циклическому цитруллинированному пептиду, наличие внесуставных проявлений. Для определения характера и выраженности хронического болевого синдрома применяли следующие методы: визуальная аналоговая шкала (ВАШ); анкета Ван-Корфа для оценки степени выраженности хронического болевого синдрома (с оценкой интенсивности болевого синдрома, степени и уровня социальной дезадаптации, класса хронической боли); Мак-Гилловский болевой опросник (с оценкой боли по сенсорной, аффективной, эвалютивной шкалам); диагностический опросник нейропатической боли DN4 для количественной оценки степени выраженности нейропатической боли. Регистрировали скорость распространения пульсовой волны (СРПВ) по сосудам эластического и мышечного типов и проводили анализ вариабельности ритма сердца (ВРС) в покое и при активной ортостатической пробе (аппаратура ООО «Нейрософт», Иваново). Статистическая обработка проводилась с использованием методов описательной статистики, непараметрического, корреляционного анализа в программе Statistica 6.0.
Результаты исследования и их обсуждение
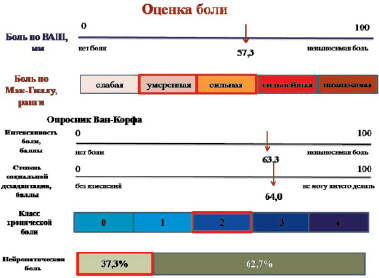
Боль по результатам опросников варьировала по интенсивности, в среднем по ВАШ составила 57,3 ± 20,1 мм. По данным Мак-Гилловского болевого опросника у 71 % пациентов наблюдалась умеренная и сильная боль. Боль по результатам анкеты Ван-Корфа: характеризовалась высокой интенсивностью (63,3 ± 20,4 %), средним уровнем дезадаптации (64 %) и легкой нетрудоспособностью, что соответствовало 2 классу хронической боли. Нейропатический компонент боли по данным опросника DN 4 выявлен у 37 % пациентов (рисунок).

Характеристика боли по опросникам
Анализ взаимосвязей ХБС с различными параметрами РА показал, что выраженность боли не связана с показателем активности РА по DAS28 и отдельными параметрами активности РА, включенным в DAS28 (число болезненных и припухших суставов, СОЭ), но коррелировала с общим числом пораженных суставов (r = 0,48) и оценкой состояния здоровья пациентом (r = 0,45). Интенсивность боли нарастала по мере увеличения продолжительности заболевания (r = 0,3).
Артериальная гипертензия 1–3 степени выявлена у 64,35 % больных, средняя длительность анамнеза составила 7,5 лет. У 55,4 % больных АГ возникла на фоне РА. Почти у всех пациентов отмечено сочетание 2 и более общепопуляционных факторов риска (возраст, отягощенная наследственность по сердечно-сосудистым заболеваниям, гиперхолестеринемия, абдоминальное ожирение). 10-летний риск смерти по SCORE равен 2,5 ± 2,48, что соответствует низкому риску у большинства больных, высокий риск отмечен у 9,9 % пациентов. При этом у 66,3 % пациентов РА, в том числе у 90 % пациентов с низким и средним риском SCORE, были выявлены поражения органов-мишеней, главным образом гипертрофия левого желудочка. СРПВ > 10 м/с отмечена у 26,7 % пациентов. Систолическое АД коррелировало с возрастом (r = 0,48) и объемом талии (r = 0,31), диастолическое – с возрастом (r = 0,48), объемом талии (r = 0,27), гиперхолестеринемией (r = 0,23); пульсовое – с объемом талии (r = 0,21). Уровни АД не коррелировали с показателями активности РА. Вместе с тем выявлена зависимость между интенсивностью боли и пульсовым АД (r = 0,4), а также максимальными цифрами систолического АД (r = 0,25). Выраженность боли по ВАШ, класс хронической боли, ее интенсивность, степень дезадаптации были взаимосвязаны с уменьшением общей мощности спектра ВРС и снижением активности парасимпатического отдела. Указанные параметры боли имели отрицательную связь с отношением СРПВ по сосудам мышечного типа к СРПВ по сосудам эластического типа, что отражает увеличение жесткости сосудов. Отношение СРПВ по сосудам мышечного типа к СРПВ по сосудам эластического типа наиболее тесно коррелировало с наличием нейропатического компонента боли (r = –0,4).
Выводы
АГ 1–3 степени выявляется более чем у половины больных РА и у большинства из них возникает на фоне РА, наиболее тесно связана с возрастом и абдоминальным ожирением и сочетается с субклиническим поражением сердца и сосудов. Уровни АД не коррелировали с активностью РА. Подъемы систолического и пульсового АД, изменения ВРС и увеличение жесткости сосудистой стенки были связаны с различными характеристиками боли, что требует большего внимания к ее оценке и коррекции.
Рецензенты:
Ушакова С.Е., д.м.н., доцент, заведующая кафедрой поликлинической терапии и эндокринологии, ГБОУ ВПО «Ивановская государственная медицинская академия» Минздрава России, г. Иваново;
Королева С.В., д.м.н., доцент, профессор кафедры гражданской защиты и управления в чрезвычайных ситуациях, ФГБОУ ВПО «Ивановский институт Государственной противопожарной службы Министерства Российской Федерации по делам гражданской обороны, чрезвычайным ситуациям и ликвидации последствий стихийных бедствий», г. Иваново.
Работа поступила в редакцию 30.09.2014.
Библиографическая ссылка
Громова М.А., Мясоедова С.Е. АРТЕРИАЛЬНАЯ ГИПЕРТЕНЗИЯ, СОСТОЯНИЕ СЕРДЕЧНО-СОСУДИСТОЙ СИСТЕМЫ И ХАРАКТЕРИСТИКА БОЛИ У БОЛЬНЫХ РЕВМАТОИДНЫМ АРТРИТОМ // Фундаментальные исследования. – 2014. – № 10-4. – С. 651-653;
URL: https://fundamental-research.ru/ru/article/view?id=35597 (дата обращения: 19.07.2020).
Предлагаем вашему вниманию журналы, издающиеся в издательстве «Академия Естествознания»
(Высокий импакт-фактор РИНЦ, тематика журналов охватывает все научные направления)
Источник
