Современные подходы в лечении остеопороза

Остеопороз – это системное заболевание, при котором процессы разрушения костной ткани превалируют над ее возможностями к регенерации и укреплению. При этом происходит вымывание солей кальция из костей, так как они становятся не в состоянии их удерживать внутри. Как итог, повышенная хрупкость костей, высокая склонность к переломам, которые случаются даже при незначительном воздействии извне. Это может быть обычный ушиб, неосторожное движение, падение.
Остеопороз – заболевание опасное, способное провоцировать летальный исход. Чаще него гибель и инвалидизация людей происходит только по причине сердечно-сосудистых патологий, сахарного диабета и раковых болезней.
Коварство заболевания заключается еще и в том, что остеопороз развивается с минимальным набором симптомов. Ощущать их больной начинает тогда, когда лечение становится малоэффективным – это та стадия, во время которой часто возникают переломы.
Узнайте больше: Переломы — виды переломов, фазы срастания
Содержание:
- Факторы, влияющие на развитие остеопороза
- Методы диагностики
- Лечение остеопороза
- Симптоматическое лечение остеопороза
- Лечение остеопороза в домашних условиях
- Меры профилактики
Факторы, влияющие на развитие остеопороза
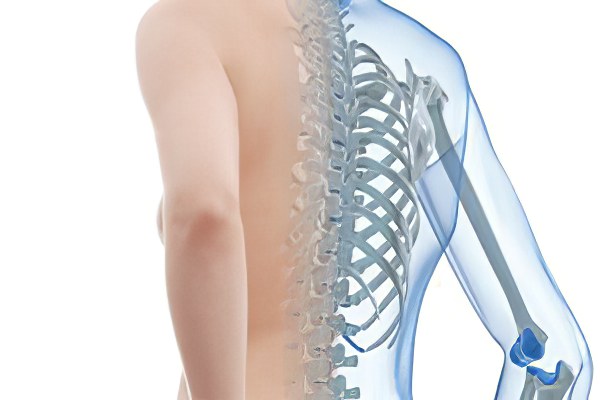
Основные факторы, способствующие развитию остеопороза:
Нехватка кальция в организме по причине погрешностей в питании. Это может быть несбалансированный рацион, приверженность разнообразным диетам, голодание и пр. Недостаток кальция в организме часто провоцируют сбои в процессе всасывания витаминов и микроэлементов.
Гиподинамия. Длительное нахождение в лежачем, обездвиженном положении приводит к тому, что в организме активизируются остеокласты. Они разрушают костную ткань, нарушают ее минерализацией. Опасно в этом плане длительное пребывание в состоянии невесомости. В связи с этим, люди, у которых диагностирован остеопороз, должны поддерживать постоянную физическую активность.
Нарушения гормонального фона. Заболевание может развиваться по причине любого гормонального дисбаланса – это сбои в процессе выработки гормонов щитовидной, паращитавидной железы, половых гормонов и гормонов гипофиза.
Вторичный остеопороз может развиваться при избыточном употреблении спиртных напитков, кофе, при наличии такое вредной привычки как курение, а также на фоне болезней крови, на фоне ревматизма, почечной недостаточности, сахарного диабета.
Если человек употребляет слишком много газированной воды, то болезнь костной ткани может развиться у него даже в молодом возрасте. Доказано, что в большей части газированных напитков содержатся вещества, которые способствуют вымыванию кальция из костей.
Еще одна причина развития остеопороза – это нарушения в работе системы пищеварения, в функционировании сердечно-сосудистой системы.
Болезни позвоночника развиваются преимущественно в пожилом возрасте, после 60 лет. Женщины страдают чаще мужчин, болезнь выявляется у них после наступления климакса. У мужского населения кальций в костях сохраняется дольше, его возрастная потеря наступает несколько позже.
Основными симптомами болезни принято считать:
Нарушения в структуре костей, что приводит к их деформации.
Сутулость, потеря в росте из-за искривления позвоночника, пародонтоз.
Нарушения подвижности суставов, как крупных, так и мелких. Привычные физические нагрузки приводят к быстрой утомляемости.
В ночные часы больного могут беспокоить судороги, возникающие в голени. Возможны тупые боли ноющего характера, либо острые боли в позвоночном столбе и в суставах. Особенно интенсивными болезненные ощущения становятся во время смены погоды.
Остановить развитие остеопороза невозможно, он является обязательным спутником старения всего организма. Предотвратить вымывание кальция из костей можно лишь в том случае, когда оно вызвано иной патологией. Однако, это не означает, что замедлить скорость развития заболевания нельзя. Грамотно выстроенная схема лечения позволяет исключить развитие осложнений.
Методы диагностики
Рентгенологическое исследование является самым частым методом диагностики заболевания. Однако, оно информативно лишь в том случае, когда произошла потеря более чем 30% костной массы. Лечить такого больного нужно долго, а эффект не всегда бывает достигнут.
Компьютерная томография. С помощью томографа можно выявить заболевание на ранней стадии его развития. Для этого приборы оснащены специальной приставкой. Также выявить заболевание помогает аппарат ультразвукового исследования. Но одномоментно удается с помощью этих устройств изучить состояние лишь одного участка тела. В то время как для оценки степени распространения патологического процесса необходимо исследовать несколько отделов.
Остеодистрофия. Современная медицина располагает рентгеновскими денсиметрами, благодаря которым можно оценить минеральную плотность костной ткани сразу на нескольких участках тела. Причем точность такого исследования является высокой. Удается отследить даже 2% потерю костной массы, а также выявить уровень мышечной массы и жира в организме, содержания кальция в костях. Эти данные соотносятся с возрастом и половой принадлежностью пациента. Денситометрическое исследование безопасно для здоровья, проводится быстро и не вызывает болезненных ощущений. Побочных эффектов после диагностики не возникает, поэтому делать ее можно столько раз, сколько потребуется.
Тем не менее, причину по которой происходит потеря костной массы установить с помощью этих методик невозможно. Сделать это в состоянии только лечащий врач.
Кроме опроса и осмотра пациента, он направит его на сдачу следующих анализов:
Мочу нужно сдать для определения в ней электролитов;
Забор крови позволяет выявить уровень кальция, витамина Д и фосфора в ней;
Требуется определение уровня остеокальцина;
Изучаются выделительные возможности почек;
Сдается кровь на паратгормон.
Эти исследования, проведенные в комплексе, позволяют составить максимально полную картину болезни и назначить подходящее лечение.
Лечение остеопороза

Методы лечения остеопороза напрямую зависят от того, какой характер имеет заболевание. Если оно возникает как вторичная патология, то потребуется устранение первопричины болезни – это может быть коррекция иммунных нарушений, болезней сердечно-сосудистой и пищеварительной системы и пр.
Первичный остеопороз формируется из-за старения организма и чаще всего возникает у женщин. Лечение требует особого подхода, так как чаще всего болезнь диагностируется в период после менопаузы. Нужно максимально замедлить вымывание кальция из костей и усилить его наращивание. При этом учесть нужно то, какие изменения произошли в синтезе половых гормонов.
Терапия делится на следующие составляющие:
Базовое лечение с приемом лекарственных препаратов. Его целью является коррекция обменных процессов в костях. Лечение длительное, непрерывное, поэтапное.
Гормонозаместительная терапия.
Симптоматическая терапия.
Операцию проводят при остеопорозе тазобедренного и коленного сустава. Если консервативная терапия оказывается безрезультатной, то показано эндопротезирование изношенного сустава на искусственный. Это способствует улучшению качества жизни больных, ее продлению, так как исключает риск спонтанного перелома шейки бедра.
Основное лечение остеопороза
Для лечения остеопороза назначают регуляторы кальциево-фосфорного обмена.
Эти препараты заменяют собой работу гормонов паращитовидной железы:
Кальцитонины (Миакальцик). Предотвращает потерю кальция из костей гормон кальцитонин, он также принимает участите в процессе их формирования, обладает обезболивающим эффектом. Лекарственное средство изготавливается из кальцитонина лосося и действует аналогично собственному гормону человека. С этой целью могут применяться такие препараты, как: Остеовер, Алостин, Вепрена.
Препараты-бисфосфонаты направлены на торможение процесса потери костной массы, нормализуют минерализацию костей. Возможно назначение следующих средств: Ризедронат, Алендронат, Ибандронат, Золедроновая кислота (Ксидифон, Этидронат, Бонефос, Фосамакс).
Комплексный препарат Остеогенон препятствует разрушению костной ткани (подавляет синтез остеокластов и стимулирует работу остеобластов), способствует процессу формирования костей.
На стимуляцию формирования костной ткани направлены производные фтора – это Кальцик, Флюокальцик, Осин, Кореберон.
Для стимуляции остеобластов используется паратиреоидный гормон терипаратид – Форстео. Его нужно вводить в виде инъекций.
Все эти препараты может назначить только врач, который будет контролировать кровь, мочу методами лабораторной диагностики. Это позволит оценить эффективность лечения.
Разрушения костей не происходит |
|
Костная ткань образуется нормально | Уровень остеокальцина в крови в возрасте до 50 лет составляет от 11 до 23 нг/мл. В возрасте после 50 лет – от 15 до 46 нг/мл. |
Норма содержания солей (ммоль/л) |
|
Гормонозаместительная терапия
Терапия с помощью гормональных препаратов применяется очень часто. Ее назначают людям с выраженным остеопорозом, с заболеванием на ранних стадиях его развития и даже тем пациентам, у которых имеются только лишь предпосылки для развития патологии. Для женщины, вступивших в менопаузальный период назначают определенные модуляторы эстрогеновых рецепторов. Это такие препараты, как Ралоксифен, Кеоксифен, Эвиста, Дролоксифен. Их прием помогает остановить процесс разрушения костей, либо значительно его замедлить. Риск переломов при этом уменьшается ровно в половину.
Возможно назначение самих эстрогенов, например, препаратов Фемостон, Клиогест, в комплексе с препаратами кальция. Но следует помнить, что прием эстрогенсодержащих средств влияет на риск развития онкологических болезней гинекологического плана. Чтобы достигнуть эффекта, потребуется принимать эстрогены, как минимум, 5 лет. Параллельно контролируется уровень гормонов в крови. Отмену препаратов производят поэтапно, уменьшая дозу медленно.
Нельзя принимать эстрогены тем пациентам, которые находятся в группе риска по онкологическим болезням, а также тем больным, у которых есть склонность к тромботическим осложнениям. К тому же гормональная терапия эстрогенами относится к поддерживающей терапии и не способна восполнить уровень кальции в костях.
Препараты кальция при остеопорозе

Чтобы остановить развитие болезни, нужно использовать препараты кальция. Они работают намного лучше, чем включение в меню продуктов питания, богатых на этот микроэлемент, либо использование народных методов лечения.
Чтобы повысить эффективность терапии препараты кальция назначают в комплексе с регуляторами кальциевого обмена:
Показан прием поливитаминов – это может быть Элевит, Кальцинова, Комплевит, Нутримакс. Но так как в этих средствах очень много компонентов, всасываются они хуже, чем моно-препараты. Поэтому их используют как профилактические, а не как лечебные средства.
Прием моновитаминов с солями кальция. Сам кальций глюконат усваивается плохо, поэтому лучше всего принимать такие средства, как Глицерофосфат кальция, Лактат кальция, Хлорид кальция.
Возможно назначение комбинированных препаратов в которых кальций сочетается с витамином Д – это может быть Кальций Д3 никомед, Ортокальций в сочетании с цитратом кальция, Витамин Д3 в сочетании с Витрум кальций.
Узнайте больше: Кальций при остеопорозе: какой кальций лучше?
Подобрать средство может только доктор. Если принимать препараты кальция без врачебного контроля, это грозит отложением солей микроэлемента в мягких тканях, что приведет к поражению почек, сердца, сосудов. Особенно опасно самостоятельное использование витамина Д для лечения детей. Неправильные дозировки могут сказаться на проблемах со здоровьем в будущем. Это же касается нерационального использования гормональных средств.
Современный метод лечения остеопороза
Врачи используют качественно новый подход в лечении остеопороза, он сводится к следующим моментам:
Необходимо точно выявить все участки костной ткани, пораженные остеопорозом.
Затем осуществляется очищение лакун костей ударно-волновым методом.
Следующий этап – введение экстракта тканей животных и ионизированного кальция под надкостицу.
Проведение стандартной терапии.
Эта схема лечения остеопороза применима у пациентов любого возраста.
В Окландском университете, находящемся в Новой Зеландии происходило исследование новейшего лекарственного средства, которое должно стать настоящим прорывом в плане лечения остеопороза. Это препарат Зомета, который выпускается Новартис Эй Джи (Швейцария) и представляет собой золедроновую кислоту. Вводить его достаточно 1 раз в год, больше никакой терапии не требуется. На основании исследования, было установлено, что распад костной ткани после введения инъекции замедляется на год, а сама кость становится за это время более плотной. Однако данных относительно предотвращения переломов костей пока нет, но испытания продолжаются.
Симптоматическое лечение остеопороза
Прием анальгетиков и миелорелаксантов при болях и спазмах мышц, прием НПВС при артритах. Это позволяет больному избежать прогрессирования болезни из-за гиподинамии.
Лечение переломов с помощью хирургического вмешательства.
Прохождения физиотерапевтического лечения, выполнение комплексов лечебной физкультуры.
Соблюдение режима питания с включением в меню продуктов, богатых на магний, фосфор кальций.
Отказ от употребления газированных напитков.
Лечение остеопороза в домашних условиях
Обязательно нужно отрегулировать свое меню. Для замедления прогрессирования остеопороза следует включить в него продукты с витамином Д, кальцием, фосфором. Это не только кисломолочные продукты, но и морская капуста, шпинат, брокколи, рыба жирных сортов, бобовые, баклажаны.
Из таблицы становится понятно, сколько кальция содержится в различных продуктах питания. Расчет осуществлен исходя из 100 г продукта.
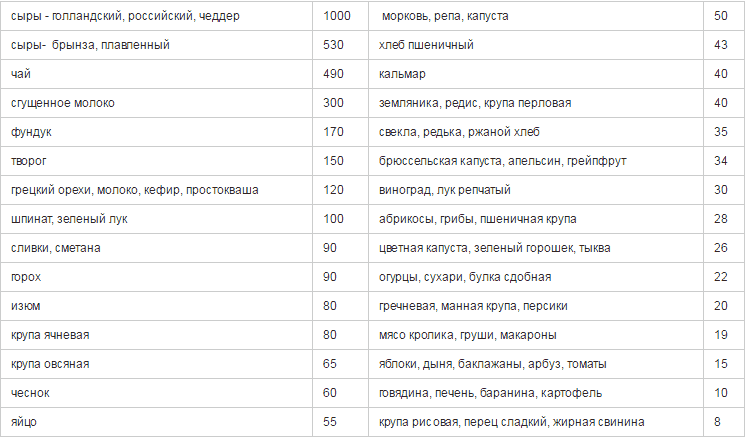
Соли кальция организм усваивает в молодости лишь на 30-35%, а в старости на 10-15%. Дополнительно этому процессу мешает шоколад, чай, кофе и алкоголь.
Если осуществляется лечение препаратами кальция, то параллельно нужно принимать витамин Д. Если этого не делать, то кальций просто выведется из организма почками. Находясь на солнце можно обогатить свой организм этим нужным ему витамином.
Дома можно выполнять физические упражнения, которые назначил врач, делать самостоятельный массаж.
Народная медицина рекомендует употреблять яичную скорлупу, настоянную на лимонном соке. Тем не менее, любые аптечные препараты, которые имеются в свободной продаже, будут намного эффективнее, чем скорлупа куриного яйца.
Меры профилактики
Профилактика остеопороза сводится к выполнению следующих мероприятий:
Мать должна позаботиться о костной системе ребенка еще в то время, пока он находится в ее утробе. Для этого ей нужно принимать витамины, которые рекомендует доктор. В период детства нужно уделять внимание накоплению костной массы, для чего ребенка следует правильно кормить, следить за тем, чтобы он занимался физической культурой, танцами, гимнастикой и пр.
В подростковом и взрослом возрасте нужно избегать вдыхания табачного дыма, употребления алкоголя, сладкой газировки. Половая жизнь должна быть регулярной.
В период менопаузы следует обращаться за квалифицированной врачебной помощью, так как в первые 10 лет после наступления климакса, кальций из костей вымывается особенно быстро.
Важно понимать, что остеопороз – это заболевание, которое вылечить самостоятельно невозможно. Принимать представленную информацию как руководство к самолечению не следует. Она предназначена для того, чтобы люди понимали опасность болезни и не откладывали качественную диагностику. Лечит остеопороз только доктор.
Автор статьи: Кузьмина Вера Валерьевна | Эндокринолог, диетолог
Образование:
Диплом РГМУ им. Н. И. Пирогова по специальности «Лечебное дело» (2004 г.). Ординатура в Московском государственном медико-стоматологическом университете, диплом по специальности «Эндокринология» (2006 г.).
Наши авторы
Источник
Остеопороз (ОП) является не только причиной страданий, инвалидизации, снижения качества жизни и преждевременной смерти пожилых людей, но представляет важнейшую социально–экономическую проблему, которая приоритетна наряду с сердечно–сосудистыми и онкологическими заболеваниями для лиц старших возрастных групп.
ОП – многофакторное заболевание, в основе которого лежат процессы нарушения костного ремоделирования с повышением резорбции костной ткани и снижением костеобразования.
Под влиянием различных факторов, таких как наследственность, расовая принадлежность, питание, физическая активность, вредные привычки, менструальный статус у женщин, прочность кости может снижаться. Четко прослежена наследуемость ОП в поколениях мать–дочь, мать–бабушка, бабушка–мать–дочь [1]. На это же указывает высокая степень корреляции (0.80) минераль¬ной плотности костной массы между гомозиготными близ¬нецами, у которых геномы полностью идентичны. У дизиготных близнецов, чьи геномы теоретически могут быть сходны от 50 до 0%, корреляция (0,20–0,40) существенно ниже [2,3]. Это позволяет обоснованно отнести ОП к генетичес¬ки обусловленным заболеваниям.
Однако, с одной стороны, признается факт наследственной предрасположенности к ОП [2–4,6]. Обсуждается до 32 генов–кандидатов (с помощью методов обратной генетики происходит поиск полиморфизмов в генах, ответственных за метаболизм костной ткани, и установление достоверности ассоциации данного полиморфизма с фенотипическими признаками остеопороза, и ген, отвечающий этому требованию, включают в группу генов–кандидатов остеопороза), детерминирующих достижение определенного пика костной массы к 20 годам, особенности метаболизма костной ткани [4].
С другой стороны, достоверно доказаны для первичного ОП такие «экзогенные» факторы риска, как дефицит потребления белка, кальция и витамина D, курение, злоупотребление алкоголем, гиподинамия, низкая масса тела, ранняя менопауза у женщин [5].
Известно, что у женщин имеется большая склонность к развитию ОП, так как недостаток женских половых гормонов (эстрогенов) после наступления менопаузы способствует снижению секреции кальцитонина, повышению чувствительности кости к резорбтивному действию паратиреоидного гормона, снижению их прямого действия на подавление остеокластов (клеток, способствующих разрушению костной ткани) [7]. У мужчин распространенность ОП в 3 раза меньше, чем у женщин.
Наиболее распространенными формами ОП являются постменопаузальный и сенильный, составляющие до 85% всех вариантов ОП.
Согласно международной классификации, ПМО относится к первичному ОП I типа и характеризуется высоким костным обменом с интенсивными процессами костной резорбции при нормальном или повышенном костеобразовании. Отличительной особенностью ПМО является преимущественное поражение трабекулярной костной ткани. В связи с этим наиболее подверженной областью является позвоночник, состоящий на 95% из трабекулярной кости, и дистальный отдел лучевой кости.
В патогенезе постменопаузального ОП пусковым моментом развития остеопении прежде всего является дефицит эстрогенов [7]. Точный механизм влияния гипоэстрогенемии на снижение массы кости еще до конца не выяснен, однако доказано наличие эстрогенных рецепторов на остеобластах. Дефицит эстрогенов способствует продукции остеобластами фактора, стимулирующего активность остеокластов и их дифференцировку, что обусловливает повышенную резорбцию кости и снижение выработки фактора, ингибирующего резорбцию костной ткани [7–9]. В настоящее время имеются доказательства, что этими веществами являются члены суперсемейства фактора некроза опухоли RANK (активатор рецептора ядерного фактора капа–бега), его лиганд – RANKL и остеопротегерин соответственно [10]. Предполагают, что недостаток эстрогенов способствует снижению секреции кальцитонина и повышенной чувствительности кости к резорбтивному действию паратиреоидного гормона [11]. Остеопротегерин обладает сильной ингибиторной активностью остеокластогенеза [10]. Баланс между RANKL и остеопротегерином фактически определяет количество резорбированной кости.
В настоящее время ОП является моделью для изучения молекулярных механизмов межклеточного взаимодействия [10,12–14].
Так, например, отсутствие гена остеопротегерина у мышей приводило к развитию раннего ОП, переломам позвонков у взрослых особей. Мыши умирали от костных аномалий, кальцификации аорты и почечных артерий. По–видимому, остеопротегерин может предотвращать кальцификацию крупных артерий [10,13].
В ходе другого исследования установлена высокая частота нарушений минеральной плотности костной ткани (71%) у больных с кальцинированным аортальным стенозом дегенеративного генеза [14]. Было показано, что кальциноз аортального клапана у пожилых лиц является самостоятельным фактором, оказывающим неблагоприятное воздействие на состояние костной ткани поясничного отдела позвоночника.
Недавно появились результаты экспериментальных и кли¬нических исследований, свидетельствующие о влиянии ста¬тинов на процессы костного ремоделирования, в частности на стимуляцию костеобразования [15]. С другой стороны, опубликованы работы, свидетельствующие о взаимосвязях уровня липидов и минеральной плотности костной ткани [16].
Изучение механизмов и факторов риска развития вторичного ОП остается в центре внимания многочисленных исследований.
Недавно опубликованный обзор, включающий более 2000 источников за последние 15 лет, показал, что на вторичный ОП приходится более 2/3 случаев у мужчин, более половины у женщин в пре– или перименопаузе и приблизительно одна пятая часть у женщин в постменопаузе [17]. Причины вторичного ОП многочисленны, а потенциальный риск переломов сопоставим с риском при первичном ОП.
Особый интерес представляет проблема развития ОП при ревматоидном артрите. Несмотря на большое число работ по изучению факторов риска ОП при ревматоидном артрите, как общих, так и ассоциированных с самим заболеванием, вклад каждого из них в процесс снижения костной плотности оценить сложно ввиду тесного их взаимодействия и вызывает повышенный интерес ученых [18,19].
В настоящее время принято выделять следующие группы риска развития остеопороза.
• Женщины хрупкого телосложения со светлой кожей, бездетные либо имеющие одного–двух детей, с семейным анамнезом переломов позвоночника или шейки бедра.
• Женщины с ранней или искусственной менопаузой.
• Женщины и мужчины с различными заболеваниями, способными вызвать вторичный остеопороз (болезнь и синдром Иценко–Кушинга, тиреотоксикоз, сахарный диабет I типа, ревматоидный артрит, состояния после резекции желудка, хронические заболевания печени, хроническая почечная недостаточность и др.).
• Лица, принимающие лекарственные препараты, побочным эффектом которых является снижение массы тела (кортикостероиды, антиконвульсанты, иммуносупрессоры, алюминий–содержащие антациды, антагонисты гонадотропинрилизинг–гормона).
Следует отметить, что женщины белой и желтой расы по сравнению с представительницами черной расы в среднем имеют более низкую прочность кости. Также показано, что риск остеопоротических переломов у женщин повышается при наличии переломов у членов их семей. Недостаточное потребление кальция в период зрелости и в пожилом возрасте может приводить к снижению минеральной плотности костной ткани. Все эти данные международных многоцентровых исследований позволили выделить факторы риска развития остеопороза (табл. 1).
Метаболизм кости характеризуется двумя разнонаправленными процессами: образованием новой костной ткани остеобластами и разрушением (резорбцией) старой кости остеокластами, которые связаны между собой и определяют количество массы кости. Для остеопороза характерен дисбаланс между этими процессами, поэтому современные ученые большое внимание уделяют изучению костного обмена. Оценка скорости образования или резорбции осуществляется путем измерения активности специфических ферментов костеобразующих или костеразрушающих клеток или путем определения компонентов, поступающих в кровоток и мочу во время синтеза или резорбции кости, что дает достаточно полную информацию об изменениях в уровне обмена кальция за короткий период времени.
Биохимические маркеры формирования кости представлены костным изоферментом щелочной фосфатазы, остеокальцином, карбокси– и аминотерминальными фрагментами проколлагена I типа.
Щелочная фосфатаза (ЩФ) – мембранные ферменты, присутствующие во всех органах и тканях. В кости ЩФ секретируется остеобластами, и предполагают, что она участвует в созревании матрикса и его минерализации и осуществляет свое действие при участии 1,25–диоксихолекальциферола. Синтез ЩФ возрастает в процессе дифференциации остеобластов при ускоренном формировании кости.
Остеокальцин – неколлагеновый кальций, связывающий белок, синтезируемый остеобластами. Остеокальцин в норме обнаруживается в остеобластах, матриксе кости и в сыворотке крови. Данный маркер имеет высокое сродство к гидроксиаппатитам и за счет этого формирует в кости комплексы с микрокристаллами гидроксиаппатита. Также предполагают, что он необходим для реализации действия 1,25 (ОН)2 Д3 витамина на кость.
Коллаген – наиболее распространенный белок в организме человека: его содержание составляет примерно 30%, а в кости около 50% от всего количества белка. В настоящее время выявлено 18 типов коллагена; в костной ткани в основном содержится коллаген I типа, который составляет 90% органического матрикса кости. Он синтезируется остеобластами в виде предшественников проколлагена I типа, представляющего собой большую молекулу, содержащую глобулярные фрагменты (карбокси– и аминотерминальные пептиды проколлагена I типа), которые отделяются от основной молекулы с помощью специфических пептидаз после выброса проколлагена из клетки. Очищенная молекула коллагена I типа включается в построение фибрилл костного матрикса, а карбокси– и аминотерминальные пептиды проколлагена I типа поступают в экстрацеллюлярную жидкость.
К маркерам костной резорбции относят тартрат–резистентную кислую фосфатазу, продукты деградации коллагена I типа – N– и C–телопептиды, определяемые в сыворотке крови, а также пиридинолин и дезоксипиридинолин, гидроксипролин и гликозиды гидроксилизина, определяемые в моче.
Таким образом, по соотношению изменения маркеров резорбции и синтеза представляется возможным судить о скорости костных потерь, предсказать риск переломов кости, а также выбрать адекватную терапию: при высокой скорости костного оборота предпочтительны препараты, подавляющие резорбцию, а при низкой – стимулирующие формирование кости (рис. 2).
Особого внимания заслуживает проблема остеопороза, вызванного приемом глюкокортикостероидов (ГК). По данным литературы, частота развития стероидного остеопороза составляет около 95%. Наиболее выраженные изменения наблюдаются в костях с трабекулярным типом строения, в большей степени поражается позвоночник.
Патогенез стероидного остеопороза сложен, но, несомненно, ключевым моментом в развитии стероидного остеопороза является прямое подавляющее действие ГК на остеобласты, ведущее к уменьшению костеобразования. При этом ГК снижают абсорбцию кальция в кишечнике и реабсорбцию кальция в почечных канальцах. Это приводит к отрицательному балансу кальция в организме и транзиторной гипокальциемии, что в свою очередь стимулирует секрецию паратиреоидного гормона и усиливает резорбцию костной ткани.
В настоящее время существует достаточное количество препаратов, применение которых уменьшает риск возникновения переломов за счет увеличения массы кости и улучшения ее качества. Лекарственные средства, применяемые для лечения остеопороза, могут быть условно разделены на три большие группы [20].
I группа – препараты, тормозящие резорбцию кости (эстрогены – дерместрил, фемостон, эстрожель, эстрофем, эстрофеминал; кальцитонины, бисфосфонаты и др.).
II группа – препараты, стимулирующие костеобразование (фториды, анаболические гормоны, паратиреоидный гормон и др.).
III группа – препараты многопланового действия (витамин D и его активные производные, комплексные соединения с кальцием, оссеин–гидроксиаппатитный комплекс).
Препараты группы кальцитонина (Миакальцик) не только существенно уменьшают выведение кальция из костной ткани, но и эффективно снижают болевой синдром, связанный с остеолитическими и остеопеническими состояниями, что выгодно отличает их от других лекарственных средств. Терапия кальцитонином показана как для лечения остеопороза у женщин в постменопаузе, особенно при невозможности назначения бисфосфонатов и купирования острых болей, связанных с остеопоротическими переломами позвоночника, так и в ходе терапии остеопороза у небеременных женщин в пременопаузе вследствие высокой безопасности. Кальцитонин назначается по 200 МЕ/сут. интраназально, лечение продолжается не более 2 мес., затем делается перерыв на 1–2 мес. Такие курсы лечения могут неоднократно повторяться (до 3 раз в год). Пациенты, имеющие высокий риск развития нестабильности эндопротеза, должны, начиная с 3–5–го дня после операции, использовать кальцитонин по 200 МЕ/сут. интраназально в течение 1 мес. Второй курс с двухнедельным перерывом; третий – после месячного перерыва, а четвертый курс – спустя 6 мес. после операции. В дальнейшем 30–дневные курсы следует повторять 3 раза в год. Причем терапия кальцитонинами должна сочетаться с назначением кальция в суточной дозе 1–1,5 г и активных метаболитов витамина Д в дозе 400 МЕ/сут или 0,5–1 мкг/сут., а также в составе комплексных препаратов. Комплексные препараты назначаются в дозировке 2 табл./капс. в сутки.
Бисфосфонаты являются синтетическими аналогами пирофосфата, который связывается с гидроксиаппатитом костей. Нужно отметить, что эти препараты принимают по крайней мере за полчаса до первого приема пищи, какой–либо жидкости или лекарств, запивать их следует только водой. Продолжительность лечения бисфосфонатами может составлять более 10 лет без перерывов при отсутствии тяжелой почечной недостаточности (клиренс креатинина должен превышать 30 мл/мин.).
В настоящее время интенсивно изучаются и имеют хорошие клинические перспективы препараты, стимулирующие костеобразование. Одним из наиболее эффективных в этом отношении веществ является фторид натрия, поскольку он может увеличивать популяцию остеобластических клеток. Показано, что фториды быстро откладываются в костях, где замещают гидроксильные ионы в гидроксиапатите с образованием менее растворимых кристаллов фтораппатита. Наибольший положительный опыт накоплен в использовании фторида натрия при стероидном остеопорозе.
Комплексные препараты кальция и витамина Д следует назначать всем пациентам, в отношении которых планируется длительное лечение ГК, желательно в сочетании с другими антиостеопоретическими лекарственными средствами с целью профилактики и лечения остеопороза.
При назначении антиостеопоретической терапии, помимо определенных показаний, не менее важно учитывать возможный спектр побочных эффектов (табл. 3). С целью обеспечения безопасности терапии необходимо регулярное (1 раз в 3–6 месяцев) мониторирование биохимических показателей (мочевина, креатинин, билирубин, аминотрансферазы, щелочная фосфатаза, общий белок, альбумин, общий и ионизированный кальций), коагулограммы (при назначении ЗГТ, СМЭР). Для уменьшения возможных нежелательных явлений со стороны верхних отделов желудочно–кишечного тракта следует рекомендовать пациентам принимать пероральные бисфосфонаты только в вертикальном положении и не ложиться в ближайшие часы. Для лучшего усвоения таблетки следует запивать водой (не менее 100 мл), не принимать молочных продуктов, препаратов кальция и железа в течение 1 часа.
Критерии эффективности антиостеопоретической терапии:
• отсутствие новых переломов костей при минимальной травме;
• стабилизация или прирост МПК через 12 месяцев;
• снижение показателей костной резорбции через 3–6 месяцев терапии.
Таким образом, тщательный анализ факторов риска у каждого пациента с предполагаемым ОП является крайне важным для диагноза, прогноза риска переломов. Еще предстоит установить гены, которые с высокой степенью до¬казательности можно будет отнести к кандидатам остеопороза, а углубленное понимание механизмов развития ОП поможет оптимизировать медицинскую помощь данной категории больных.
Литература
1. McKay H.A., Bailey D.A., Wilkinson A.A., et al. Familial comparison of bone mineral density at the proximal femur and lumbar spine. Bone miner 1994;24(2):95–107.
2. Slemenda C.W., Christian J.C., Williams C.J. Genetic determinants of bone mass in adult women: a reevaluation of the twin model and the potential importance of gene interaction on heritability estimates. J Bone Miner Res 1991;6(6):561–7.
3. Smith D.M., Nance W.E., Kang K.W. et al. Genetics factors in determining bone mass. J Clin Invest 1973;52(11):2800–8.
4. Niu T., Xu X. Candidate genes for osteoporosis. Therapeutic implications. Am J Pharmacogenomics 2001;1(1):11–9.
5. Bouxsein M.L., Courtney A.C., Hayes W.C. Ultrasonic and densitometric properties of the calcaneus correlate with the failure loads of cadaveric femur. Calcif Tiss Int 1995;56(2):99–103.
6. Пучкова Л.В., Дорохова И.И. Новые генетические факторы риска при остеопорозе. Остеопороз и остеопатии 2005;1:16–9.
7. Riggs B.L., Hartmann L.C.. Selective estrogen–receptor modulators – mechanisms of action and application to clinical practice. N Engl J Med 2003;348(7):618–29.
8. Windahl S.H., Galien R., Chiusaroli R., et al. Bone protection by estrens occurs through non–tissue–selective activation of the androgen receptor J. Clin Invest 2006;116(9):2500–9.
9. McDonnell D.P. The Molecular Pharmacology of SERMs. Trends Endocrinol Metab 1999;10(8):301–311.
10. Aoki K., Saito H., Itzstein C., et al. A TNF receptor loop peptide mimic blocks RANK ligand–induced signaling, bone resorption, and bone loss. J Clin Invest 2006;116(6):1525–34.
11. Weitzmann M.N., Pacifici R. Estrogen deficiency and bone loss: an inflammatory tale. J Clin Invest 2006;116:1186–1194.
12. Назаренко Г.И., Андропова О.В., Анохин В.Н. Дегенеративный (кальцинированный) аортальный стеноз, атеросклероз и остеопороз: клинико–морфологические параллели. Клиницист 2006;1:11–17.
13. Dellegrottaglie S., Sanz J., Rajagopalan S. Molecular determinants of vascular calcification: a bench to bedside view. Curr Mol Med 2006;6(5):515–24.
14. Карпова Н.Ю., Шостак Н.А., Рашид М.А. и соавт. Состояние костного метаболизма у больных кальцинированным аортальным стенозом дегенеративного генеза. Клиницист 2006; 1:18–22.
15. Скрипникова И.А. Взаимосвязь ге
