Тактика ведения пациента с артритом

Статья посвящена ревматоидный артриту — клиническим ситуацииям и алгоритмам лечения

Ревматоидный артрит (РА) – хроническое системное иммуновоспалительное заболевание неизвестной этиологии, сопровождающееся развитием симметричного прогрессирующего эрозивно-деструктивного полиартрита и внесуставными проявлениями [1]. РА ассоциирован с высоким риском кардиоваскулярных событий, остеопоротических переломов, ранней инвалидизацией и преждевременной смертностью пациентов. Улучшить прогноз и исходы болезни способны только своевременная диагностика и раннее активное лечение больных РА.
Течение болезни складывается из нескольких последовательных стадий: ранней, развернутой и поздней, каждая из них имеет свои клинические особенности и подходы к терапии.
Базовые принципы терапии РА («Treat to target» или «Лечение до достижения цели») [2, 3]:
1. Достижение ремиссии (DAS28 (суммарный индекс (включает упрощенный счет из 28 суставов), позволяет многократно оценивать активность РА и может быть использован для контроля его активности в повседневной практике) <2,6) или как минимум низкой активности заболевания (DAS28 <3,2).
2. Ранняя активная терапия базисными противовоспалительными препаратами (БПВП), в первую очередь метотрексатом (МТ), не позднее первых 3 мес. от начала болезни.
3. Лечение должно быть максимально активным, с быстрой эскалацией дозы МТ и последующим изменением (при необходимости) схемы лечения в течение 3 мес. до достижения ремиссии (или низкой активности) болезни.
4. Тщательный контроль изменений активности заболевания и коррекция терапии не реже 1 раза в 3 мес. или ежемесячно у больных с высокой и умеренной активностью РА.
5. В случае недостаточной эффективности стандартной терапии БПВП показано назначение генно-инженерных биологических препаратов (ГИБП).
6. Определение тактики терапии должно быть согласовано с пациентом.
К факторам неблагоприятного прогноза (ФНП) у больных РА относятся [4]:
– молодой возраст;
– женский пол;
– высокие титры ревматоидного фактора (РФ) и/или антитела к циклическому цитруллиновому пептиду (АЦЦП);
– эрозивный процесс в суставах по данным рентгенографического исследования или магнитно-резонансной томографии (МРТ);
– повышение уровней острофазовых показателей: скорости оседания эритроцитов (СОЭ) или С-реактивного белка (СРБ);
– высокая активность заболевания согласно индексам DAS28, SDAI (Simplified Disease Activity Index) или CDAI (Clinical Disease Activity Index);
– внесуставные проявления (синдром Шегрена, поражение легких и т. д.).
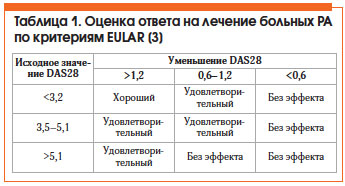
Оценка эффективности лечения РА по критериям Европейской антиревматической лиги (EULAR) представлена в таблице 1. Общепризнанным методом оценки активности РА является расчет индекса DAS28, который можно автоматически произвести на сайте www.das-score.nl.
Критерии эффективности терапии РА [5]:
• хороший клинический ответ (≈ ACR 70) (критерии Американской коллегии ревматологов);
• низкая активность болезни (DAS28 ≤ 3,2) или ремиссия (DAS28 ≤ 2,6);
• улучшение функции (HAQ (Health Assessment Questionare, опросник состояния здоровья, позволяющий оценить функциональные способности больных РА) <1,5) и качества жизни;
• предотвращение прогрессирования деструкции:
– замедление нарастания рентгенологических индексов (Sharp, Larsen);
– отсутствие появления новых эрозий;
– стабилизация или улучшение состояния по данным МРТ.
У пациентов, находящихся в состоянии ремиссии более 1 года после отмены глюкокортикостероидов (ГКС), следует рассмотреть вопрос о возможности прекращения лечения ГИБП, особенно если они применялись в комбинации с БПВП. Важное значение при определении тактики лечения имеет выбор пациентов.
Рассмотрим отдельные клинические ситуации и подходы к терапии при РА.
I. Пациент с впервые установленным ранним РА
Ранняя стадия РА – условно выделенная, клинико-патогенетическая стадия заболевания с длительностью активного синовита до 1 года, характеризуется преобладанием экссудативных изменений в пораженных суставах, частым атипичным течением и хорошим ответом на лечение. Выделение понятия «ранний РА» связано со сложившимися представлениями о патогенезе болезни и необходимости проведения ранней активной терапии РА. Ранний РА может дебютировать как недифференцированный артрит, что требует динамического наблюдения за больными и проведения тщательного дифференциально-диагностического поиска. На ранней стадии РА наиболее информативными являются диагностические критерии Американского и Европейского ревматологических сообществ, предложенные в 2010 г. (табл. 2).

Диагноз РА может быть установлен при общем счете не менее 6 баллов.
Доказано, что адекватная базисная терапия на ранней стадии РА позволяет предотвратить структурные повреждения, что способствует сохранению функциональной активности пациентов и улучшает отдаленный прогноз. БПВП необходимо назначать не позднее 3 мес. от начала РА с быстрой эскалацией дозы для достижения оптимального эффекта (DAS <2,4) и последующей заменой препарата в течение 3–6 мес. при его неэффективности [1]. Терапию БПВП следует продолжать даже при снижении активности заболевания и достижении ремиссии.
К БПВП первого ряда отнесены МТ, лефлуномид (ЛФ) и сульфасалазин (СС) (табл. 3), т. к. доказана их эффективность в отношении предотвращения деструктивных изменений суставов (уровень доказательности А). Препараты «второй линии» (гидроксихлорохин, препараты золота и др.) применяются при неэффективности препаратов первого ряда либо в комбинации с ними.
МТ – «золотой стандарт» терапии активного РА. При необходимости назначения МТ в дозе > 15 мг/нед. рекомендуется использовать парентеральный путь введения (в/м или п/к). Также с целью минимизации побочных явлений необходимо назначение фолиевой кислоты 1 мг/cут (5 мг/нед.), исключая дни приема МТ.

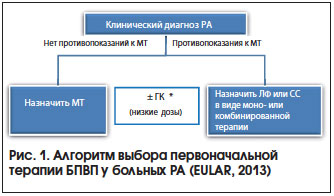
Основные стратегии лечения раннего РА (рис. 1) [7]:
1. Монотерапия МТ c последующей заменой на другие БПВП (ЛФ, СС) через 3–6 мес. в случае неэффективности или плохой переносимости).
2. Комбинированная базисная терапия, в т. ч. в сочетании с высокой дозой ГК. Используются комбинации БПВП как первого ряда (МТ + СС или МТ + ЛФ), так и второго ряда (МТ + Плаквенил) и т. д.
3. Комбинированная терапия синтетическими БПВП + ГИБП (в первую очередь ингибиторы фактора некроза опухоли (ФНО) при сохраняющейся > 3–6 мес. высокой активности РА, а также при наличии ФНП. Например, МТ 25 мг/нед. + Инфликсимаб 3 мг/кг массы тела.
II. Пациент с развернутым РА, не отвечающий на традиционные БПВП
Развернутая стадия РА – заболевание с отчетливо выраженной симптоматикой и длительностью болезни более 1 года. Суставной синдром имеет стойкий, симметричный и полиартикулярный характер с преимущественным поражением суставов кистей и стоп, выявляются признаки высокой или умеренной лабораторной активности, серопозитивность по РФ, эрозивный процесс в суставах по данным рентгенографии. Если диагноз устанавливается впервые, то стратегия ведения больного та же, что и при раннем РА. В случае уже проводившегося лечения с недостаточным эффектом или непереносимостью синтетических БПВП (как в виде монотерапии, так и при комбинированном их использовании), а также наличием ФНП прибегают к назначению ГИБП (рис. 2). Использование ГИБП позволяет максимально избирательно воздействовать на отдельные звенья иммунопатогенеза РА и существенно улучшить состояние больных РА, резистентных к стандартным БПВП и ГК [8]. Установлено, что комбинация традиционных БПВП с ГИБП более эффективна, чем монотерапия.
Назначение ГИБП показано:
– при длительно сохраняющейся (> 3–6 мес.) высокой активности РА;
– при высокой активности заболевания < 3 мес., только при наличии у больных ФНП.
Препаратами первого ряда среди ГИБП являются ингибиторы ФНО-α. Другие ГИБП назначаются больным РА с неадекватным ответом на блокаторы ФНО-α или при невозможности их применения (табл. 4).

Противопоказания к назначению ГИБП: отсутствие лечения одним или более БПВП (в первую очередь МТ) в полной терапевтической дозе; купирование обострений; тяжелые инфекционные заболевания (сепсис, септический артрит, пиелонефрит, остеомиелит, туберкулезная и грибковая инфекции, вирус иммунодефицита человека), злокачественные новообразования; беременность и лактация.
III. Пациент с поздним РА и остеопоротическими переломами
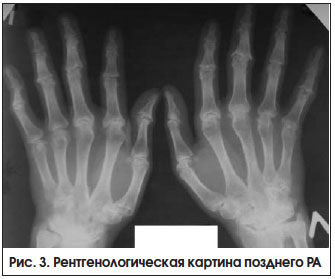
Поздняя стадия РА определяется как стадия необратимых структурных изменений (деформаций, подвывихов) суставов при длительности болезни > 2-х лет, с выраженными признаками активного воспаления или без них (рис. 3). Неуклонное прогрессирование болезни приводит к формированию различных видов подвывихов и контрактур суставов, в связи с чем возрастает роль реабилитационных и ортопедических мероприятий.
Развитие остеопороза (ОП) и ассоциированных с ним переломов является одним из наиболее тяжелых осложнений РА, определяющим неблагоприятное течение и прогноз болезни. Частота остеопоротических переломов среди больных РА в 1,5–2,5 раза выше, чем в общей популяции [9]. Предполагается, что развитие ОП и суставной деструкции при РА имеет единые патогенетические механизмы, в основе которых лежит цитокин-зависимая активация остеокластогенеза, приводящая к повышению костной резорбции [10]. Развитие ОП при РА определяется множеством общих и специфических, ассоциированных с заболеванием и лечением, факторов риска.
РА-ассоциированные факторы риска ОП и переломов [11]:
– активность воспалительного процесса,
– рентгенологическая стадия,
– тяжесть функциональных нарушений (HAQ > 1,25),
– длительность болезни,
– прием ГК,
– высокий риск падений.
У больных РА прием ГК в 4–5 раз повышает риск вертебральных переломов и удваивает риск переломов бедра. При этом доказано, что не существует безопасной дозы ГК. Также следует помнить, что развитие переломов у больных, получающих ГК, происходит при более высоких значениях минеральной плотности ткани (МПК), чем при первичном ОП, поэтому антиостеопоротическую терапию следует начинать при значениях Т-критерия < -1,5 стандартного отклонения от референсных значений.
Программа ведения больных РА и с остеопоротическими переломами включает контроль активности РА, коррекцию модифицируемых факторов риска ОП и переломов, предупреждение падений, антиостеопоротическую терапию, диету и физические упражнения. Всем больным РА необходимы проведение расчета абсолютного риска переломов (FRAX-алгоритм) (fracture risk assessment tool, 10-летний абсолютный риск перелома – инструмент оценки риска перелома ВОЗ) и профилактическое назначение препаратов кальция и витамина D. Назначение антиостеопоротической терапии без учета данных МПК проводится у пациентов в возрасте 65 лет и старше при наличии в анамнезе переломов при минимальной травме. Препаратами первой линии в лечении ОП у больных РА являются бисфосфонаты (БФ) и антитела к RANKL (лиганду рецептора активатора ядерного фактора каппа бета), обладающие антирезорбтивным действием (табл. 5). Привлекательность БФ при РА заключается еще и в том, что, по данным экспериментальных исследований, они могут оказывать благоприятное влияние на течение болезни. Установлено, что БФ способны ингибировать cинтез провоспалительных цитокинов и развитие костных эрозий при РА [12]. У пациентов с ранним артритом БФ в комбинации с МТ эффективно предотвращают развитие костной деструкции [13].

IV. Пожилой пациент с РА и НПВП-гастропатией
РА у лиц пожилого возраста характеризуется активным быстропрогрессирующим течением, высоким уровнем коморбидности и неблагоприятными исходами. Особое значение в структуре коморбидных состояний при РА имеют кардиоваскулярная и гастроинтестинальная патологии. По данным многочисленных исследований, сердечно-сосудистая заболеваемость и смертность у больных РА в 2–4 раза выше, чем в общей популяции, что диктует необходимость своевременного выявления и коррекции факторов кардиоваскулярного риска.
Рекомендации по снижению кардиоваскулярного риска у больных РА [14]:
• АСК следует принимать за ≥2 ч до приема нестероидных противовоcпалительных препаратов (НПВП).
• Не использовать НПВП в течение 3–6 мес. после острого сердечно-сосудистого события или процедуры.
• Регулярно контролировать артериальное давление.
• Использовать НПВП в низких дозах с коротким периодом полураспада (избегать назначения НПВП с пролонгированным высвобождением).
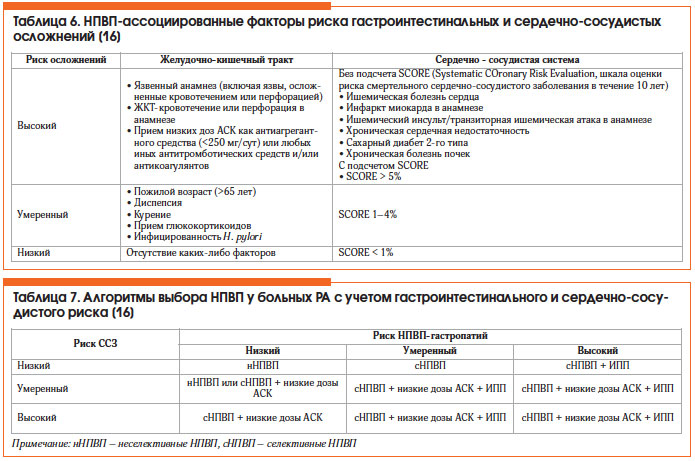
НПВП-гастропатия – одно из наиболее частых осложнений длительного приема НПВП, проявляющееся в виде эрозивного или язвенного поражения верхних отделов желудочно-кишечного тракта (ЖКТ) (преимущественно антральный и препилорический отделы желудка). Прием НПВП не влияет на прогрессирование РА, однако позволяет лучше контролировать симптомы заболевания на фоне терапии БПВП и ГИБП. НПВП-ассоциированные факторы риска гастроинтестинальных и сердечно-сосудистых осложнений представлены в таблице 6.
Экспертами EULAR разработан «калькулятор» для индивидуального подбора НПВП в зависимости от наличия факторов риска в отношении ЖКТ и сердечно-сосудистой системы [15]. К НПВП с наименьшим кардиоваскулярным риском отнесены напроксен, целекоксиб, кетопрофен, низкие дозы ибупрофена (<1200 мг/сут). Основные лекарственные средства, которые используют для лечения НПВП-индуцированных гастропатий, — ингибиторы протонной помпы (ИПП), Н2-блокаторы и мизопростол (синтетический аналог ПГ Е2). Алгоритмы выбора НПВП у больных РА с учетом гастроинтестинального и сердечно-сосудистого риска представлены в таблице 7 [16].
Не так давно появилась новая генерация НПВП, которые повышают активность оксида азота (NO) в слизистой желудка (NO-НПВП). Как известно, NO обладает гастропротективными свойствами: стимулирует секрецию слизи, бикарбоната, улучшает микроциркуляцию, ингибирует адгезию лейкоцитов к эндотелию, что и определяет фармакологические преимущества данной группы НПВП. Одним из представителей NO-НПВП является препарат Найзилат (амтолметин гуацил), который наряду с высокой анальгетической и противовоспалительной активностью обладает гастропротективными свойствами. В рандомизированных клинических исследованиях были продемонстрированы более низкие частота и тяжесть повреждений слизистой оболочки желудка после применения амтолметин гуацила по сравнению с таковыми других неселективных НПВП (диклофенак, индометацин, пироксикам), при сопоставимой противовоспалительной и анальгетической их эффективности [17]. Сравнительное исследование амтолметин гуацила 1200 мг/сут и целекоксиба 400 мг/сут у больных РА показало равнозначные эффективность и безопасность препаратов [18]. Терапевтическая доза амтолметин гуацила (Найзилат) составляет 600 мг 2 р./сут натощак, поддерживающая – 600 мг/сут.
Заключение
РА является гетерогенным заболеванием, исходы которого во многом определяются своевременной диагностикой болезни и правильно выбранной тактикой лечения. Ранняя стадия РА, особенно первые 3 мес. от начала заболевания, наиболее благоприятны для проведения эффективной базисной терапии. Основой ведения больных РА является тщательное мониторирование активности заболевания (не реже 1 р./3 мес.) с последующей коррекцией терапии при необходимости. Выбор терапии определяется стадией РА, активностью болезни, наличием ФНП, сосуществующими коморбидными состояниями, а также эффективностью предшествующего лечения.
Источник
Реактивный артрит – аутоиммунное заболевание, которое развивается после перенесенных инфекционных заболеваний и проявляется поражением суставов. Ревматологи Юсуповской больницы устанавливают диагноз с помощью новейшей аппаратуры и лабораторных методов диагностики. Комплексную терапию проводят, придерживаясь клинических рекомендаций по лечению реактивного артрита. Врачи клиники терапии индивидуально подбирают лекарственные препараты, используют только фармакологические средства, зарегистрированные в РФ.
Тяжёлые случаи заболевания обсуждают на заседании Экспертного Совета. В его работе принимают участие кандидаты и доктора медицинских наук, врачи высшей категории. Ведущие специалисты в области ревматологии коллегиально вырабатывают тактику ведения больных реактивным артритом. Медицинский персонал внимательно относится к пожеланиям пациентов и их родственников.

Причины реактивного артрита разные. К реактивным артритам относят все воспаления суставов, которые хронологически связаны с какой-либо инфекцией. При этом в синовиальной жидкости поражённых суставов микроорганизмы не выявлялись. Связь артрита с предшествующей инфекцией подтверждают путём тщательного выяснения истории развития болезни, анализа клинических проявлений артрита, определения возбудителя, обнаружением в крови высоких титров антител к нему.
Реактивные артриты занимают одно из ведущих мест по распространённости среди ревматических заболеваний. Их удельный вес составляет 10-15%. В общей структуре реактивных артритов лидирующее положение занимают урогенные реактивные артриты, связанные с инфицированием органов мочеполовой системы. Энтерогенные формы заболевания, при которых основной очаг инфекции локализуется в кишечнике, развиваются реже.
Симптомы реактивного артрита
Реактивный артрит является серонегативным спондилоартритом. Он отвечает критериям Европейской группы по изучению спондилоартритов. Различают следующие наиболее характерные признаки ревматоидного артрита:
- Заболевание дебютирует до 30–40 лет;
- Прослеживается хронологическая связь артрита с предшествующей кишечной инфекцией (диареей), конъюнктивитом, урогенитальной инфекцией;
- Болезнь начинается внезапно;
- Поражено ограниченное количество суставов (моноолигоартрит);
- Имеет место асимметричность поражения суставов и осевого скелета;
- В патологический процесс вовлекается сухожильно-связочный аппарат.
При реактивном артрите проявляются признаки системного воспаления (кожа, слизистые оболочки, глаза, внутренние органы). Инфекция доказана бактериологическими или верологическими исследованиями. Отмечается серонегативность по ревматоидному фактору. Есть случаи серонегативных спондилоартропатий в семье или положительный HLA-B27. Заболевание протекает относительно доброкачественно с полным обратным развитием воспаления, но не исключены рецидивы и хроническое течение процесса.
Независимо от причины заболевания клиническая картина реактивного артрита протекает однотипно. К моменту развития заболевания симптомы кишечной инфекции стихают или подвергаются полному обратному развитию. Болезнь развивается через 3–60 дней после перенесенной инфекции. У50% пациентов появляется лихорадочный синдром и развивается асимметричный олигоартрит с преимущественным поражением суставов нижних конечностей:
- Коленных;
- Голеностопных;
- Пальцев стоп (особенно первых пальцев).
Если в коленном суставе быстро развивается выпот, в подколенной области образуются кисты. В последующем они разрываются, формируется псевдофлебитическим синдром. Значительно реже поражаются суставы верхних конечностей.
В 10–16% случаев развивается тендовагинит отдельных пальцев стоп. Он проявляется выраженной болью, отечностью и специфической багрово-синюшной окраской кожи. Палец напоминает сосиску. У 30% больных поражаются места прикрепления сухожилий и связок к костям возле суставов. Воспаление локализуется преимущественно в пяточных областях. Может развиться ахиллобурсит, подошвенные апоневрозиты и трохантериты.
На ранней стадии заболевания примерно в 50% случаев врачи выявляют следующие признаки поражения позвоночника:
- Боли в нижнем отделе или в области проекции крестцово-подвздошных сочленений;
- Чувство скованности;
- Спазм паравертебральных мышц;
- Боль.
Среди внесуставных проявлений ревматоидного артрита наиболее типичным является поражение органа зрения: двусторонний катаральный слабо выраженный конъюнктивит, который появляется вместе с артритом и угасает в течение нескольких дней спонтанно, острый передний увеит, следствием которого может быть регрессирующее снижение зрения вплоть до полной слепоты.
Признаком ревматоидного артрита могут быть специфические поражения кожи и слизистых оболочек:
- Кератодермия;
- Кератодермические псориазоподобные высыпания на разных участках тела и волосистой части головы;
- Поражения ногтей на пальцах стоп (изменение цвета, повышенная ломкость, шероховатость, бугристость);
- Подногтевой гиперкератоз;
- Онихолизис.
У 20-40% пациентов развивается кольцевидный баланит или баланопостит. В 5–10% случаев определяются малосимптомные безболезненные эрозии в ротовой полости, которые могут оставаться незамеченными. У больных с иерсиниозным реактивным артритом может развиться узловая эритема. Одним из проявлений реактивного артрита может быть увеличение паховых лимфоузлов. Может развиться поражение скелетных мышц по типу миозита, невриты периферических нервов.
Диагностика реактивного артрита
У пациентов, страдающих реактивным артритом, во время комплексного обследования врачи находят следующие изменения лабораторных показателей;
- Анемию (уменьшение количества эритроцитов);
- Умеренный нейтрофильный лейкоцитоз (увеличение количества лейкоцитов за счёт нейтрофилов);
- Увеличение скорости оседания эритроцитов, увеличение СОЭ, уровня С-реактивного белка;
- Протеинурию (появление белка в моче);
- Лейкоцитурию (лейкоциты в моче);
- Микрогематурию (эритроциты в моче).
Ревматоидные факторы и антинуклеарный фактор не выявляют. При исследовании синовиальной жидкости определяются неспецифические признаки воспаления: низкая вязкость, рыхлый муциновый сгусток, высокое количество лейкоцитов с преобладанием нейтрофилов. Для выявления триггерных инфекционных агентов врачи Юсуповской больницы используют микробиологические, иммунологические и молекулярно-биологические методы исследования.
Лечение реактивного артрита
При наличии симптомов острого реактивного артрита, ассоциированного с хламидиями, в острой фазе заболевания проводят антибиотикотерапию. Санация организма больного от хламидийной инфекции представляет собой достаточно сложную задачу. При воспалении уретры воспалительный процесс не ограничивается мочеиспускательным каналом, а распространяется на его вышележащие отделы. Это значительно затрудняет санацию очага.
Для лечения урогенитального хламидиоза при ревматоидном артрите препаратами выбора являются антибиотики из групп макролидов или тетрациклинов. Длительность курса антибиотикотерапии от 28 до 30 дней. При неэффективности или непереносимости указанных препаратов назначают фторхинолоны.
При энтерогенном реактивном артрите антибиотики не назначают. Для лечения поражения суставов применяют нестероидные противовоспалительные средства (диклофенак, мелоксикам, нимесулид) в стандартных суточных дозах, и глюкокортикоиды (триамцинолон, бетаметазон). Кортикостероидные гормоны вводят в полость сустава или околосуставные ткани. При наличии кардита, нефрита назначают глюкокортикоиды внутрь в средних дозах.
При хроническом течении реактивного артрита проводят терапию сульфасалазином, метотрексатом, азатиоприном. При резистентных к терапии хронических вариантах заболевания применяют ингибиторы фактора некроза опухоли α. При стихании активности артрита специалисты клиники реабилитации включают в план лечения физиотерапевтические процедуры, массаж, лечебную физкультуру. Пациентам рекомендуют санаторно-курортное лечение.
У 80% пациентов после 6-12 месяцев лечения отмечается полное выздоровление, симптомы заболевания исчезают. Если ликвидированы причины воспалительного процесса, рецидивов не наступает, если не произойдёт повторного инфицирования. В 20% случаев патологический процесс переходит в хроническую стадию. Редко наступает летальный исход вследствие развития амилоидоза или тяжёлого поражения сердца.
При появлении первых симптомов реактивного артрита звоните Юсуповскую больницу. Специалисты контакт центра запишут вас на приём к ревматологу в удобное вам время. После комплексного обследования врач назначит лечение, которое направлено на искоренение причины заболевания и ликвидацию симптомов болезни.
Источник
