Влияние щитовидной железы при ревматоидном артрите
11 апреля 2016г.
Ревматоидный артрит (РА) в настоящее время рассматривается как одно из наиболее частых аутоиммунных заболеваний, характеризующееся значительным снижением продолжительности жизни по сравнению с популяцией в целом, а также выраженными нарушениями функции суставов [2]. Развитие и течение РА связано с изменением иммунологической реактивности организма, сложными ферментативными и обменными сдвигами, в регуляции которых большое значение имеет эндокринная система [4]. Известно, что тиреоидные гормоны играют важную роль в обменных процессах, иммуногенезе, проницаемости клеточных мембран, транспорте ионов, синтезе белка, активности ферментных систем, являются регуляторами трофических функций организма, обмена веществ, оказывают влияние на адаптационно-приспособительные процессы. Избыточная концентрация тиреоидных гормонов способствует усилению аутоиммунных реакций. Нарушения деятельности желез внутренней секреции могут привести к тем изменениям обмена веществ в организме, которые, даже не получая явного отражения в клинической картине, могут иметь несомненное значение в особенностях клинического течения РА и определять эффективность лечения [3].
Целью нашей работы явилось определение особенностей течения РА в сочетании с аутотиреоидной патологией и изучение функциональной активности щитовидной железы при данной патологии.
Нами было обследовано 25 больных РА с сопутствующей аутотиреоидной патологией (АТП). В ее состав входили: хронический аутоиммунный тиреоидит (ХАИТ) в фазе эутиреоза, первичный гипотиреоз на фоне атрофической формы ХАИТ, гипертиреоз на фоне ХАИТ, смешанный токсический зоб. Все пациенты были женского пола, в возрасте от 21 до 77 лет (средний возраст 55,16±15,3 лет). Средняя продолжительность РА составила 5,08±3,29 лет. Средняя продолжительность клинической манифестации дисфункции щитовидной железы составила 3,01±1,74 года, что в большинстве случаев, свидетельствует о развитии/обострении тиреоидной патологии на фоне уже имеющегося РА. Большинство обследованных больных имели II-III рентгенологические стадии и умеренную активность РА.
При изучении патологии, связанной с сопутствующим заболеванием щитовидной железы, в первую очередь у обследованных нами больных обращали на себя внимание характерные жалобы. Среди них наиболее частыми были жалобы астено-невротического характера: общая слабость (100%), утомляемость (100%), повышенная потливость (66,7%), дрожание рук (83,3%), похудание, сердцебиение. У больных РА с тиреоидной патологией частыми оказались трофические расстройства, такие как выпадение волос, ломкость ногтей которые встречались у 50% больных. Из других симптомов, ассоциируемых с эндокринной патологией, обращало внимание и поражение сердечно-сосудистой системы: тахикардия (66,7%), нарушение ритма (33,3%) и блокады различного рода (16,6%), неприятные ощущения и боли в области сердца (50%), нарушения процессов реполяризации на ЭКГ. В целом, у пациентов с РА и поражением щитовидной железа имела место более высокая частота поражения сердца (n=9, 36,6%) и почек (n=7, 28 %) по сравнению с ранее опубликованными данными о РА в целом.
Помимо клинических особенностей заболевания, мы исследовали концентрацию антител к T3 и T4 методом непрямого иммуноферментного анализа. В качестве антигена использовались гормоны, иммобилизированные на магнитных полиакриламидных гранулах по методу И.П. Гонтаря с соавт [1]. Результаты выражали в относительных единицах оптической плотности (е.о.п.), точку разделения положительных и отрицательных результатов вычисляли с использованием референтной группы здоровых лиц (n=23). Кроме того, у больных РА измеряли концентрации свободных Т3 и к Т4.
В результате измерений выявлено достоверное повышение содержания антител к Т3 и к Т4 у больных РА с АТП (0,198±0,003 и 0,156±0,05 е.о.п., соответственно) по сравнению со здоровыми лицами (0,052±0,008 и 0,041±0,008 е.о.п., соответственно. Различия между РА с АТП и здоровыми лицами были статистически значимыми (p
Выводы: Полученные данные показывают заинтересованность щитовидной железы в развитии метаболических и клинических синдромов при РА. Таким образом, повышение уровня АТ к тиреоидным гормонам может использоваться для прогнозирования течения клинического варианта РА наряду с традиционными клинико-лабораторными показателями, что позволит начать своевременную коррекцию начинающихся нарушений и для возможной коррекции терапии с учетом поражения щитовидной железы.
Список литературы
1. Зборовский А.Б., Гонтарь И.П., Александров А.В. и соавт. Возможности использования иммобилизированных наносистем в ревматологии // Доктор.Ру. – 2009. – №3. – С.53-57.
2. Кремлева О.В. Ревматоидный артрит: влияние болезни на социальные аспекты качества жизни /О.В.Кремлева, Г.Б. Колотова // Научно-практич. ревматол. – 2004. — № 2. – С. 14-18.
3. Шустов С.Б. Функциональная и топическая диагностика в эндокринологии / Шустов С.Б., Халимов Ю.Ш. – СПб, 2001 — 238 с.
4. Hochberg M.C., Silman A.J., Smolen J.S. et al. Rheumatology: 6th ed. – Philadelphia etc.: Mosby Elsevier, 2015.– 1905 p.
Источник
Ахунова Г.Р., Валеева Ф.В., Киселева Т.А., Салихов И.Г.
Введение. Ревматоидный артрит (РА) – распространенное (около 1% населения планеты) аутоиммунное ревматическое заболевание, характеризующееся симметричным эрозивным артритом (синовитом) и широким спектром внесуставных (системных) проявлений. Характерными проявлениями РА являются боли, нарушение функции суставов и неуклонно прогрессирующая деформация суставов, необратимое поражение внутренних органов, приводящие к ранней потере трудоспособности (около трети пациентов становятся инвалидами в течение 20 лет от начала болезни) и сокращению продолжительности жизни пациентов (в среднем на 5–15 лет) [1].
В последние годы взгляд на РА как на неизлечимое заболевание пересматривается. Это cвязано с расширением возможностей ранней диагностики РА, что позволяет начинать активную, тщательно контролируемую (tight control) терапию базисными противовоспалительными препаратами (БПВП), в первую очередь метотрексатом (МТ), в ранней стадии болезни и разработкой нового класса генно-инженерных биологических препаратов (ГИБП), которые селективно блокируют важные звенья иммунопатогенеза РА [2].
Пациенты с РА подвергнуты повышенной частоте развития патологии щитовидной железы, что объясняется общностью иммунологических механизмов развития этих заболеваний. Распространенность тиреоидной патологии в целом среди больных РА достигает 28% [3].
Работы отечественных авторов по изучению функционального состояния щитовидной железы у больных РА на фоне современной терапии немногочисленны [4]. Особый интерес представляет изучение функционального состояния ЩЖ в эру лечения больных РА генно-инженерными биологическими препаратами. Зарубежные и отечественные исследования по этой теме отсутствуют, что и предопределило актуальность данной работы.
Цель. Оценить функциональное состояние щитовидной железы у больных РА на фоне терапии БПВП и ГИБП.
Материалы и методы. В исследование включено 47 больных (38 (80,9%) женщин и 9 (19,1%) мужчин) с достоверным по классификационным критериям ACR (1987) РА, наблюдавшихся в отделении ревматологии ГАУЗ «Республиканская клиническая больница» МЗ РТ и МУЗ «Городская клиническая больница №7» г. Казани. Критериями включения были: отсутствие в анамнезе лечения «базисными» препаратами в группе пациентов, получающих БПВП, отсутствие в анамнезе лечения ГИБП в группе пациентов, получающих биологическую терапию, отсутствие приема L – тироксина у всех пациентов. В соответствии с терапией пациенты были разделены на пять групп: ритуксимаб получали – 12 (25,5%) больных, тоцилизумаб – 7 (14,9%), абатацепт – 3 (6,4%) и инфликсимаб – 4 (8,5%), БПВП – 21 (44,7%) больных (14 — метотрексат, 3 — лефлуномид, 2 — сульфасалазин, 2 — плаквенил).
Терапия ГИБП проводилась по стандартной схеме [5,6].
На момент начала лечения ритуксимабом 11 пациентов находились на базисной терапии РА, 9 из них получали метотрексат в дозе 7,5 – 15 мг в неделю, 2 – лефлуномид в дозе 20 мг в день. На момент назначения тоцилизумаба и абатацепта все пациенты получали метотрексат (в дозе 7,5 – 20 мг и 10 – 15 мг в неделю соответственно), инфликсимаба – 1 пациент получал метотрексат в дозе 12,5 мг в неделю, 2 – лефлуномид в дозе 10 и 20 мг в день.
В группе больных, начавших впервые получать лечение БПВП, 14 пациентам назначен метотрексат в дозе 7,5-15 мг в неделю, 3 пациентам — лефлуномид в дозе 20 мг в день, 2 пациентам — сульфасалазин в дозе 2000 мг в день, 2 пациентам — плаквенил в дозе 200 мг в день.
У всех пациентов в ходе исследования оценивали стандартные параметры суставного синдрома: число болезненных суставов (ЧБС), число припухших суставов (ЧПС), продолжительность утренней скованности в минутах, выраженность боли по 100 миллиметровой визуальной аналоговой шкале (ВАШ) и общее состояние здоровья пациентов (ОСЗП) по ВАШ. Количественная оценка активности РА проводилась с использованием индекса DAS 28 (Disease Activity Score), рекомендованного EULAR. Активность заболевания расценивалась как низкая (DAS28 ≤3,2), умеренная (3,2<DAS28≤5,1) или высокая (DAS28>5,1). Функциональная способность пациентов была определена по классификации О. Steinbroker (функциональный класс – ФК) и Станфордской шкале оценки здоровья Health Assessment Questionnaire (HAQ). Степень функциональных нарушений по данным опросника HAQ определялась по баллам: от 0 до 0,5 баллов – популяционная «норма», от 0,5 до 1,0 баллов – минимальные, от 1,0 до 2,0 баллов – умеренные, от 2,0 до 3,0 баллов – выраженные функциональные нарушения. Исследовали лабораторные параметры: скорость оседания эритроцитов (СОЭ), уровень С-реактивного белка (СРБ) и ревматоидного фактора. Также всем пациентам оценивали уровень свободного тироксина (fТ4), свободного трийодтиронина (fТ3), тиреотропного гормона (ТТГ), антител к тиреоидной пероксидазе (АТ к ТПО) и тиреоглобулину (АТ к ТГ).
Эффект терапии оценивали по критериям ACR и EULAR (DAS 28). Оценку эффективности проводили через 24 недели терапии.
Возраст больных РА составил 44 [32,5; 52] года, длительность заболевания – 2,3 [0,2; 4,4] года. Серопозитивный РА диагностирован у 38 (80,9%) больных, серонегативный – у 9 (19,1%). Средняя степень активности РА определена у 8 (17%) больных, высокая — у 39 (83%). I рентгенологическая стадия РА установлена у 2 (4,3%) пациентов, II – у 21 (44,7%), III – у 14 (29,8%), IV — у 10 (21,3%) пациентов. Медленно-прогрессирующее течение заболевания было у 31 (66%) пациента, быстропрогрессирующее – у 16 (34%). Системные проявления были выявлены у 38 (80,9%) больных. Индекс HAQ составил 1,5 [1,1;1,9]. ФК I — II был диагностирован у 18 (38,3%) пациентов, ФК III — IV – у 29 (61,7%) пациентов.
Статистическая обработка полученных результатов осуществлялась с использованием пакета программ Excel, Statististica 6,0 для Windows. Достоверность различий при сравнении количественных параметров оценивали с помощью критерия Уилкоксона. Для сравнения долей применялись таблицы сопряжённости, с последующим использованием точного критерия Фишера или критерия χ кв. Пирсона. Различия считались достоверными при p<0,05.
Результаты и обсуждение. Среди обследованных больных, начавших получать ритуксимаб (n=12) было 8 (66,7%) женщин и 4 (33,3%) мужчин в возрасте 41 [29,0;48,8] лет с длительностью РА 4 [2,6;9,3] года. Серопозитивный РА был диагностирован у 10 (83,3%) больных, серонегативный РА – у 2 (16,7%). У 10 (83,3%) пациентов было медленно — прогрессирующее течение РА. II рентгенологическая стадия РА установлена у 3 (25,0%) пациентов, III – у 5 (41,7%), IV — у 4 (33,3%) пациентов. Системные проявления РА были выявлены у 10 (83,3%) больных. Средняя степень активности РА была диагностирована у 1 (8,3%) больного, высокая – у 11 (91,7%).
Изучение динамики активности заболевания по индексу DAS 28 показало его достоверное снижение через 6 месяцев от начала терапии (p<0,05) (табл. 1). Также на фоне терапии ритуксимабом отмечена достоверная положительная динамика ЧБС, ЧПС, интенсивности боли и ОСЗП по ВАШ, длительности утренней скованности, СОЭ, СРБ и индекса HAQ (p<0,05).
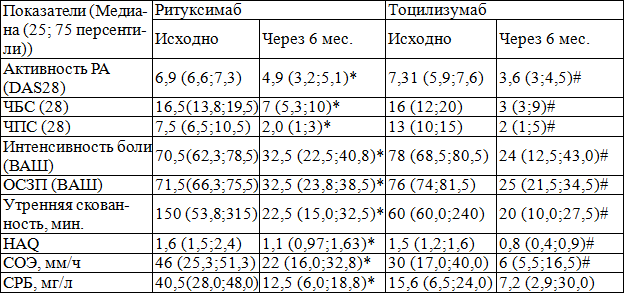
Таблица 1. Динамика основных клинических и лабораторных показателей у больных РА на фоне терапии ритуксимабом и тоцилизумабом

Примечания: * — р<0,05 в группе пациентов, получающих ритуксимаб; # — р<0,05 в группе пациентов, получающих тоцилизумаб
Оценка эффективности терапии ритуксимабом по критериям EULAR (рис. 1) показала, что через 6 месяцев лечения хороший эффект достигнут у 4 (33,3%) пациентов, удовлетворительный эффект — у 8 (66,7%) пациентов с РА. Оценка эффективности терапии по критериям ACR (рис. 2) показала, что через 6 месяцев лечения уменьшение параметров на 20% отмечалось у 12 (100%) пациентов, на 50% — у 7 (58,3%) и на 70% — у 3 (25%) пациентов.
Рис. 1. Эффективность терапии по критериям EULAR через 6 мес. лечения
Рис. 2. Эффективность терапии по критериям ACR через 6 мес. лечения
В начале исследования в группе пациентов, получавших ритуксимаб (n=12), у 1 (8,3%) пациента был диагностирован субклинический гипотиреоз и у 1 (8,3%) пациента были выявлены АТ к ТПО и АТ к ТГ.
На фоне терапии ритуксимабом у пациента с субклическим гипотиреозом произошла нормализация уровня ТТГ. У данного пациента была достигнута клинико-лабораторная ремиссия РА по критериям EULAR и 70% улучшение по критериям ACR. У пациента, с исходно высоким уровнем АТ к ТПО и АТ к ТГ, на фоне лечения ритуксимабом произошло снижение их уровня. Пациент достиг удовлетворительного эффекта по EULAR и 50% улучшения по ACR.
У 2 пациентов с исходно нормальными показателями антител к щитовидной железе на фоне лечения ритуксимабом произошло повышение уровня АТ к ТПО у одного пациента (1 (8,3%)) и АТ к ТГ у другого (1 (8,3%)). Эти пациенты достигли удовлетворительного эффекта по EULAR, 20 % улучшения по ACR.
Таким образом, на фоне улучшения клинических и лабораторных параметров РА произошло улучшение функции щитовидной железы и снижение уровня антител к щитовидной железе.
Среди обследованных больных, начавших получать тоцилизумаб (n=7) было 6 (85,7%) женщин и 1 (14,3%) мужчина в возрасте 44 [41,5;47,5] лет с длительностью РА 3 [3,3;4,4] года. Серопозитивный РА был диагностирован у всех пациентов (7 (100%)). У 5 (71,4%) пациентов было медленно — прогрессирующее течение РА. II рентгенологическая стадия РА установлена у 3 (42,9%) пациентов, III – у 3 (42,%), IV — у 1 (14,3%) пациента. Системные проявления РА были выявлены у 4 (57,1%) больных. Средняя степень активности РА была диагностирована у 1 (14,3%) больного, высокая – у 6 (85,7%) больных.
При оценке динамики индекса активности болезни (DAS 28) выявлено, что тоцилизумаб достоверно снижал активность заболевания через 6 месяцев от начала терапии (p<0,05) (табл. 1). Также на фоне терапии тоцилизумабом отмечена достоверная положительная динамика ЧБС, ЧПС, интенсивности боли и ОСЗП по ВАШ, длительности утренней скованности, СОЭ и индекса HAQ (p<0,05).
Оценка эффективности терапии тоцилизумабом по критериям EULAR (рис. 1) показала, что через 6 месяцев лечения у 1 (14,3%) пациента достигнута ремиссия, у 2 (28,6%) пациентов — хороший эффект, у 4 (57,1%) пациентов — удовлетворительный эффект. Оценка эффективности терапии по критериям ACR (рис. 2.) показала, что через 6 месяцев лечения уменьшение параметров на 20% отмечалось у 7 (100%) пациентов, на 50% — у 5 (71,4%) и на 70% — у 4 (57,1%) пациентов.
В начале исследования в группе пациентов, получавших тоцилизумаб (n=7) у 1 (14,3%) пациента был диагностирован субклинический гипотиреоз с повышенным уровнем АТ к ТПО и АТ ТГ, у 2 (28,6%) пациентов был выявлен повышенный уровень АТ к ТГ.
Через 6 месяцев лечения тоцилизумабом у пациента с субклическим гипотиреозом уровень ТТГ и антител к щитовидной железе незначительно снизился. Пациент достиг хорошего эффекта по критериям EULAR и 70% улучшения по ACR. У одного пациента, с исходно высоким уровнем АТ к ТГ, был впервые диагностирован субклинический гипотиреоз, но произошла нормализация уровня АТ к ТГ. При этом активность заболевания по индексу DAS 28 оставалась высокой, был достигнут удовлетворительный эффект по EULAR и 20% улучшение по ACR. У второго пациента с исходно высоким уровнем АТ к ТГ на фоне лечения тоцилизумабом их уровень нормализовался. У пациента была диагностирована ремиссия по EULAR, 70% улучшение по ACR.
Таким образом, на фоне улучшения клинических и лабораторных параметров РА произошло улучшение функции щитовидной железы и снижение уровня антител к щитовидной железе. У пациента с недостаточной эффективностью проводимой терапии функция щитовидной железы ухудшилась.
Среди обследованных больных, начавших получать абатацепт (n=3) было 3 (100%) женщины в возрасте 39 [30,5; 51,0] лет с длительностью РА 1,3 [1,1; 2,7] года. Серопозитивный РА был диагностирован у всех пациентов (3 (100%)). У 1 (33,3%) пациента было медленно — прогрессирующее течение РА. II рентгенологическая стадия РА установлена у 1 (33,3%) пациента, III – у 2 (66,7%) пациентов. Системные проявления РА были выявлены у всех пациентов (3 (100%)). Средняя степень активности РА была диагностирована у 1 (33,3%) больного, высокая – у 2 (66,7%) больных.
Изучение динамики активности заболевания по индексу DAS 28 показало его снижение через 6 месяцев от начала терапии (табл. 2). Также на фоне терапии абатацепта отмечена положительная динамика ЧБС, ЧПС, интенсивности боли и ОСЗП по ВАШ, длительности утренней скованности, СОЭ и индекса HAQ (p>0,05).
Таблица 2. Динамика основных клинических и лабораторных показателей у больных РА на фоне терапии абатацепта и инфликсимаба
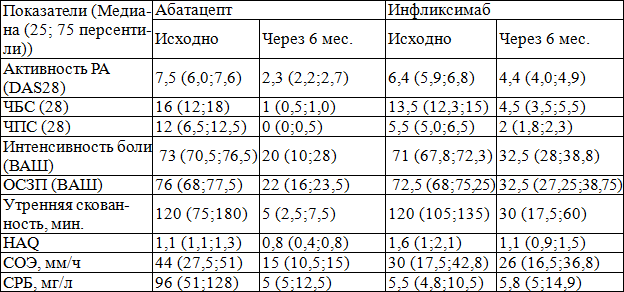
Примечание: в группе пациентов, получающих абатацепт и инфликсимаб, достоверных различий нет
Оценка эффективности терапии абатацептом по критериям EULAR (рис. 1) показала, что через 6 месяцев лечения хороший эффект достигнут у всех пациентов (3 (100%)). Оценка эффективности терапии по критериям ACR (рис. 2) показала, что через 6 месяцев лечения у всех пациентов наблюдалось уменьшение параметров на 20%, на 50% и на 70%.
В начале исследования в группе пациентов, получавших абатацепт (n=3) у 2 (66,7%) пациентов были выявлены повышенные уровни антител к щитовидной железе (у одного пациента – АТ к ТПО и АТ к ТГ, у другого – только АТ к ТПО).
У пациента с исходно высоким уровнем антител к щитовидной железе на фоне лечения абатацептом уровень АТ к ТПО снизился, уровень АТ к ТГ нормализовался. У данного пациента была достигнута ремиссия РА по критериям EULAR и 70% улучшение по ACR. У другого пациента с исходно высоким уровнем АТ к ТПО через 6 месяцев лечения их уровень уменьшился, но произошло увеличение уровня АТ к ТГ. У пациента достигнут хороший эффект по EULAR, 70 % улучшение по ACR.
Таким образом, на фоне улучшения клинических и лабораторных параметров РА произошло снижение уровня антител к щитовидной железе.
Среди обследованных больных, начавших получать инфликсимаб (n=4) было 3 (75%) женщины, 1 (25%) мужчина в возрасте 45 [39,3;50,3] лет с длительностью РА 5 [4,5;10,5] лет. Серопозитивный РА был диагностирован у 3 (75%) пациентов, серонегативный — у 1 (25%). У 2 (50%) пациентов было медленно — прогрессирующее течение РА. III рентгенологическая стадия РА установлена у 1 (25%) пациента, IV – у 3 (75%) пациентов. Системные проявления РА были выявлены у 2 пациентов (50%). Высокая степень активности РА была диагностирована у всех больных (4 (100%)).
На фоне терапии инфликсимабом отмечена положительная динамика ЧБС, ЧПС, интенсивности боли и ОСЗП по ВАШ, длительности утренней скованности, СОЭ, индекса HAQ, активности заболевания по индексу DAS 28 (p>0,05).
Оценка эффективности терапии инфликсимабом по критериям EULAR (Рис. 1.) показала, что через 6 месяцев лечения хороший эффект достигнут у 1 (25%) пациента, удовлетворительный эффект – у 2 (50%) пациентов, у 1 (25%) пациента эффект отсутствовал. Оценка эффективности терапии по критериям ACR (рис. 2) показала, что через 6 месяцев лечения уменьшение параметров на 20% отмечалось у всех пациентов (4 (100%)), на 50% — у 2 (50%) и на 70% — у 1 (75%) пациента.
При клинической оценке тиреоидного статуса у пациентов, получавших инфликсимаб (n=4) исходно не наблюдалось нарушений функции щитовидной железы или повышенного уровня антител к щитовидной железе.
Через 6 месяцев лечения инфликсимабом у одного пациента впервые был диагностирован субклический гипотиреоз. У данного пациента эффект по критериям EULAR отсутствовал. Эффективость терапии по критериям ACR составила 20%. Возникновение субклинического гипотиреоза можно объяснить неэффективностью проводимой терапии вследствие того, что пациенту не были назначены БПВП из–за наличия противопоказаний. Инфликсимаб одобрен для применения при РА только в комбинации с БПВП.
Среди обследованных больных, начавших получать БПВП (n=21) было 18 (85,7%) женщин, 3 (14,3%) мужчин в возрасте 46 [33;52] лет с длительностью РА 0,2 [1,5;2] года. Серопозитивный РА был диагностирован у 15 (71,4%) пациентов, серонегативный – у 6 (28,6%). Медленно — прогрессирующее течение РА было у 13 (61,9%) пациентов, быстро-прогрессирующее – у 8 (38,1%). I рентгенологическая стадия РА установлена у 2 (9,5%) пациентов, II – у 14 (66,7%) пациентов, III – у 3 (14,3%) пациентов, IV – у 2 (9,5%) пациентов. Системные проявления РА были выявлены у 13 (61,9%) пациентов. Средняя степень активности РА была диагностирована у 5 (23,8%) больных, высокая – у 16 (76,2%) больных.
Изучение динамики активности заболевания по индексу DAS 28 показало его достоверное снижение через 6 месяцев от начала терапии (p<0,05) (табл. 3). Также на фоне терапии БПВП отмечена достоверная положительная динамика ЧБС, ЧПС, интенсивности боли и ОСЗП по ВАШ, длительности утренней скованности, СОЭ, СРБ и индекса HAQ (p<0,05).
Таблица 3. Динамика основных клинических и лабораторных показателей у больных РА на фоне терапии БПВП
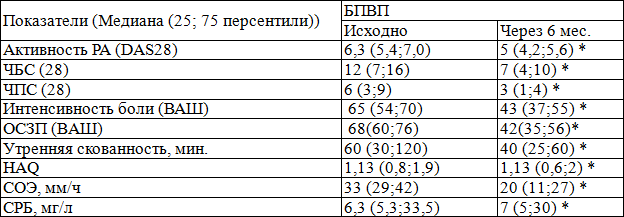
Примечание: * — р<0,05
Оценка эффективности терапии БПВП по критериям EULAR (рис. 1) показала, что через 6 месяцев лечения хороший эффект достигнут у 4 (19,0%) пациентов, удовлетворительный – у 8 (38,1%) пациентов, эффект не достигнут у 9 (42,9%) пациентов. Оценка эффективности терапии по критериям ACR (рис. 2) показала, что через 6 месяцев лечения уменьшение параметров на 20% отмечалось у 15 (71,4%) пациентов, на 50% — у 6 (28,6%) пациентов.
В начале исследования в группе пациентов, получавших БПВП (n=21) у 2 (9,5%) пациентов был диагностирован субклинический гипотиреоз; у 8 (38,1%) пациентов были выявлены повышенные уровни антител к щитовидной железе (у 2 (9,5%) пациентов – АТ к ТПО и АТ к ТГ, у 4 (19,0%) – только АТ к ТПО и у 2 (9,5%) – АТ к ТГ).
Через 6 месяцев лечения БПВП у одного пациента с субклическим гипотиреозом уровень ТТГ снизился незначительно. Отсутствовал эффект по критериям EULAR, было достигнуто 20% улучшение по ACR. У другого пациента с субклиническим гипотиреозом уровень ТТГ нормализовался. Пациент достиг хорошего эффекта по EULAR и 50% улучшения по ACR.
Через 6 месяцев лечения БПВП у пациента с исходно повышенным уровнем АТ к ТПО, впервые был диагностирован субклинический гипотиреоз, и произошло повышение уровня АТ к ТПО. У пациента не было эффекта по EULAR и по ACR.
У 2 пациентов с исходно высокими уровнями антител к щитовидной железе, уровень АТ к ТГ нормализовался. Уровень АТ к ТПО у пациента достигшего хорошего эффекта по EULAR и 50% улучшения по ACR снизился, а у пациента, не достигшего эффекта по EULAR и ACR, их уровень повысился.
На фоне лечения БПВП у всех пациентов с исходно высоким уровнем АТ к ТГ, их уровень нормализовался. При этом у пациентов отсутствовал эффект по EULAR, было достигнуто 20% улучшение по ACR.
Среди 3 пациентов с исходно высоким уровнем только АТ к ТПО, на фоне лечения у одного пациента уровень АТ к ТПО снизился, но повысился уровень АТ к ТГ, еще у одного пациента произошло снижение уровня АТ к ТПО, а у 3-го пациента уровень АТ к ТПО повысился. При этом первый пациент достиг удовлетворительного эффекта по EULAR и 50% улучшения по ACR, второй пациент достиг удовлетворительного эффекта по EULAR и 20% улучшения по ACR, третий пациент не достиг эффекта по EULAR и ACR.
Таким образом, на фоне улучшения клинических и лабораторных параметров РА произошло улучшение функции щитовидной железы и снижение уровня антител к щитовидной железе.
Заключение. Отмечено достоверное улучшение клинических и лабораторных параметров в группе пациентов, получающих ритуксимаб, тоцилизумаб, БПВП через 6 месяцев терапии (р<0,05). Улучшение клинико – лабораторных показателей было и в группе пациентов, получающих абатацепт и инфликсимаб (p>0,05).
При сравнительной оценке эффективности терапии между разными биологическими агентами по критериям EULAR и ACR различия в эффективности не были выявлены.
Проведенное исследование показало улучшение функции щитовидной железы у пациентов с исходно выявленным субклиническим гипотиреозом, снижение или нормализацию титра антител к щитовидной железе на фоне проводимой терапии.
Современная базисная терапия оказывает положительное влияние на функциональное состояние щитовидной железы у пациентов с РА.
Источник
