Все про подагру на
Над статьей доктора
Шестернина А. С.
работали
литературный редактор
Елена Бережная,
научный редактор
Сергей Федосов
Дата публикации 6 декабря 2017Обновлено 22 июля 2019
Определение болезни. Причины заболевания
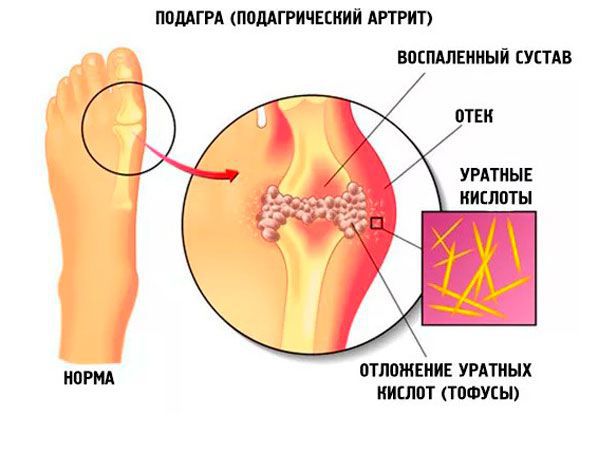
Подагра — системное заболевание, которое развивается в связи с воспалительным процессом, возникшим в месте отложения кристаллов моноурата натрия у людей с повышенным уровнем мочевой кислоты в сыворотке крови (более 360 мкмоль/л). Гиперурикемия возникает под воздействием как внешнесредовых, так и генетических факторов.

Заболеванию, как правило, подвержены мужчины, однако в последнее время оно выявляется и у слабого пола. Распространенность подагры растет, и это можно связать с ростом уровня жизни населения. Бессимптомная гиперурикемия встречается часто, однако далеко не всегда при этом развивается подагра.
На развитие подагры влияет:
- наследственность (предрасположенность к нарушению обмена пуринов);
- избыток в пище пуринов;
- нарушение функции почек, когда теряется их способность выводить мочевую кислоту (хроническая почечная недостаточность, поликистоз почек, гидронефроз, нефропатия в связи со злоупотреблением нестероидными противовоспалительными препаратами, при голодании);
- увеличение распада пуриновых нуклеотидов (цитостатическая терапия, лучевая и химиотерапия, хирургические вмешательства, гемолиз).[1][19]
Особенности современного течения подагры:
- значительный рост заболеваемости;
- увеличение частоты встречаемости у женщин;
- увеличение коморбидных состояний;
- начало заболевания в молодом возрасте.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением — это опасно для вашего здоровья!
Симптомы подагры
Подагра поражает опорно-двигательный аппарат и мочевыделительную систему. Возникает острый моноартрит, сопровождающийся нестерпимой, быстронарастающей и быстропроходящей за несколько часов или суток суставной болью, кожа над суставом краснеет, сам он увеличивается в объеме.
Из других симптомов — повышенная температура тела, слабость, потливость. При переходе в хроническую форму заболевания вокруг пораженных суставов образуются тофусы, суставы деформируются.
В почках образуются уратные камни, провоцируя тянущие боли в пояснице и периодическое появление крови в моче, никтурию (больше мочи выделяется ночью).[2][3]
Патогенез подагры
Поскольку образование уратов растет и нарушается выведение их почками, образуется избыток мочевой кислоты в крови, и происходит накопление уратов в тканях организма. Когда происходит отложение кристаллов моноурата в полости сустава, возникает воспалительный процесс из-за активации различных провоспалительных цитокинов. Кроме того, эти кристаллы откладываются в почечной ткани, приводя к развитию нефропатии и уратного нефролитиаза.[7]
Классификация и стадии развития подагры
3 стадии развития подагры:
- острый приступ подагрического артрита;
- межприступные периоды;
- хроническая тофусная подагра.[8]
Впервые подагрический приступ настигает пациента без предвестников, как правило, в возрасте от 40 до 50 лет, хотя известны случаи заболевания и в гораздо более молодом возрасте. Острая суставная боль, чаще в плюснефаланговом суставе большого пальца стопы (классический вариант начала), застает человека во второй половине ночи или в ранние утренние часы. Любое движение в суставе или прикосновение вызывает сильнейшую боль. Нарушение диеты, застолья с алкогольными напитками (алкоголь блокирует почку к выделению мочевой кислоты), хирургические вмешательства, инфекционные заболевания, повышенные нагрузки и травматизация сустава предшествуют возникновению приступа. Пациенты жалуются на покраснение пораженной области, ее припухание, сильную боль, общую слабость и недомогание, повышение температуры тела, потливость, разбитость, подавленность. Также характерными являются острые бурситы (препателлярный или локтевой сумки).[6]
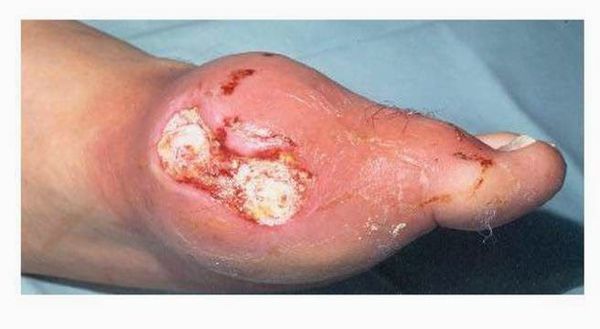
В течение нескольких дней (около недели) приступ самостоятельно проходит. Именно из-за этого подагра часто создаёт видимость доброкачественности: всё проходит (особенно в начале) самостоятельно, и проблема забывается до следующего обострения. На самом деле подагра при таком подходе может привести к разрушению и деформации суставов, хронической болезни почек. Далее при отсутствии адекватного контроля над заболеванием приступы учащаются, перестают проходить самостоятельно, проходят за больший промежуток времени. Позже человек вообще перестает чувствовать себя здоровым, а находится в состоянии затянувшегося приступа. В результате этого над областью пораженных суставов образуются безболезненные подкожные узелки с крошковидным, творожистым содержимым – тофусы (соли мочевой кислоты беловатого или желтоватого цвета). Излюбленное место расположения тофусов – область суставов кистей и стоп, ахиллово сухожилие, ушные раковины, голеностопные и локтевые суставы. При хронической тофусной подагре происходит разрушение хряща, что грозит деформацией, полным разрушением сустава и его анкилозом (полное заращение и отсутствие движений). Иногда тофусы могут самостоятельно вскрываться, а из них выделяется густое содержимое.[9][17]
Осложнения подагры
- образование тофусов;
- формирование деформаций и анкилозов суставов;
- нефролитиаз (камни в почках);
- депрессия как следствие постоянного болевого синдрома;
- повышение артериального давления, ишемическая болезнь сердца. Гиперурикемия связана с повышенным риском смерти от болезней сердечно-сосудистой системы;
- статистически значимо при подагре гораздо более часто встречаются сопутствующие заболевания (артериальная гипертензия, сахарный диабет, атеросклероз, гипертриглицеридемия — метаболический синдром).[10]
Диагностика подагры
Диагностические критерии подагры Wallace (предложены ААР в 1975 году, одобрены ВОЗ в 2002 году):
- наличие кристаллов мочевой кислоты в суставной жидкости;
- наличие тофусов, содержание кристаллов мочевой кислоты в которых подтверждено химически или поляризационной микроскопией;
- наличие 6 из 12 следующих признаков:
- типичная картина острой суставной атаки (один и более раз) в анамнезе;
- признаки воспаления наиболее выражены в первые сутки;
- воспаление одного сустава (моноартрит);
- покраснение кожи над пораженным суставом;
- припухание и боль в первом плюснефаланговом суставе;
- поражение первого плюснефалангового сустава с одной стороны;
- поражение суставов стопы с одной стороны;
- тофусы и образования, напоминающие их;
- лабораторные изменения (повышение уровня мочевой кислоты в крови);
- несимметричный отек суставов;
- кисты под кортикальным слоем кости без эрозий на рентгенографии;
- стерильная синовиальная жидкость.[13]
При пункции врач получает синовиальную жидкость, в которой под микроскопом обнаруживаются кристаллы моноурата натрия. Они могут обнаруживаться и в тофусе. Диагноз при этом можно установить со стопроцентной вероятностью. Ураты выглядят как иглообразные кристаллы с одним утонченным концом. В отсутствие поляризационного микроскопа диагноз основывается в основном на типичных клинических проявлениях подагры. Острый артрит, болевые ощущения при котором нарастают лавинообразно, появляется отек и покраснение пораженного сустава, является веским поводом подумать о подагре. Рентгенологическое исследование суставов на ранней стадии болезни малоинформативно. Изменения выявляются на поздней стадии. В частности, симптом «пробойника» (субкортикальные кисты) — типичный рентгенологический признак подагры — полезен для диагностики ее тофусных форм. Также при рентгенографии при подагре отсутствует околосуставной остеопороз, редко видим сужение суставной щели, часто выявляется остеолиз.[11]
Дифференциальная диагностика:
- гнойный артрит;
- болезнь отложения кристаллов пирофосфата кальция дигидрата;
- ревматоидный артрит;
- реактивный артрит;
- псориатический артрит;
- остеоартроз.
Стоит обратить внимание на то, что во время приступа уровень содержания мочевой кислоты в крови может быть нормальным, так как она в этот момент усиленно выводится почками. На ее уровень в крови не следует ориентироваться при постановке диагноза.
Лечение подагры
Нелекарственные методы:
- соблюдение диеты;
- ограничение употребления алкоголя;
- уменьшение избыточного веса.
Диета при подагре является довольно строгой, но выполнение диетических рекомендаций является залогом успешного лечения. Продукты, которые богаты пуринами, подлежат исключению или минимизации. Обильное щелочное питье помогает почкам избавиться от избытка мочевой кислоты в крови (почки — единственный орган, выводящий мочевую кислоту).
Начнем с главного источника пуринов — птицы и мяса. Курица — один из самых вредных видов птицы. Курице немного уступают (содержат меньше пуринов) утка и гусь. Индейка замыкает список, обладая самым низким содержанием пуринов среди птицы. Говядина — лидер среди мясных продуктов по содержанию пуринов, далее идут телятина и свинина, баранина.
Что касается рыбы, то самые вредные — лососевые виды, далее шпроты, килька, сардины, треска. Морские обитатели, живущие в раковинах (устрицы), являются самыми богатыми на пурины. Субпродукты также очень вредны (мозги, печень, легкие, почки), так же, как и холодец, мясные бульоны и соусы. Колбасу (любую) стоит полностью исключить из рациона. Не рекомендуются также: грибы и грибные бульоны, бобовые, щавель, яйца, шоколад, дрожжи, рис полированный, инжир, геркулес, капуста цветная, дрожжи. Алкогольные напитки запрещены (особое внимание пиву, вину, шампанскому).
Объем употребляемой за сутки жидкости — 2-2,5 литра. Рекомендовано щелочное питье: щелочная минеральная вода, вода с добавлением лимона, соки.
Теперь о бедных пуринами продуктах — как раз о тех, которые необходимо есть. Ими являются: молоко и молочные, молочнокислые продукты, многие овощи (капуста белокочанная, картофель, огурцы, помидоры, морковь, лук), орехи, фрукты, мучные изделия, крупы, мед, масло сливочное. Отварное мясо и рыбу рекомендуется есть 2-3 раза в неделю. Можно есть сало, так как жир почти не содержит пуринов. Некоторые исследования свидетельствуют, что 1,5 литра кофе в день приравнивается к 100 мг аллопуринола, а таккже известно, что вишня и черешня обладают гипоурикемическим действием.[4][15]
Лекарственные методы
Лечение приступа подагры:
- колхицин и нестероидные противовоспалительные препараты — это первое, чем стоит лечить приступ подагры. Колхицин является растительным препаратом (производное безвременника). При приеме колхицина довольно часто возникают побочные эффекты (рвота, жидкий стул, сильный дискомфорт в животе, синдром мальабсорбции, геморрагический энтероколит, редко возникает миелосупрессия и гиперкоагуляция), поэтому стоит строго придерживаться рекомендуемых дозировок. Нестероидные противовоспалительные препараты (ацеклофенак, нимесулид, диклофенак, эторикоксиб) стоит принимать в максимальных терапевтических дозировках — меньшие могут быть неэффективны. Анальгетики при подагре неэффективны;
- глюкокортикоиды внутрисуставно, внутрь или парентерально, когда противопоказан колхицин, нестероидные противовоспалительные препараты или же лечение ими неэффективно. Эти препараты дают выраженный эффект, но должны быть назначены только врачом, злоупотребление глюкокортикоидами имеет необратимые последствия (развитие сахарного диабета, неконтролируемая артериальная гипертензия и т. д.);
- канакинумаб (Иларис) — моноклональные антитела к интерлейкину-1, используются у пациентов с частыми приступами (более трех приступов за последний год), которые не могут принимать колхицин и НПВП.[12][20]
Лечение хроничекого подагрического артрита
Чтобы успешно лечить хроническую подагру, нужно предупредить образование и растворить уже имеющиеся кристаллы моноурата натрия, а для этого необходимо поддерживать уровень мочевой кислоты ниже 360 мкмоль/л.
- аллопуринол — урикодепрессор, доза подбирается индивидуально с врачом. При почечной недостаточности доза подбирается под особым контролем. Аллопуринол подлежит отмене во время приступа;[18]
- фебуксостат (аденурик) — используется при неэффективности аллопуринола, выводится печенью, является альтернативой для лечения пациентов с патологией почек;
- бензбромарон — блокирует обратное всасывание мочевой кислоты в канальцах почек и способствует ее выведению через почки и кишечник;
- пеглотиказа — раствор ферментов, который расщепляет подагрические соли, в РФ не зарегистрирован, применятся только при тяжелом течении подагры;
- первое время, для исключения повторных приступов, можно использовать колхицин (0,5-1,0 грамм в сутки).[5][16]
Пациенты подлежат диспансерному наблюдению у врача-ревматолога. Врач определяет периодичность контроля анализов, меняет (увеличивает или уменьшает) дозы получаемых препаратов, занимается лечением приступа. Противоподагрические средства принимаются длительное время. Также к лечению сопутствующей патологии могут быть подключены смежные специалисты (кардиолог, эндокринолог, уролог, нефролог). Пациент может быть госпитализирован в ревматологическое отделение при длительном по времени приступе, неэффективном лечении на амбулаторном этапе, а также для подбора постоянной терапии.
Прогноз. Профилактика
Прогноз зависит от своевременности и успешности начатого лечения, приверженности пациента к лечению, соблюдения диетических рекомендаций. По большей части прогноз благоприятный, но он ухудшается при развитии поражения почек, которое может стать даже причиной смерти пациента.
Строгое соблюдение диеты является основным моментом в профилактике приступов подагры. Необходимо ограничить употребление алкоголя, не принимать некоторые лекарства (мочегонные препараты из группы тиазидов и петлевые мочегонные, неселективные бета-блокаторы, аспирин, никотиновую кислоту, леводопу). Если пациент худеет, то следует опасаться быстрой потери веса. Нужно стараться избегать обезвоживания и тяжелых физических нагрузок, воздействия низких температур. В профилактических целях аллопуринол может быть назначен только пациентам, страдающим онкологическими заболеваниями и получающим химиотерапию.[14]
Источник
Пода́гра (др.-греч. ποδάγρα, буквально — капкан для ног; от πούς, ποδός — нога и ἄγρα — ловля, охота)[3] — метаболическое заболевание, которое характеризуется отложением в различных тканях организма кристаллов уратов в форме моноурата натрия или мочевой кислоты. В основе возникновения лежит накопление мочевой кислоты и уменьшение её выведения почками, что приводит к повышению концентрации последней в крови (гиперурикемия). Клинически подагра проявляется рецидивирующим острым артритом и образованием подагрических узлов — тофусов. Поражение почек также является одним из основных клинических проявлений подагры наряду с артритом.
Чаще заболевание встречается у мужчин, однако в последнее время возрастает распространённость заболевания среди женщин, с возрастом распространённость подагры увеличивается. Для лечения используются препараты, воздействующие на патогенетический механизм заболевания, а также препараты для симптоматического лечения.
История[править | править код]
«Подагра». Иллюстрация Джеймса Гилрея, 1799. Мастер карикатуры изобразил болевой синдром при подагре как демона или дракона
Подагра известна с глубокой древности. Первые документальные свидетельства заболевания известны из Древнего Египта и датируются 2600 годом до н. э.[4] Они основываются на описании подагрического артрита большого пальца[4]. Древнегреческий целитель и врач Гиппократ в V веке до н. э. описывал клинические симптомы подагрического артрита в своих «Афоризмах», где он отметил, что заболевание не встречается у евнухов и женщин до наступления менопаузы[5][6]. Римский философ и врач Авл Корнелий Цельс описывал взаимосвязь развития подагры с употреблением алкоголя и связанными с ней нарушениями работы почек[7]. В 150 году Гален указывал, что подагра обусловлена «распущенностью, несдержанностью и наследственностью»[8].
В конце XVII века английский врач-клиницист Томас Сиденгам, более 30 лет страдавший подагрой, классифицировал её как отдельную болезнь и весьма точно описал клиническую картину острого приступа подагрического артрита в работе «Трактат о подагре» (лат. «Tractatus de podagra et hydrope»). В нём он сравнивал болевой синдром при подагре с болями «от зажима конечности прессом» и описывал ощущения больного, сравнимые с тем, как «в палец впилась клыками огромная собака»[9]. В 1679 году голландский учёный Антони ван Левенгук впервые описал микроскопическое строение кристаллов мочевой кислоты[5].
В 1848 году английский физиолог Альфред Баринг Гаррод (Alfred Baring Garrod, 1819—1906) при помощи нитки, опущенной в кровь пациента, страдающего подагрой, открыл и описал факт повышения содержания мочевой кислоты в крови при этом заболевании[10][11][12].
Первые научные работы французского врача Жана Мартена Шарко относятся к области подагры: «Повреждения хряща при подагре» (фр. Les altérations des cartilages dans la gouite, 1858), «Подагрические отложения (тофусы) в наружном ухе у подагриков» (Les concrétions tophacées de l’oreille externe chez les goutteux, 1860), «Изменения в почках при подагре» (Les altérations du rein chez les goutteux, 1864), «О подагре и свинцовых отравлениях» (Les rapports de la goutte et de l’intoxication saturnine, 1864).
В 1899 году было обнаружено наличие кристаллов уратов в суставной жидкости во время приступа подагрического артрита. В 1961 году MacCarty и Hollander выявили роль кристаллов уратов в возникновении и развитии подагрического воспаления[13].
Исторически сложилось так, что со Средних веков и до XX века подагрой страдали преимущественно богатые и знатные люди, в связи с чем она носила название «болезнь королей»[4][14], «болезнь богачей» и «болезнь аристократов»[4]. Считалось, что она была связана с избыточным весом, перееданием (особенно злоупотреблением мясной пищей) и чрезмерным употреблением алкогольных напитков. К примеру, в 1739 году француз Эжен Мушрон (фр. Eugène Moucheron) издал брошюру под названием «О благородной подагре и сопровождающих её добродетелях», в которой воспевал подагру и отмечал, что это болезнь королей, принцев, выдающихся полководцев, умных и одарённых людей, а также приводил примеры коронованных особ, политических деятелей, людей искусства, страдавших подагрой[15]. Новая вспышка интереса к подагре возникла в начале XX века, когда Хавелок Эллис (англ. Henry Havelock Ellis, 1859—1939) опубликовал в 1927 году книгу под названием «История английского гения». В ней автор касался темы подагры и приводил в пример 55 известных выдающихся англичан, болеющих ею[16]. В 1955 году вышла работа Эгона Орована «The origin of man», опубликованная в журнале «Nature», в которой он описывал повышенную частоту болеющих подагрой среди гениев и объяснял её тем, что мочевая кислота структурно является весьма сходной с метилированными пуринами: кофеином, теофиллином и теобромином, являющимися стимуляторами умственной активности, оказывающими стимулирующее воздействие на высшие мозговые функции, в частности, концентрацию внимания и способность к концентрации. Орован указал, что мочевая кислота у всех развитых млекопитающих, за исключением человекообразных обезьян и человека, расщепляется под действием вырабатываемого в печени фермента уриказы до аллантоина, у приматов же, из-за отсутствия уриказы, она сохраняется в крови[16]
Эпидемиология[править | править код]
Гиперурикемия выявляется у 4—12 % населения, подагрой страдает 0,1 % населения России[17].
В США и Европе подагрой болеют 2 % жителей, среди мужчин в возрасте 55—65 лет подагрой болеют 4—6 %.
Соотношение мужчин к женщинам составляет от 7:1 до 19:1. Пик заболеваемости приходится на 40-50 лет у мужчин, 60 лет и старше у женщин. До менопаузы женщины заболевают редко, вероятно за счёт воздействия эстрогенов на экскрецию мочевой кислоты[17].
Частота подагрического артрита в различных популяциях колеблется и составляет от 5 до 50 на 1000 мужчин и 1-9 на 1000 женщин, а число новых случаев в год — соответственно 1−3 на 1000 у мужчин и 0,2 на 1000 у женщин[17]. За последнее десятилетие[когда?] частота случаев заболевания подагрой возросла[18].
Острый приступ подагры у подростков и молодых людей наблюдают редко, обычно он опосредован первичным или вторичным дефектом синтеза мочевой кислоты[17].
Этиология[править | править код]
Факторы развития заболевания[править | править код]
Существует целый ряд факторов риска, способствующих возникновению и развитию подагры у определённых лиц.
К факторам риска развития подагры относят артериальную гипертонию, гиперлипидемию, а также:
- повышенное поступление в организм пуриновых оснований, например, при употреблении большого количества красного мяса (особенно субпродуктов), некоторых сортов рыбы, какао, чая, шоколада, гороха, чечевицы, фруктозы, алкоголя (особенно пива, содержащего много гуанозина и ксантина — предшественников мочевой кислоты);
- увеличение количества пуриновых нуклеотидов при общем катаболизме (например при противоопухолевой терапии; массивном апоптозе у людей с аутоиммунными болезнями);
- торможение выведения мочевой кислоты с мочой (например при почечной недостаточности);
- повышенный синтез мочевой кислоты при одновременном снижении выведения её из организма (например, при злоупотреблении алкоголем, шоковых состояниях, гликогенозе с недостаточностью глюкозо-6-фосфатазы);
- наследственная предрасположенность (характер наследования всё ещё окончательно не выяснен).
Патогенез[править | править код]
В основе патогенеза заболевания находится повышение уровня мочевой кислоты в крови. Но данный симптом не является синонимом заболевания, так как гиперурикемия также наблюдается при других заболеваниях (болезни крови, опухоли, заболевания почек и т. д.), чрезвычайно высоких физических перегрузках и питании жирной пищей.
Выделяют минимум три основных элемента возникновения подагры:
- накопление мочекислых соединений в организме;
- отложение данных соединений в органах и тканях;
- развитие острых приступов воспаления в данных местах поражения, образования подагрических гранулем и подагрических «шишек» — тофусов, обычно вокруг суставов.
Симптомы и течение заболевания[править | править код]
Полная естественная эволюция подагры проходит четыре стадии:
- бессимптомная гиперурикемия;
- острый подагрический артрит;
- межкритический период;
- хронические подагрические отложения в суставах.
Нефролитиаз может развиться в любой стадии, кроме первой.
Наблюдается постоянно повышенная концентрация мочевой кислоты в плазме крови и в моче; воспаление суставов по типу моноартритов, что сопровождается сильной болью и лихорадкой; уролитиаз и рецидивирующие пиелонефриты, завершающиеся нефросклерозом и почечной недостаточностью.
Диагностика[править | править код]
Диагноз подагрического артрита может быть установлен на основании эпидемиологических критериев диагностики, принятых на третьем международном симпозиуме по исследованиям ревматических болезней, Нью-Йорк, 1966.
1. При химическом или микроскопическом выявлении кристаллов мочевой кислоты в синовиальной жидкости или отложении уратов в тканях.
2. При наличии двух или более таких критериев:
- чёткий анамнез и/или наблюдение хотя бы двух атак болевого припухания суставов конечностей (атаки, по меньшей мере, на ранних стадиях, должны начинаться внезапно с сильным болевым синдромом; на протяжении 1-2 недель должна наступать полная клиническая ремиссия);
- чёткий анамнез и/или наблюдение подагрической атаки (см. выше) с поражением большого пальца ноги;
- клинически доказанные тофусы; чёткий анамнез и/или наблюдение быстрой реакции на колхицин, то есть уменьшение объективных признаков воспаления на протяжении 48 часов после начала терапии.
Рентгеновское исследование не включено в список обязательных диагностических исследований, однако оно может показать тофусные отложения кристаллов и повреждение костной ткани в результате повторных воспалений. Рентгеновское исследование также может быть полезно для мониторирования влияния хронической подагры на суставы.
Выявления гиперурикемии недостаточно для установления диагноза, так как лишь 10 % лиц с гиперурикемией страдают подагрой[17].
Диагностические критерии подагры (ВОЗ 2000г)[править | править код]
I. Наличие характерных кристаллических уратов в суставной жидкости.
II. Наличие тофусов (доказанных), содержащих кристаллические ураты, подтверждённые химически или поляризационной микроскопией.
III. Наличие как минимум 6 из 12 ниже представленных признаков:
- более чем одна острая атака артрита в анамнезе;
- максимум воспаления сустава уже в первые сутки;
- моноартикулярный характер артрита;
- гиперемия кожи над поражённым суставом;
- припухание или боль, локализованные в I плюснефаланговом суставе;
- одностороннее поражение суставов свода стопы;
- узелковые образования, напоминающие тофусы;
- гиперурикемия;
- одностороннее поражение I плюснефалангового сустава;
- асимметричное припухание поражённого сустава;
- обнаружение на рентгенограммах субкортикальных кист без эрозий;
- отсутствие флоры в суставной жидкости.
Наиболее достоверны такие признаки, как острый или, реже, подострый артрит, обнаружение кристаллических уратов в синовиальной жидкости и наличие доказанных тофусов. Кристаллы уратов имеют вид палочек или тонких игл с обломанными или закруглёнными концами длиной около 10 мкм. Микрокристаллы уратов в синовиальной жидкости обнаруживаются как свободно лежащими, так и в нейтрофилах.
Дифференциальная диагностика[править | править код]
Подагру дифференцируют с сепсисом, который может протекать параллельно с ней, а также с другими микрокристаллическими артритами (кристаллассоциированными синовиитами прежде всего с хондрокальцинозом (в первую очередь с депозицией пирофосфата кальция — особенно у лиц пожилого возраста); реактивными, псориатическим и ревматоидным артритами.
Лечение[править | править код]
Больные подагрой, впервые выявленной или в периоде обострения заболевания, подлежат стационарному лечению в специализированных ревматологических отделениях областных или городских больниц. Больные подагрой в период ремиссии заболевания при условии назначения адекватной терапии могут находиться под надзором ревматолога, нефролога по месту жительства в районных поликлиниках. Ориентировочная продолжительность лечения в стационарных условиях (специализированные ревматологические отделения) — 7-14 суток при условии подбора адекватной эффективной терапии, улучшение клинических и лабораторных признаков заболевания.
На сегодняшний день, современная фармакология так и не смогла представить ни одного препарата, который одновременно был бы универсальным, и мог бы действительно решать вопрос лечения подагры.
Лечение при подагре предусматривает:
- по возможности быстрое и осторожное купирование острого приступа;
- профилактику рецидива острого подагрического артрита;
- профилактику или регресс осложнений болезни, вызванной отложением кристаллов однозамещенного урата натрия в суставах, почках и других тканях;
- профилактику или регресс сопутствующих симптомов, таких как ожирение, гипертриглицеридемия или гипертензия;
- профилактику образования мочекислых почечных камней.
Лечение при остром приступе подагры[править | править код]
При остром подагрическом артрите проводят противовоспалительное лечение. Чаще всего используют колхицин. Его назначают для приёма внутрь обычно в дозе 0,5 мг каждый час или 1 мг каждые 2 ч, и лечение продолжают до тех пор, пока: 1) не наступит облегчение состояния больного; 2) не появятся побочные реакции со стороны желудочно-кишечного тракта или 3) общая доза препарата не достигнет 6 мг на фоне отсутствия эффекта. Колхицин наиболее эффективен, если лечение начинают вскоре после появления симптомов. В первые 12 ч лечения состояние существенно улучшается более чем у 75 % больных. Однако у 80 % больных препарат вызывает побочные реакции со стороны желудочно-кишечного тракта, которые могут проявляться раньше клинического улучшения состояния или одновременно с ним. При приёме внутрь максимальный уровень колхицина в плазме достигается примерно через 2 ч. Следовательно, можно предположить, что его приём по 1,0 мг каждые 2 ч с меньшей вероятностью обусловит накопление токсичной дозы до проявления терапевтического эффекта. Поскольку, однако, терапевтическое действие связано с уровнем колхицина в лейкоцитах, а не в плазме, эффективность режима лечения требует дальнейшей оценки.
При внутривенном введении колхицина побочные эффекты со стороны желудочно-кишечного тракта не наступают, а состояние больного улучшается быстрее. После однократного введения уровень препарата в лейкоцитах повышается, оставаясь постоянным в течение 24 ч, и поддаётся определению даже спустя 10 сут. В качестве начальной дозы внутривенно следует вводить 2 мг, а затем, если необходимо, двукратно повторить введение по 1 мг с интервалом в 6 ч. При внутривенном введении колхицина следует соблюдать специальные предосторожности. Он оказывает раздражающее действие и при попадании в окружающие сосуд ткани может вызвать резкую боль и некроз. Важно помнить, что внутривенный путь введения требует аккуратности и что препарат следует разводить в 5—10 объёмах обычного солевого раствора, а вливание продолжать не менее 5 мин. Как при пероральном, так и при парентеральном введении колхицин может угнетать функцию костного мозга и вызывать алопецию, недостаточность печёночных клеток, психическую депрессию, судороги, восходящий паралич, угнетение дыхания и смерть. Токсические эффекты более вероятны у больных с патологией печени, костного мозга или почек, а также у получающих поддерживающие дозы колхицина. Во всех случаях дозу препарата необходимо уменьшить. Его не следует назначать больным с нейтропенией.
При остром подагрическом артрите эффективны и другие противовоспалительные средства, в том числе индометацин, фенилбутазон, напроксен, эторикоксиб и др.
Индометацин можно назначать для приёма внутрь в дозе 75 мг, после которой через каждые 6 ч больной должен получать по 50 мг; лечение этими дозами продолжается и на следующие сутки после исчезновения симптомов, затем дозу уменьшают до 50 мг каждые 8 ч (трижды) и до 25 мг каждые 8 ч (тоже трижды). К побочным эффектам индометацина относятся желудочно-кишечные расстройства, задержка натрия в организме и симптомы со стороны центральной нервной системы. Несмотря на то, что указанные дозы могут вызывать побочные эффекты почти у 60 % больных, индометацин переносится обычно легче, чем колхицин, и служит, вероятно, средством выбора при остром подагрическом артрите.
Препараты, стимулирующие экскрецию мочевой кислоты, и аллопуринол при остром приступе подагры неэффективны.
При острой подагре, особенно при противопоказаниях или неэффективности колхицина и нестероидных противовоспалительных средств, пользу приносит системное или местное (то есть внутрисуставное) введение глюкокортикоидов. Для системного введения, будь то пероральное или внутривенное, следует назначать умеренные дозы в течение нескольких дней, так как концентрация глюкокортикоидов быстро уменьшается и их действие прекращается. Внутрисуставное введение длительно действующего стероидного препарата (например гексацетонид триамцинолона в дозе 15—30 мг) может купировать приступ моноартрита или бурсита в течение 24—36 ч. Это лечение особенно целесообразно при невозможности использовать стандартную лекарственную схему.
Диета[править | править код]
Традиционные рекомендации по диете заключаются в ограничении потребления пуринов и алкоголя. К продуктам с высоким содержанием пуринов относятся мясные и рыбные продукты, а также чай, какао и кофе. Недавно также было показано, что снижение веса, достигаемое умеренным ограничением углеводов и калорийной пищи в сочетании с пропорциональным повышением белка и ненасыщенных жирных кислот, приводило у больных подагрой к значительному уменьшению уровня мочевой кислоты и дислипидемии[19].
См. также[править | править код]
- Артрит микрокристаллический
- Хондрокальциноз
- Ураты
- Мочевая кислота
- Тофус
Примечания[править | править код]
- ↑ 1 2 3 4 Monarch Disease Ontology release 2018-06-29sonu — 2018-06-29 — 2018.
- ↑ 1 2 3 4 база данных Disease ontology (англ.) — 2016.
- ↑ Подагра / В. Г. Барскова // Перу — Полуприцеп. — М. : Большая российская энциклопедия, 2014. — С. 524. — (Большая российская энциклопедия : [в 35 т.] / гл. ред. Ю. С. Осипов ; 2004—2017, т. 26). — ISBN 978-5-85270-363-7.
- ↑ 1 2 3 4 Richette P., Bardin T. Gout // Lancet. — January 2010. — Vol. 375, № 9711. — P. 318—328. — doi:10.1016/S0140-6736(09)60883-7. — PMID 19692116.
- ↑ 1 2 Pillinger M. H., Rosenthal P., Abeles A.M. Hyperuricemia and gout: new insights into pathogenesis and treatment // Bulletin of the NYU Hospital for Joint Diseases. — 2007. — Vol. 65, № 3. — P. 215–221. — PMID 17922673. Архивировано 16 декабря 2008 года.
- ↑ The Internet Classics Archive Aphorisms by Hippocrates. MIT.
- ↑ A. Cornelius Celsus. On Medicine. University of Chicago.
- ↑ Зилва Дж. Ф., Пэннелл П. Р. Клиническая химия в диагностике и лечении. — М.: Медицина, 1988. — 528 с. — ISBN 5-225-00220-X.
- ↑ Насонова В., Барскова В. Болезнь изобилия // Наука и жизнь. — 2004. — № 7.
- ↑ Garrod A. B. The nature and treatment of gout and rheumatic gout. — London: Walton and Maberly, 1859.
- ↑ Keitel W. The High Priest of gout – Sir Alfred Baring Garrod (1819–1907) // Z Rheumatol. — 2009. — Vol. 68, № 10. — P. 851—856. — doi:10.1007/s00393-009-0541-4. — PMID 19937040.
- ↑ Storey G. D. Alfred Baring Garrod (1819–1907) // Rheumatology (Oxford). — 2001. — Vol. 40, № 10. — P. 1189—1190. — doi:10.1093/rheumatology/40.10.1189. — PMID 11600751.
- ↑ McCarthy D. J., Hollander J. L. Identification of urate crystals in gouty synovial fluid. // Annals of Internal Medicine. — 1961. — Vol. 54. — P. 452.
- ↑ The Disease Of Kings — Forbes.com. Forbes.
- ↑ Засельский В., Лалаянц И. Природа гениальности // Огонёк. — 1996. — № 27. — С. 4.
- ↑ 1 2 Лалаянц И. Мочевая кислота бьёт в голову. Шишки гениальности следовало бы искать не на голове, а на ногах // Вокруг света. — 2008.
- ↑ 1 2 3 4 5 Под ред. С.Л. Насонова. Клинические рекомендации. Ревматология. — ГЭОТАР-Медиа, 2008. — С. 112—119. — 288 с. — ISBN 978-5-9704-0698-4.
- ↑ Lisa K. Stamp, Tony R. Merriman, Nicola Dalbeth. Gout (англ.) // The Lancet. — 2016-10-22. — Т. 388, вып. 10055. — С. 2039–2052. — ISSN 1474-547X 0140-6736, 1474-547X. — doi:10.1016/S0140-6736(16)00346-9.
- ↑ Барскова, В.Г. & Насонова, В.А. (2002), Подагра и синдром инсулинорезистентности, <https://medinfa.ru/article/31/117288/> Архивная копия от 1 февраля 2009 на Wayback Machine
Ссылки[править | править код]
- Мочевая кислота бьет в голову // Вокруг света
Источник
